Clear Sky Science · de
Somatische Mutationen und klonale Evolution in normalen Geweben und der Krebsentstehung
Verborgene Veränderungen in gesunden Zellen
Lange bevor ein Tumor im Scan sichtbar ist oder als Knoten tastbar wird, sammeln unsere Zellen im Stillen genetische Veränderungen an, während wir altern, auf die Umwelt reagieren und sich von täglicher Abnutzung erholen. Dieser Übersichtsartikel erklärt, wie sich diese unsichtbaren Veränderungen, sogenannte somatische Mutationen, in ansonsten normalen Geweben ansammeln, wie bestimmte Mutationen einigen Zellen einen Wettbewerbsvorteil verschaffen und wie langsame „klonale Evolution“ über Jahrzehnte schließlich die Voraussetzungen für Krebs schaffen kann. Das Verständnis dieser verborgenen Landschaft verändert die Vorstellungen darüber, wann Krebs tatsächlich beginnt und wie man ihn viel früher im Leben erkennen oder verhindern könnte.
Wie Wissenschaftler winzige Zellfamilien verfolgen
Normale Gewebe sind Mosaike vieler winziger Zellfamilien oder Klone, von denen die meisten zu klein für ältere Methoden sind. Der Review beschreibt neue Werkzeuge, mit denen Forschende DNA von sehr wenigen Zellen mit bemerkenswerter Präzision lesen können. Ein Ansatz ist das Herausschneiden winziger Gewebestücke mit laserbasierter Mikrodiskektion und das Sequenzieren aller darin enthaltenen DNA, was einen Schnappschuss der räumlichen Anordnung der Klone liefert. Ein anderer besteht darin, aus einzelnen Zellen miniature Versionen von Organen — sogenannte Organoide — zu züchten und deren Nachkommen zu sequenzieren, wodurch die persönliche Mutationsgeschichte jeder Zelle sichtbar wird. Eine dritte Strategie nutzt ultra-akkurate Sequenzierung, die seltene Mutationen in großen Zellgemischen finden kann, ohne dass diese gezüchtet werden müssen. Zusammengenommen zeigen diese Techniken, dass selbst „gesunde“ Gewebe voller Zellen mit krebsähnlichen Mutationen sind. 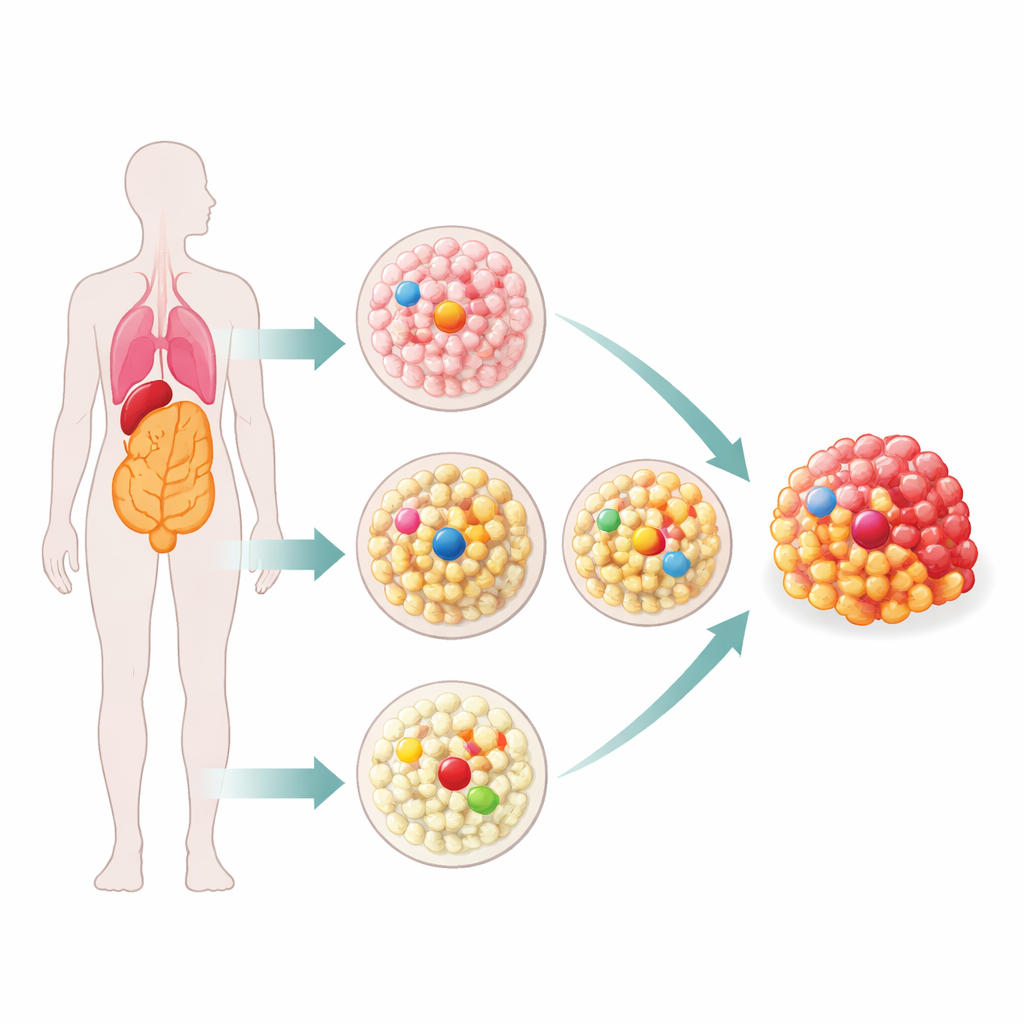
Warum Mutationen fortlaufend auftreten
Mutationen in normalen Zellen entstehen aus zwei grundlegenden Quellen: internem Verschleiß und äußeren Einwirkungen. Schon bei unseren allerersten Zellteilungen im Embryo ist die DNA-Kopie nicht perfekt, und chemische Reaktionen innerhalb der Zellen schädigen das genetische Material im Laufe der Zeit langsam. Diese altersbedingten Prozesse hinterlassen charakteristische „Signaturen“ in der DNA, die in vielen Organen zu sehen sind, sogar in langlebigen Zellen wie Neuronen und Muskelzellen. Darauf aufbauend fügen äußere Einflüsse wie Tabakrauch, Alkohol, ultraviolettes Licht, Entzündungen, bestimmte Infektionen und medizinische Behandlungen wie Chemotherapie eigene, erkennbare Muster der Schädigung hinzu. Menschen, die mit erblichen Schwächen in der DNA-Reparatur oder anderen Schutzsystemen geboren sind, können in normalen Geweben deutlich mehr Mutationen ansammeln, was erklärt, warum einige Familien ein deutlich höheres Krebsrisiko haben.
Wenn mutierte Zellen einen Vorteil erlangen
Die meisten Mutationen sind harmlose Mitläufer, doch einige verändern Schlüsselgene, die Wachstum, Überleben oder Reparatur steuern. Zellen mit solchen „Treiber“-Mutationen können einen kleinen, aber wichtigen Vorteil gegenüber ihren Nachbarn gewinnen, was ihrem Klon erlaubt zu expandieren. Im Blut beispielsweise werden Stammzellen mit bestimmten Treiber-Mutationen mit dem Alter häufiger — ein Zustand, der als klonale Hämatopoese bezeichnet wird und das Risiko für Blutkrebs sowie für einige Herz- und Lebererkrankungen erhöht. In vielen Oberflächengeweben — wie Haut, Speiseröhre, Atemwegen, Blase, Magen und Gebärmutter — breiten sich Bereiche von Zellen mit krebsassoziierten Treibern wie NOTCH1, TP53 oder PIK3CA über ansonsten normal aussehendes Gewebe aus. Häufig treten diese Mutationen überraschend früh im Leben auf, sogar in der Kindheit, und können große Gewebebereiche umgestalten, lange bevor unter dem Mikroskop eine präkanzeröse Läsion erkennbar ist.
Nicht alle Klone entwickeln sich in Richtung Krebs
Die klonale Evolution verläuft je nach Organ unterschiedlich, und ein vergrößerter Klon bedeutet nicht automatisch, dass Krebs folgt. In Strukturen wie Darm, Prostata und Leber leben Stammzellen in kleinen, räumlich getrennten Einheiten, was begrenzt, wie weit sich ein einzelner Klon ausbreiten kann. Einige Klone entstehen nicht zur Tumorförderung, sondern um Zellen beim Überleben von Stress zu helfen. Beispielsweise können Zellen bei chronischen Entzündungs- oder Stoffwechselerkrankungen Mutationen erwerben, die schädliche Signale abschwächen oder toxische Schäden reduzieren — eine Form der „adaptiven Rettung“. Andere Mutationen, etwa bestimmte Veränderungen im Notch-Signalweg der Speiseröhre, können sogar das Wachstum entstehender Tumoren verlangsamen, was darauf hindeutet, dass manche mutierten Klone vor Krebs schützen könnten. Nur ein kleiner Bruchteil der vielen Klone mit Treiber-Mutationen scheint zusätzlich die Alterationen zu erwerben, die nötig sind, um gefährlich zu werden.
Der lange Weg von der normalen Zelle zum Krebs
Indem sie Mutationsmuster aus normalem Gewebe, präkanzerösen Wucherungen und Tumoren derselben Person zusammensetzen, können Forschende nun grobe Zeitlinien der Krebsentstehung rekonstruieren. Bei Bluterkrankungen und Brustkrebs entstehen anfängliche Treiber-Mutationen oft Jahrzehnte vor der Diagnose, mit langsamem klonalem Wachstum, gefolgt von späteren Treffern, die schließlich die manifeste Krankheit auslösen. Dennoch bleiben zentrale Fragen offen: Welche Kombinationen von Mutationen und Umweltfaktoren schubsen einen Klon über die Schwelle, warum manche Hochrisiko-Klone nie fortschreiten und wie Änderungen der zellulären „Software“ (epigenetische Markierungen) mit DNA-Mutationen zusammenwirken. Mit verbesserten Werkzeugen könnte das Kartieren dieser verborgenen klonalen Geschichten bald Blut- oder Gewebetests ermöglichen, die riskante Klone früh aufspüren, Präventionsstrategien wie Rauchstopp oder Infektionskontrolle lenken und letztlich die Krebsmedizin dahin bewegen, Jahre vor der Tumorentstehung einzugreifen. 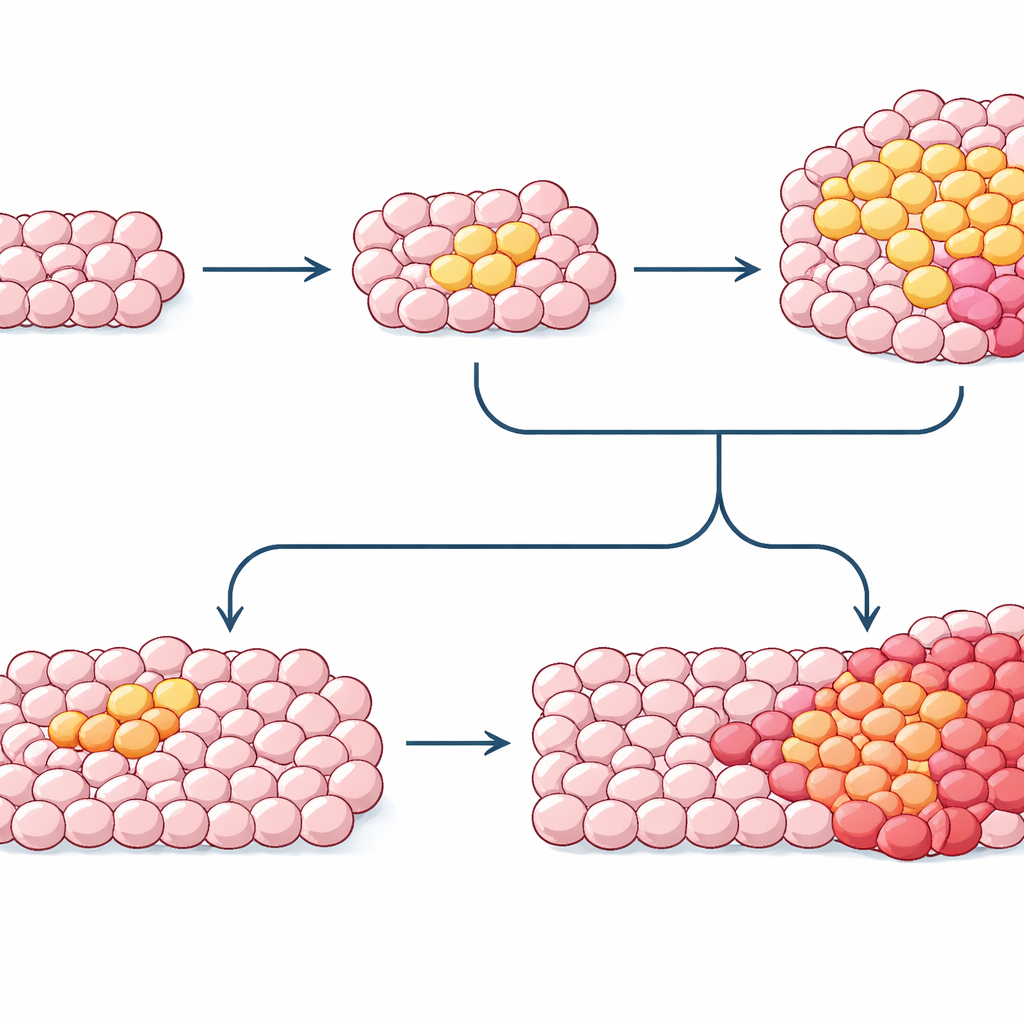
Was das für die tägliche Gesundheit bedeutet
Dieser Artikel zeigt, dass Krebs kein plötzliches Ereignis ist, sondern der Endpunkt eines langen, größtenteils stillen evolutionären Prozesses, der in normalen Geweben abläuft. Unsere Zellen verändern sich ständig, geprägt von Alter, Genen und Umwelt, und viele tragen Mutationen lange bevor eine Krankheit auftritt. Indem man versteht, welche Formen klonalen Wachstums gefährlich sind, welche harmlos oder sogar schützend sind und wie Lebensstil oder erbliche Faktoren das Gleichgewicht verschieben, hoffen Wissenschaftler, intelligentere Screening-Strategien zu entwickeln, Risikoschätzungen zu individualisieren und Wege zu finden, die zelluläre Evolution vom Krebs wegzulenken.
Zitation: Yoshida, K. Somatic mutations and clonal evolution in normal tissues and cancer development. Exp Mol Med 58, 961–969 (2026). https://doi.org/10.1038/s12276-025-01592-0
Schlüsselwörter: somatische Mutationen, klonale Evolution, normale Gewebe, Krebsrisiko, frühe Karzinogenese