Clear Sky Science · ar
الطفرات الجسدية والتطوّر الكلوني في الأنسجة السليمة وتكوّن السرطان
تغيّرات خفيّة داخل الخلايا السليمة
قبل وقت طويل من أن يظهر الورم في فحص أو يُشعر به ككتلة، تجمع خلايانا بصمت تغيّرات وراثية مع التقدّم في العمر واستجاباتنا للبيئة وشفاءنا من التلف اليومي. تشرح هذه المقالة الاستعراضية كيف تتراكم هذه التغيّرات غير المرئية، المسماة طفرات جسدية، في أنسجة تبدو طبيعية، وكيف تمنح بعض الطفرات خلايا محددة ميزة تنافسية، وكيف أن "التطوّر الكلوني" البطيء على مدى عقود يمكن أن يمهّد في النهاية لحدوث السرطان. إعادة تشكيل فهم هذا المشهد الخفي تغيّر الأفكار حول متى يبدأ السرطان فعلاً وكيف يمكن اكتشافه أو الوقاية منه في مراحل أبكر من الحياة.
كيف يتتبع العلماء عائلات الخلايا الدقيقة
الأنسجة السليمة عبارة عن فسيفساء من العديد من عائلات الخلايا الصغيرة، أو النسائل، ومعظمها صغير جدًا بحيث لا يمكن دراسته بالطرق القديمة. تصف المراجعة أدوات جديدة تتيح للباحثين قراءة الحمض النووي من عدد قليل جدًا من الخلايا بدقة ملحوظة. إحدى الطرق هي اقتطاع قطع نسيجية دقيقة باستخدام تفكيك بصري بالليزر وتسلسل كل الحمض النووي بداخلها، مما يعطي لقطة لكيفية ترتيب النسائل في الفراغ. طريقة أخرى هي زراعة نسخ مصغّرة من الأعضاء، تسمى الأُرْغِيّات، من خلية واحدة وتسلسل أحفادها، مكشوفة بذلك تاريخ الطفرات الخاص بكل خلية. استراتيجية ثالثة تستخدم تسلسلًا شديد الدقة يمكنه العثور على طفرات نادرة في مزيج كبير من الخلايا دون الحاجة إلى زراعتها. معًا تُظهر هذه التقنيات أن الأنسجة "السليمة" حتى هي مليئة بخلايا تحمل طفرات شبيهة بتلك المرتبطة بالسرطان. 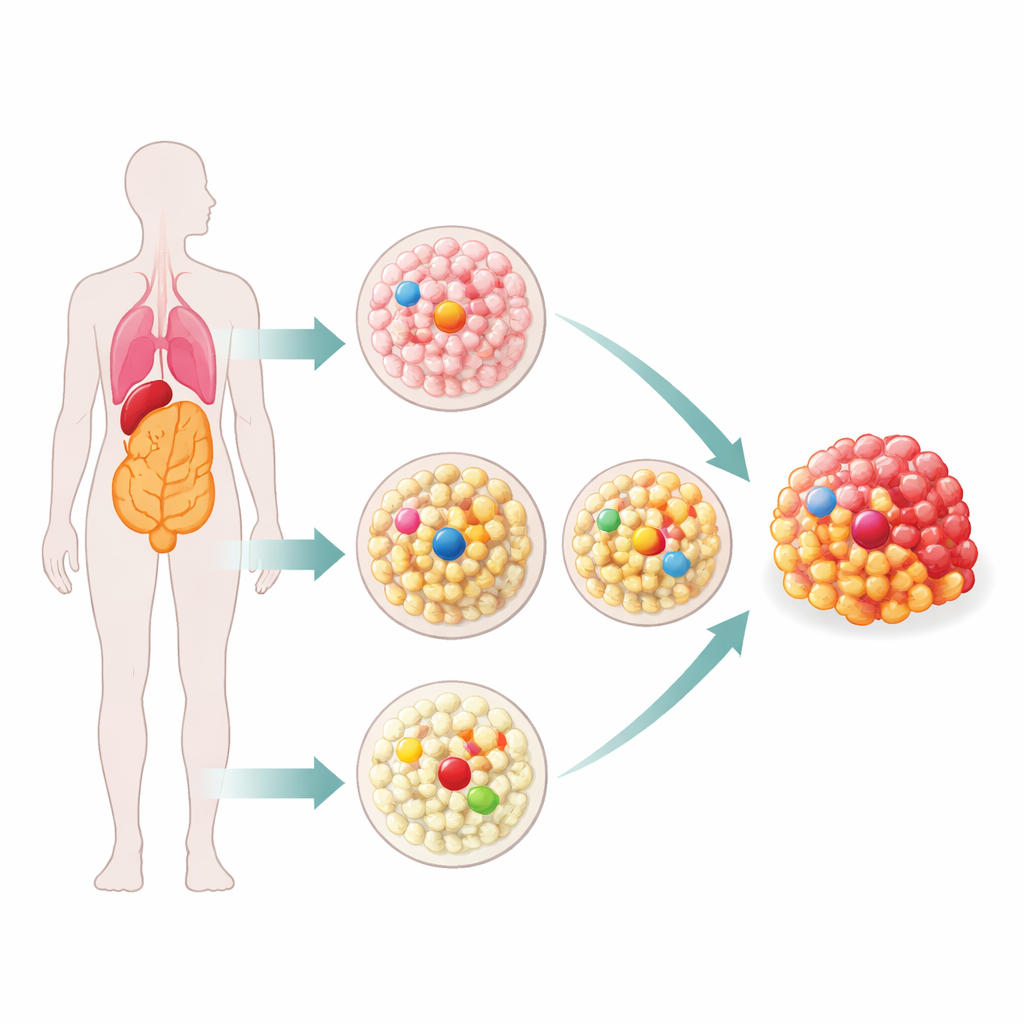
لماذا تستمر الطفرات في الظهور
تنشأ الطفرات في الخلايا السليمة من مصدرين عامين: التلف الداخلي والتعرّضات الخارجية. منذ انقسام الخلايا الأولى في الجنين، تكون عملية نسخ الحمض النووي غير مثالية، وتُحدث التفاعلات الكيميائية داخل الخلايا أضرارًا بطيئة للمادة الوراثية مع مرور الوقت. تترك هذه العمليات المرتبطة بالعمر "بصمات" مميزة في الحمض النووي تُرى عبر العديد من الأعضاء، حتى في الخلايا طويلة العمر مثل الخلايا العصبية والعضلية. بالإضافة إلى ذلك، تضيف المؤثرات الخارجية مثل دخان التبغ والكحول والأشعة فوق البنفسجية والالتهاب وبعض العدوى والعلاجات الطبية كالعلاج الكيميائي أنماط ضرر مميزة خاصة بها. الأشخاص المولودون بضعف وراثي في إصلاح الحمض النووي أو أنظمة الحماية الأخرى يمكن أن يتراكم لديهم عدد أكبر بكثير من الطفرات في الأنسجة السليمة، وهو ما يساعد على تفسير سبب ارتفاع مخاطر السرطان في بعض العائلات.
عندما تكسب الخلايا الطافرة ميزة
معظم الطفرات سرّية ولا تضر، لكن بعضها يغيّر جينات رئيسية تتحكم في النمو والبقاء والإصلاح. الخلايا الحاملة لهذه الطفرات "الدافعة" قد تكسب ميزة صغيرة لكنها مهمة على جيرانها، مما يسمح لنسيلتها بالتمدد. في الدم، على سبيل المثال، تصبح الخلايا الجذعية الحاملة لطفرات دافعة معينة أكثر شيوعًا مع التقدم في العمر، وهي حالة تُسمى التنسّج الكلوي للدم (clonal hematopoiesis) وتزيد من خطر أمراض الدم وبعض أمراض القلب والكبد. في العديد من الأنسجة السطحية — مثل الجلد والمريء والمجاري الهوائية والمثانة والمعدة والرحم — تنتشر بقع من الخلايا الحاملة لطفرات مرتبطة بالسرطان مثل NOTCH1 وTP53 أو PIK3CA في أنسجة تبدو طبيعية. غالبًا ما تظهر هذه الطفرات مبكرًا بشكل مفاجئ في الحياة، حتى في الطفولة، ويمكنها إعادة تشكيل مساحات كبيرة من النسيج قبل وقت طويل من ظهور أي آفة ما قبل سرطانية تحت المجهر.
ليس كل النسائل تتجه نحو السرطان
يتطوّر النسيل الكلوني بشكل مختلف من عضو لآخر، ولا يعني توسّع نسيل واحد بالضرورة أنه سيتبعه سرطان. في تراكيب مثل القولون والبروستات والكبد، تعيش الخلايا الجذعية في وحدات صغيرة ومنفصلة ماديًا، مما يحد من مدى انتشار أي نسيلة واحدة. بعض النسائل تنشأ ليس لتعزيز الأورام بل لمساعدة الخلايا على البقاء تحت الضغط. على سبيل المثال، في الأمراض الالتهابية أو الأيضية المزمنة، قد تكتسب الخلايا طفرات تُضعِف إشارات ضارة أو تقلل التلف السام، وهو شكل من "الإنقاذ التكيفي". طفرات أخرى، مثل تغييرات معينة في مسار Notch بالمريء، قد تبطئ حتى نمو الأورام الناشئة، مما يلمّح إلى أن بعض النسائل الطافرة قد تحمي من السرطان. فقط جزء صغير من العديد من النسائل الحاملة لطفرات دافعة يبدو أنه يكتسب التغيرات الإضافية اللازمة ليصبح خطيرًا.
الطريق الطويل من الخلية السليمة إلى السرطان
من خلال تجميع أنماط الطفرات من الأنسجة السليمة والنموّات ما قبل السرطانية والأورام في نفس الشخص، يمكن للباحثين الآن إعادة بناء جداول زمنية تقريبية لتطوّر السرطان. في اضطرابات الدم وسرطان الثدي، تنشأ الطفرات الدافعة الأولى غالبًا قبل عقود من التشخيص، مع نمو نسلي بطيء يتبعه ضروب لاحقة تُشعل المرض الظاهر. ومع ذلك تبقى أسئلة رئيسية: أي توافقيات من الطفرات والعوامل البيئية تدفع نسيلةً ما إلى الانزلاق نحو الخطر، لماذا لا تتقدم بعض النسائل عالية المخاطر، وكيف تتفاعل تغيّرات "برمجية" الخلية (العلامات فوق الجينية) مع طفرات الحمض النووي. مع تحسّن الأدوات، قد يتيح رسم هذه التاريخات الكلونية الخفية اختبارات دموية أو نسيجية تكشف النسائل عالية الخطر مبكرًا، وتوجّه استراتيجيات الوقاية مثل الإقلاع عن التدخين أو مكافحة العدوى، وفي النهاية تحوّل طب السرطان نحو التدخل قبل سنوات من تكوّن الورم. 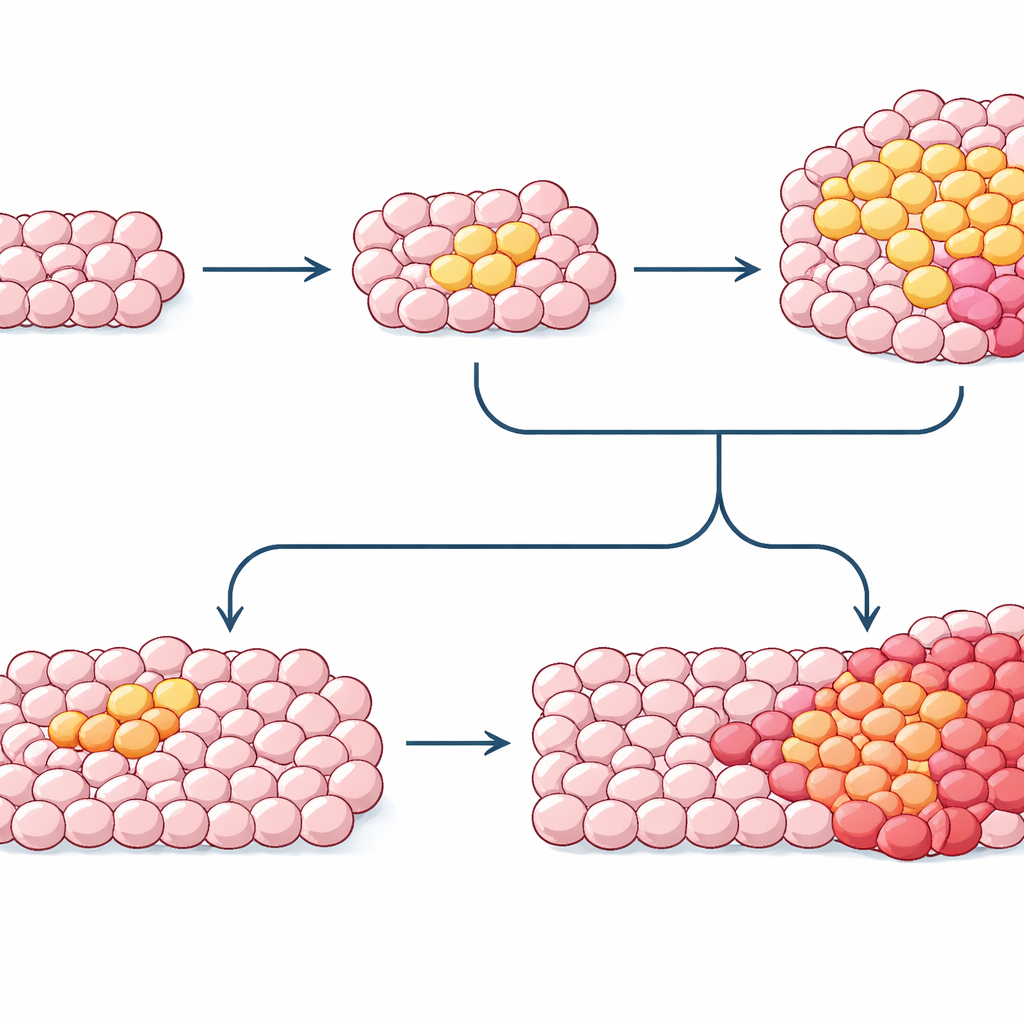
ما معنى هذا لصحتنا اليومية
تُظهر هذه المقالة أن السرطان ليس حدثًا مفاجئًا بل نقطة نهاية لعملية تطورية طويلة ومعظمها صامتة تحدث داخل الأنسجة السليمة. خلايانا تتغير باستمرار بتأثير العمر والجينات والبيئة، ويحمل الكثير منها طفرات قبل ظهور أي مرض. من خلال معرفة أي أشكال النمو الكلوني خطرة، وأيها بلا ضرر أو حتى وقائي، وكيف تميل العوامل الحياتية أو الوراثية التوازن، يأمل العلماء في تصميم فحوصات أذكى، وتخصيص تقديرات المخاطر وتطوير طرق لتوجيه التطور الخلوي بعيدًا عن السرطان.
الاستشهاد: Yoshida, K. Somatic mutations and clonal evolution in normal tissues and cancer development. Exp Mol Med 58, 961–969 (2026). https://doi.org/10.1038/s12276-025-01592-0
الكلمات المفتاحية: الطفرات الجسدية, التطوّر الكلوني, الأنسجة السليمة, مخاطر السرطان, البداية المبكرة للسرطان