Clear Sky Science · tr
Acinetobacter baumannii’nin kapsüler polisakkaritleri antimikrobiyal direnç ve doğal bağışıklık tepkisini değiştirir
Neden hastane mikropları koruyucu bir örtü giyer
Modern hastanelerde inatçı bir mikrop kötü şöhrete sahip: birçok antibiyotiğe dirençli ve tıbbi ekipman üzerinde uzun süre kalan Acinetobacter baumannii. Bu çalışma, kapsül adı verilen şeker moleküllerinden oluşan yapışkan dış katmanını inceliyor ve basit ama önemli bir soruyu soruyor: bu örtü mikrobu sadece gizliyor mu, yoksa ilaçlara ve vücudun ilk savunma hattına karşı aktif olarak hayatta kalmasına yardımcı mı oluyor?
Tehlikeli bir mikrop etrafında şekerli bir kalkan
A. baumannii sıklıkla yoğun bakım ünitelerindeki kişileri enfekte ederek pnömoni, kan dolaşımı ve idrar yolu enfeksiyonlarına yol açar. Birçok suş çoklu antibiyotiklere dirençli olduğundan, hekimler güçlü dezenfektanlara, deterjanlara ve hatta ışık temelli yöntemlere de güvenir. Araştırmacılar birçok bu bakteriyi çevreleyen kalın, şekerli bir tabaka olan kapsüle odaklandı. Klinik tipik bir suşu, kapsül üretemeyecek şekilde genetik olarak değiştirilmiş neredeyse özdeş bir versiyonla karşılaştırdılar. Bu, mikrobu güçlü kılan özelliklerin ne kadarının özellikle bu dış katmandan kaynaklandığını sorma imkanı verdi.
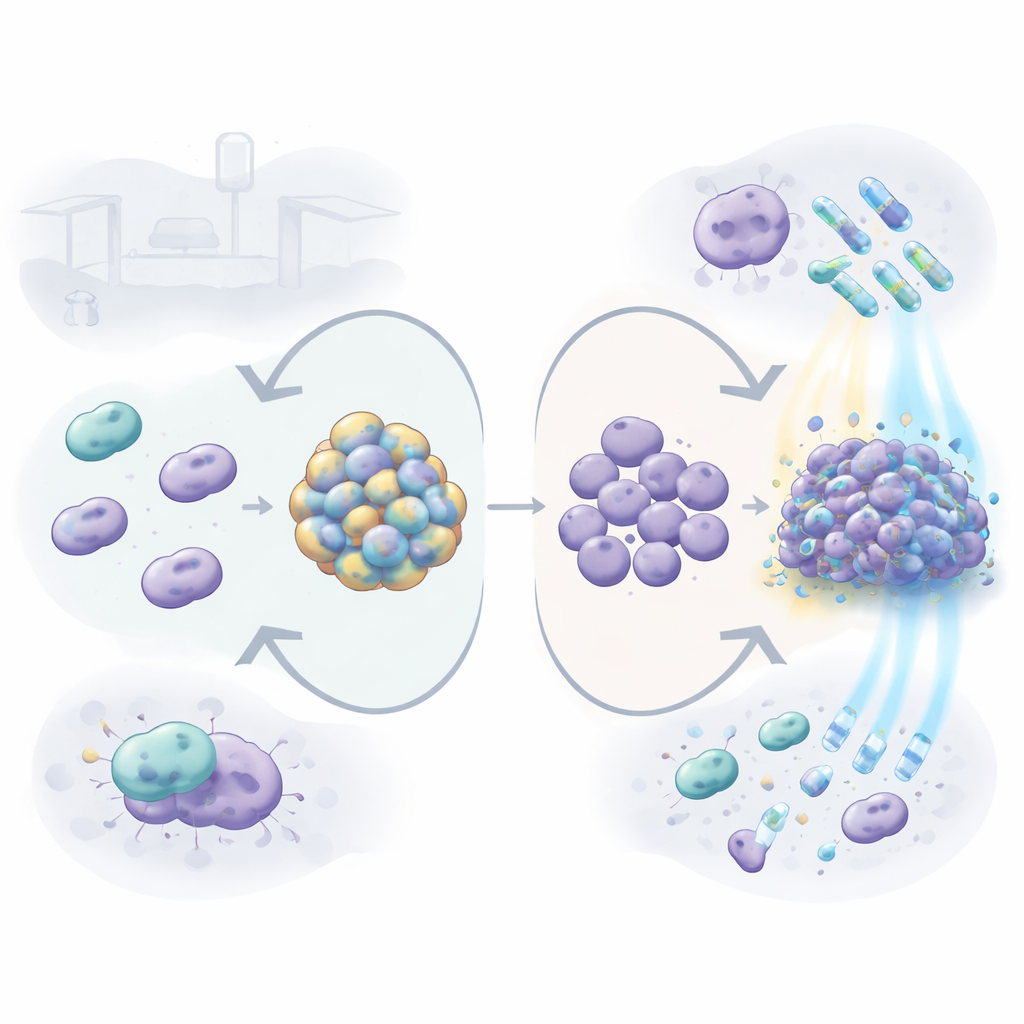
Örtü, hastane yüzeylerinde hayatta kalmayı nasıl değiştiriyor
Kapsül çıkarıldığında, serbest yüzen (planktonik) bakteriler hastanelerde yaygın olarak kullanılan bazı ilaçlara ve temizleyicilere karşı daha savunmasız hale geldi; bunlar arasında gentamisin, tetrasiklin, kolistin ve deterjan SDS yer aldı. Başka bir deyişle, örtüsüz halde mikrop öldürülmesi daha kolaydı. Ancak hikâye bakteriler biyofilm oluşturduğunda değişti—kateter veya ventilatör tüplerinde oluşturduklarına benzeyen plastik yüzeylerde yapışkan tabakalar. Kapsülsüz mutant çok daha kalın bir biyofilm üreterek ekstraselüler DNA gibi materyaller açısından zenginleşti. Bu yoğun topluluklar özellikle kolistin, klorheksidin ve hidrojen peroksit gibi bazı tedavilere, normal yani kaplı suş tarafından yapılan biyofilmden daha iyi direnç gösterdi. Bu, dış örtü eksik olduğunda bakterinin güçlendirilmiş ortak bir barınak inşa ederek telafi edebileceğini düşündürüyor.
Işık temelli tedavi ve kan bileşenleri
Araştırma ekibi ayrıca zararsız bir boya (klorofilin) ve mavi ışık kullanarak ihtiyaç duyulduğunda toksik oksijen türleri üreten fotodinamik terapi adlı umut verici alternatif yaklaşımı test etti. Burada da kapsül mikrobu korudu: örtüden yoksun bakteriler hem serbest hücreler hem de biyofilmler halinde bu ışık temelli saldırıya 10 ila 100 kat daha duyarlıydı. Araştırmacılar daha sonra yüzeylerden vücut benzeri bir ortama geçerek bakterileri kan serumu içinde büyüttü ve onları bağışıklık hücrelerine maruz bıraktı. Aktif serumda kapsülsüz mutant neredeyse büyüyemedi ve zayıf biyofilm oluşturdu; oysa kaplı suş gelişti; bu, kapsülün normalde mikrop temizlemeye yardımcı olan kan bileşenlerine karşı koruma sağladığını gösteriyor. Makrofajlara—bağışıklık sisteminin profesyonel “yutan” hücreleri—eklendiklerinde mutant çok daha kolay yutularak öldürüldü. Aynı zamanda kapsül üretimi için gerekli gen birçok stres koşulunda, antibiyotikler, dezenfektanlar, mavi ışık, serum ve makrofajlara maruz kalma dahil olmak üzere, daha aktif hale geldi; bu da bakterinin tehdit altındayken örtüsünü aktif olarak güçlendirdiğini gösteriyor.
Bağışıklık yanıtını susturma ve yönlendirme
Kapsülün inflamasyon üzerindeki etkisini anlamak için yazarlar fare ve insan hücrelerini kaplı veya kaplı olmayan suşlarla enfekte etti. Her ikisi de bağışıklık tepkilerini tetikledi, ancak kapsülsüz mutant genelde IL-6 ve IL-1β gibi iltihaplanma habercileri için daha güçlü sinyaller oluşturdu. Makrofajlarda normal kaplı suş, kontrollü ve görece sessiz bir hücre ölümü biçimi olan apoptozla ilişkilendirilen kaspaz-3 proteini daha güçlü biçimde aktive etti; oysa mutant tepkileri daha iltihaplı yolaklara kaydırıyor gibiydi. Araştırma ekibi kapsül materyalini izole edip herhangi bir bakteri olmadan bağışıklık hücrelerine eklediğinde, beklenmedik biçimde bu materyal uyarıcı olarak davrandı; birkaç iltihaplı molekülün üretimini artırdı ve insan nötrofillerini doz-bağımlı şekilde bir zar üzerinden çekti. Bakterilerin saldığı küçük dış zar vezikülleri (veziküller) de yüzeylerinde kapsül taşıdıklarında daha az iltihap uyandırdı; bu, şekerli örtünün diğer, daha alarm verici bakteriyel yapıları maskeleyebileceğini düşündürüyor.
Gelecekteki tedaviler için bunun anlamı
Genel olarak çalışma, A. baumannii kapsülünün pasif bir örtüden daha fazlası olduğunu gösteriyor. Tek hücreleri antibiyotiklerden, dezenfektanlardan, kan bileşenlerinden, mavi ışık tedavisinden ve bağışıklık saldırısından koruyor; aynı zamanda bazı inflamatuar sinyalleri yatıştırıyor ve bağışıklık hücrelerini daha sessiz yanıt biçimlerine yönlendiriyor. Yine de kapsül çıkarıldığında bakteriler belirli ajanlara dirençli daha kalın biyofilm oluşturabilir ve dökülen kapsül parçaları kendileri bağışıklık hücrelerini çekip inflamasyonu körükleyebilir. Gelecekteki terapiler açısından bu, kapsülü soyan ilaçlar veya enzimlerin enfeksiyonların temizlenmesine yardımcı olabileceği anlamına geliyor—ancak yalnızca ortaya çıkan biyofilmleri nüfuz edebilecek ve yeni ortaya çıkan kapsülsüz bakterilerden yararlanabilecek diğer tedavilerle akıllıca birleştirildiklerinde.
Atıf: Klimkaite, L., Kukanauskaite, G., Naujalis, J. et al. Capsular polysaccharides of Acinetobacter baumannii modulate antimicrobial resistance and innate immune response. Sci Rep 16, 14478 (2026). https://doi.org/10.1038/s41598-026-44001-w
Anahtar kelimeler: Acinetobacter baumannii, bakteriyel kapsül, biyofilm, antibiyotik direnci, doğal bağışıklık