Clear Sky Science · sv
Kapsulära polysackarider hos Acinetobacter baumannii påverkar antibiotikaresistens och det medfödda immunsvaret
Varför sjukhusbakterier bär en skyddande mantel
I moderna sjukhus har en enveten bakterie blivit ett ökänd problem: Acinetobacter baumannii, en bakterie som står emot många antibiotika och dröjer kvar på medicinsk utrustning. Denna studie granskar dess slemmiga yttre skikt, gjort av sockermolekyler kallade en kapsel, och ställer en enkel fråga med stora konsekvenser: döljer detta skikt bara bakterien, eller hjälper det aktivt den att överleva läkemedel och kroppens första försvarslinje?
Ett socker-skydd runt en farlig bakterie
A. baumannii infekterar ofta patienter på intensivvårdsavdelningar och orsakar pneumoni, blod- och urinvägsinfektioner. Många stammar är resistenta mot flera antibiotika, så läkare förlitar sig också på starka desinfektionsmedel, rengöringsmedel och till och med ljustekniker för att kontrollera spridningen. Forskarna fokuserade på kapseln, ett tjockt, sockerrikt lager som omsluter många av dessa bakterier. De jämförde en typisk klinisk stam med en nästan identisk variant som genetiskt modifierats så att den inte längre kunde bilda kapseln. Det gjorde det möjligt att undersöka hur mycket av bakteriens uthållighet som specifikt beror på det yttre skiktet.
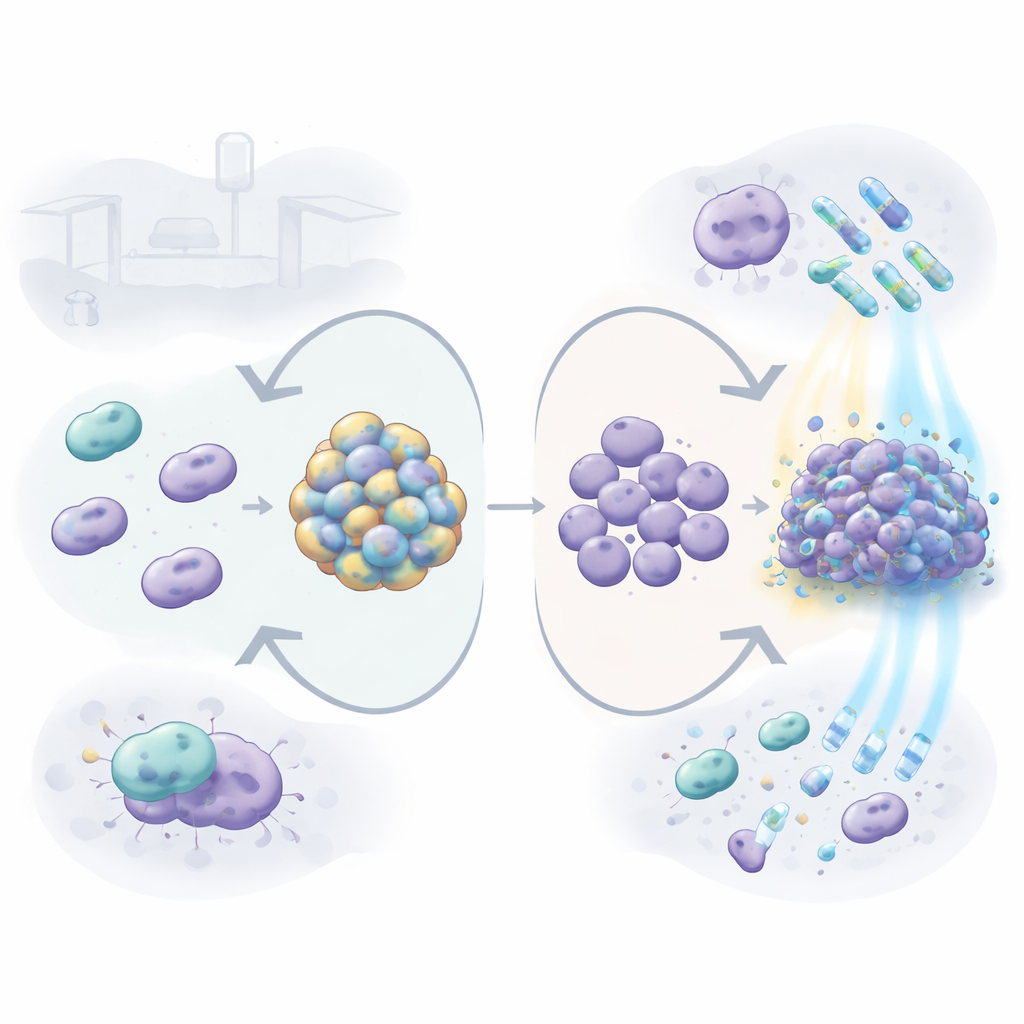
Hur manteln påverkar överlevnad på sjukhusytor
När kapseln togs bort blev fritt simmande (planktoniska) bakterier mer känsliga för flera läkemedel och rengöringsmedel som ofta används på sjukhus, inklusive antibiotika som gentamicin, tetracyklin och colistin, samt tvättmedlet SDS. Med andra ord var bakterien lättare att döda utan sin mantel. Men bilden ändrades när bakterierna bildade biofilmer — klibbiga lager på plastytor som liknar dem de bildar på katetrar eller ventilatorrör. Den kapsel-fria mutanten svarade genom att bilda en mycket tjockare biofilm, rik på extracellulärt material såsom DNA. Dessa täta samhällen visade sig motstå vissa behandlingar, särskilt colistin, klorhexidin och väteperoxid, bättre än biofilmer från den normala, kapselklädda stammen. Det tyder på att när det yttre skiktet saknas kan bakterien kompensera genom att bygga ett förstärkt gemensamt skydd.
Ljusterapi och blodkomponenter
Teamet testade också en lovande alternativ metod kallad fotodynamisk terapi, som använder ett ofarligt färgämne (klorofyllin) och blått ljus för att framkalla giftiga syremolekyler vid behov. Även här gynnade kapseln bakterien: bakterier utan mantel var 10–100 gånger mer känsliga för denna ljusdrivna attack, både som fria celler och som biofilmer. Forskarna gick sedan från ytor till en mer kroppslik miljö, odlande bakterierna i blodserum och exponera dem för immunceller. I aktivt serum växte den kapsel-fria mutanten knappt och bildade svaga biofilmer, medan den kapselklädda stammen trivdes, vilket visar att kapseln skyddar mot molekyler i blodet som normalt hjälper till att rensa bort mikrober. När bakterierna tillsattes till makrofager — immunsystemets professionella "ätarceller" — svaldes och dödades mutanten mycket lättare. Samtidigt ökade aktiviteten i genen som behövs för kapselproduktion under många stressförhållanden, inklusive exponering för antibiotika, desinfektionsmedel, blått ljus, serum och makrofager, vilket visar att bakterien aktivt förstärker sitt skikt när den hotas.
Tysta och omdirigera immunsvaret
För att förstå hur kapseln påverkar inflammation infekterade författarna mus- och humana celler med antingen den kapselklädda eller den oklädda stammen. Båda utlöste immunreaktioner, men den kapsel-fria mutanten framkallade i allmänhet starkare signaler för inflammatoriska budbärare såsom IL-6 och IL-1β. I makrofager aktiverade den normala kapselklädda stammen kraftigare caspas-3, ett protein kopplat till en kontrollerad, relativt tyst form av celldöd kallad apoptos, medan mutanten verkade luta svaren mot mer inflammatoriska vägar. När teamet renade kapselmaterialet och tillsatte det till immunceller utan några bakterier närvarande, agerade det oväntat som en stimulans, ökade produktionen av flera inflammatoriska molekyler och lockade mänskliga neutrofiler över ett membran på ett dosberoende sätt. Små ytbubblor (vesiklar) som frisätts av bakterierna var också mindre inflammatoriska när de bar kapsel på ytan, vilket tyder på att det sockerrika skiktet kan dölja andra, mer alarmerande bakteriestrukturer.
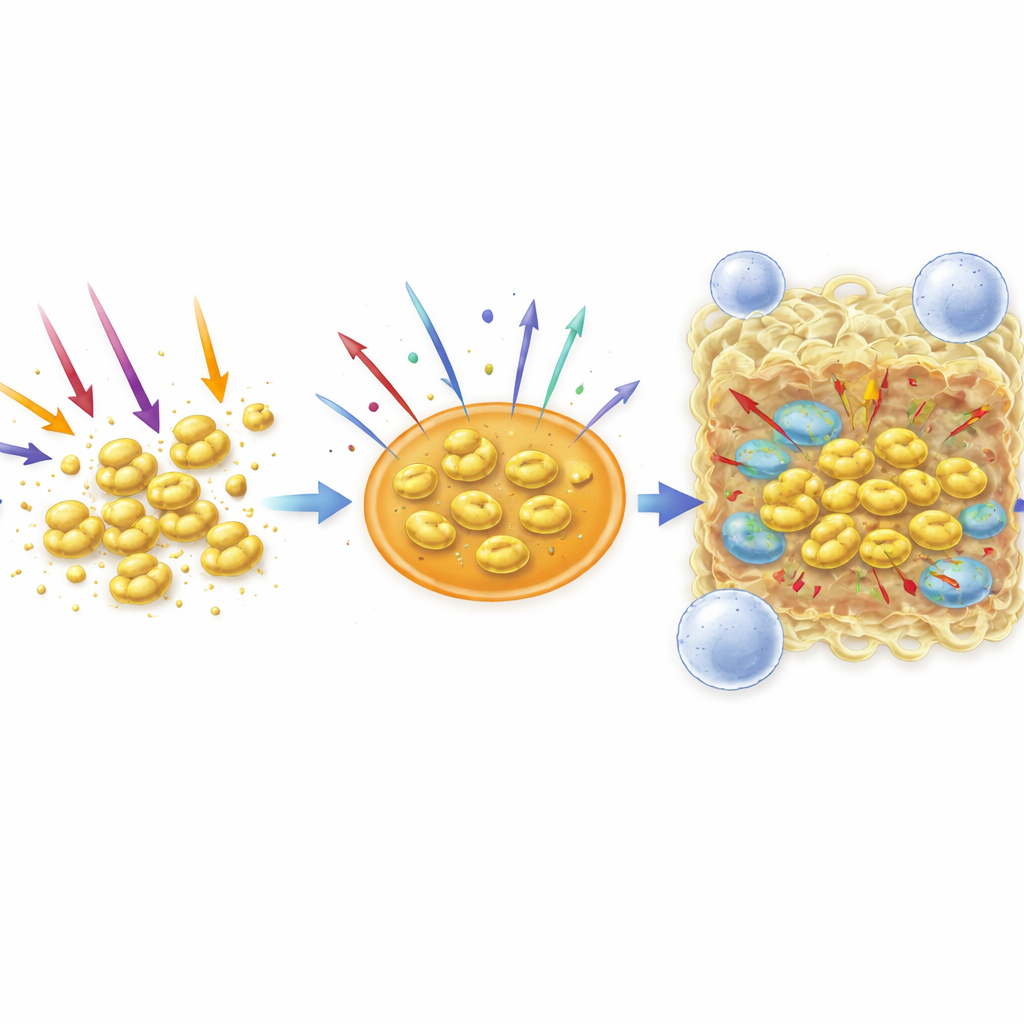
Vad detta betyder för framtida behandlingar
Sammantaget visar studien att kapseln hos A. baumannii är mer än en passiv mantel. Den skyddar enskilda celler från antibiotika, desinfektionsmedel, blodkomponenter, blåljusbehandling och immunsvar, samtidigt som den dämpar vissa inflammatoriska signaler och styr immunceller mot tystare svar. Men när kapseln tas bort kan bakterier bygga tjockare biofilmer som motstår vissa medel, och delar av avkastad kapsel kan själva dra till sig immunceller och elda på inflammation. För framtida terapier innebär detta att läkemedel eller enzymer som syftar till att avlägsna kapseln skulle kunna hjälpa kroppen att rensa dessa infektioner — men endast om de kombineras klokt med andra behandlingar som kan tränga igenom de resulterande biofilmerna och utnyttja de nyligen exponerade bakterierna.
Citering: Klimkaite, L., Kukanauskaite, G., Naujalis, J. et al. Capsular polysaccharides of Acinetobacter baumannii modulate antimicrobial resistance and innate immune response. Sci Rep 16, 14478 (2026). https://doi.org/10.1038/s41598-026-44001-w
Nyckelord: Acinetobacter baumannii, bakteriekapsel, biofilmer, antibiotikaresistens, medfött immunförsvar