Clear Sky Science · it
I polisaccaridi capsulari di Acinetobacter baumannii modulano la resistenza agli antimicrobici e la risposta immunitaria innata
Perché i germi ospedalieri indossano un manto protettivo
Nei reparti ospedalieri moderni, un germe ostinato è diventato un noto problema: Acinetobacter baumannii, un batterio che resiste a molti antibiotici e persiste sulle attrezzature mediche. Questo studio esamina il suo rivestimento esterno vischioso, costituito da molecole di zucchero chiamate capsula, e pone una domanda semplice ma dalle grandi conseguenze: questo manto nasconde soltanto il germe, o lo aiuta attivamente a sopravvivere ai farmaci e alla prima linea di difesa del corpo?
Uno scudo zuccherino attorno a un germe pericoloso
A. baumannii infetta spesso persone nelle terapie intensive, causando polmoniti, infezioni del sangue e urinarie. Molti ceppi sono resistenti a più antibiotici, perciò i medici si affidano anche a disinfettanti potenti, detergenti e persino a metodi basati sulla luce per contenerlo. I ricercatori si sono concentrati sulla capsula, uno spesso strato zuccherino che circonda molti di questi batteri. Hanno confrontato un ceppo clinico tipico con una versione quasi identica alterata geneticamente in modo da non poter più produrre questa capsula. Ciò ha permesso di capire quanto della robustezza del germe dipenda specificamente da quel rivestimento esterno.
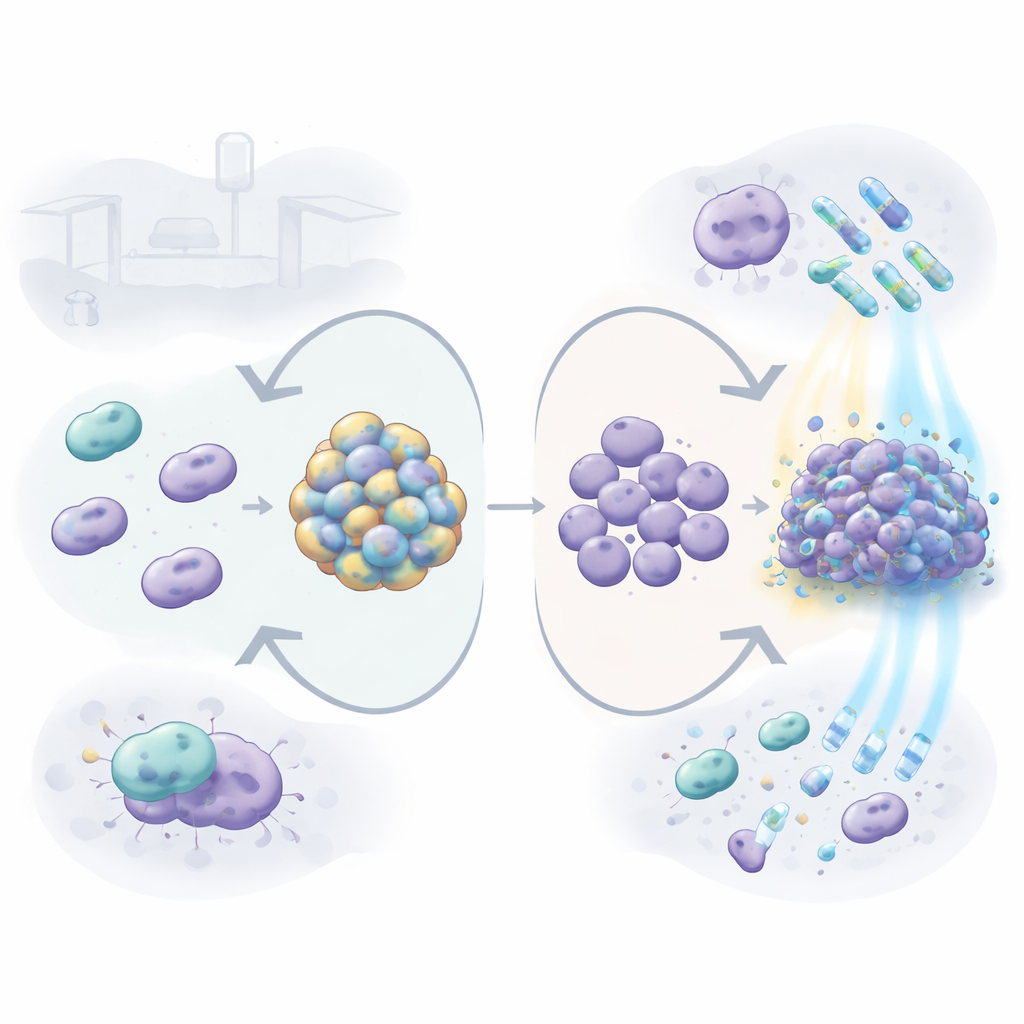
Come il manto altera la sopravvivenza sulle superfici ospedaliere
Quando la capsula è stata rimossa, i batteri liberi (planktonici) sono diventati più vulnerabili a diversi farmaci e detergenti comunemente usati in ospedale, compresi gli antibiotici gentamicina, tetraciclina e colistina, e il detergente SDS. In altre parole, senza il suo manto il germe era più facile da uccidere. Ma la storia è cambiata quando i batteri hanno formato biofilm—strati appiccicosi su superfici plastiche simili a quelli che si formano su cateteri o tubi ventilatori. Il mutante privo di capsula ha reagito producendo un biofilm molto più spesso, ricco di materiale extracellulare come il DNA. Queste comunità dense si sono rivelate più resistenti ad alcuni trattamenti, in particolare colistina, clorexidina e perossido di idrogeno, rispetto ai biofilm prodotti dal ceppo normale con capsula. Ciò suggerisce che, quando il rivestimento esterno manca, il batterio può compensare costruendo un rifugio comunitario fortificato.
Trattamento basato sulla luce e componenti del sangue
Il gruppo ha testato anche un approccio alternativo promettente chiamato terapia fotodinamica, che utilizza un colorante innocuo (clorofillina) e luce blu per generare su richiesta molecole di ossigeno tossiche. Anche qui la capsula ha aiutato il germe: i batteri privi del manto erano da 10 a 100 volte più sensibili a questo attacco indotto dalla luce, sia come cellule libere sia come biofilm. I ricercatori sono poi passati dalle superfici a un contesto più simile al corpo, coltivando i batteri in siero sanguigno ed esponendoli a cellule immunitarie. In siero attivo, il mutante privo di capsula è cresciuto molto poco e ha formato biofilm deboli, mentre il ceppo capsulato è prosperato, indicando che la capsula protegge da molecole presenti nel sangue che normalmente aiutano a eliminare i microbi. Quando i batteri sono stati messi a contatto con i macrofagi—cellule “mangianti” del sistema immunitario—il mutante è stato inghiottito e ucciso molto più facilmente. Allo stesso tempo, il gene necessario per la produzione della capsula diventava più attivo in molte condizioni stressanti, inclusa l’esposizione ad antibiotici, disinfettanti, luce blu, siero e macrofagi, mostrando che il batterio aumenta attivamente il suo manto quando è minacciato.
Attutire e riconfigurare la risposta immunitaria
Per capire come la capsula influenzi l’infiammazione, gli autori hanno infettato cellule murine e umane con il ceppo capsulato o con quello privato della capsula. Entrambi hanno scatenato reazioni immunitarie, ma il mutante privo di capsula in genere ha provocato segnali più forti per messaggeri infiammatori come IL-6 e IL-1β. Nei macrofagi, il ceppo normale con capsula ha attivato più fortemente la caspasi-3, una proteina collegata a una forma controllata e relativamente tranquilla di morte cellulare chiamata apoptosi, mentre il mutante sembrava indirizzare le risposte verso vie più pro-infiammatorie. Quando il team ha purificato il materiale capsulare e lo ha aggiunto alle cellule immunitarie senza batteri presenti, esso ha inaspettatamente agito come stimolante, promuovendo la produzione di diverse molecole infiammatorie e attirando neutrofili umani attraverso una membrana in modo dipendente dalla dose. Anche le piccole vescicole di membrana esterna rilasciate dai batteri sono risultate meno infiammatorie quando portavano la capsula sulla loro superficie, suggerendo che il manto zuccherino può mascherare altre strutture batteriche più allarmanti.
Cosa significa per i trattamenti futuri
Complessivamente, lo studio mostra che la capsula di A. baumannii è più di un semplice manto passivo. Protegge le singole cellule da antibiotici, disinfettanti, componenti del sangue, terapia con luce blu e attacco immunitario, attenuando alcuni segnali infiammatori e indirizzando le cellule immunitarie verso risposte più silenziose. Tuttavia, quando la capsula viene rimossa, i batteri possono formare biofilm più spessi che resistono a certi agenti, e frammenti di capsula rilasciati possono a loro volta attirare cellule immunitarie e amplificare l’infiammazione. Per le terapie future, questo significa che farmaci o enzimi mirati a rimuovere la capsula potrebbero aiutare il corpo a eliminare queste infezioni—ma solo se combinati in modo intelligente con altri trattamenti in grado di penetrare i biofilm risultanti e sfruttare i batteri ora esposti.
Citazione: Klimkaite, L., Kukanauskaite, G., Naujalis, J. et al. Capsular polysaccharides of Acinetobacter baumannii modulate antimicrobial resistance and innate immune response. Sci Rep 16, 14478 (2026). https://doi.org/10.1038/s41598-026-44001-w
Parole chiave: Acinetobacter baumannii, capsula batterica, biofilm, resistenza agli antibiotici, immunità innata