Clear Sky Science · ru
Капсульные полисахариды Acinetobacter baumannii модулируют антимикробную резистентность и врождённый иммунный ответ
Почему больничные микробы носят защитное покрытие
В современных больницах один упрямый микроорганизм стал печально известным нарушителем порядка: Acinetobacter baumannii — бактерия, устойчивая ко многим антибиотикам и сохраняющаяся на медицинском оборудовании. В этом исследовании изучают её слизистое внешнее покрытие, состоящее из сахарных молекул — капсулу, — и задают простой вопрос с важными последствиями: прячет ли эта оболочка лишь микроб, или она активно помогает ему выживать при воздействии препаратов и первой линии защиты организма?
Сахарный щит вокруг опасного микроба
A. baumannii часто вызывает инфекции у пациентов в отделениях интенсивной терапии — пневмонии, инфекции крови и мочевыводящих путей. Многие штаммы устойчивы к нескольким антибиотикам, поэтому врачи также используют сильные дезинфицирующие средства, моющие вещества и даже методы на основе света, чтобы контролировать его распространение. Исследователи сосредоточились на капсуле — плотном сахаристом слое, окружающем многие из этих бактерий. Они сравнили типичный клинический штамм с практически идентичной генетически модифицированной версией, лишённой способности синтезировать капсулу. Это позволило выяснить, в какой степени устойчивость микроорганизма обусловлена именно этой внешней оболочкой.
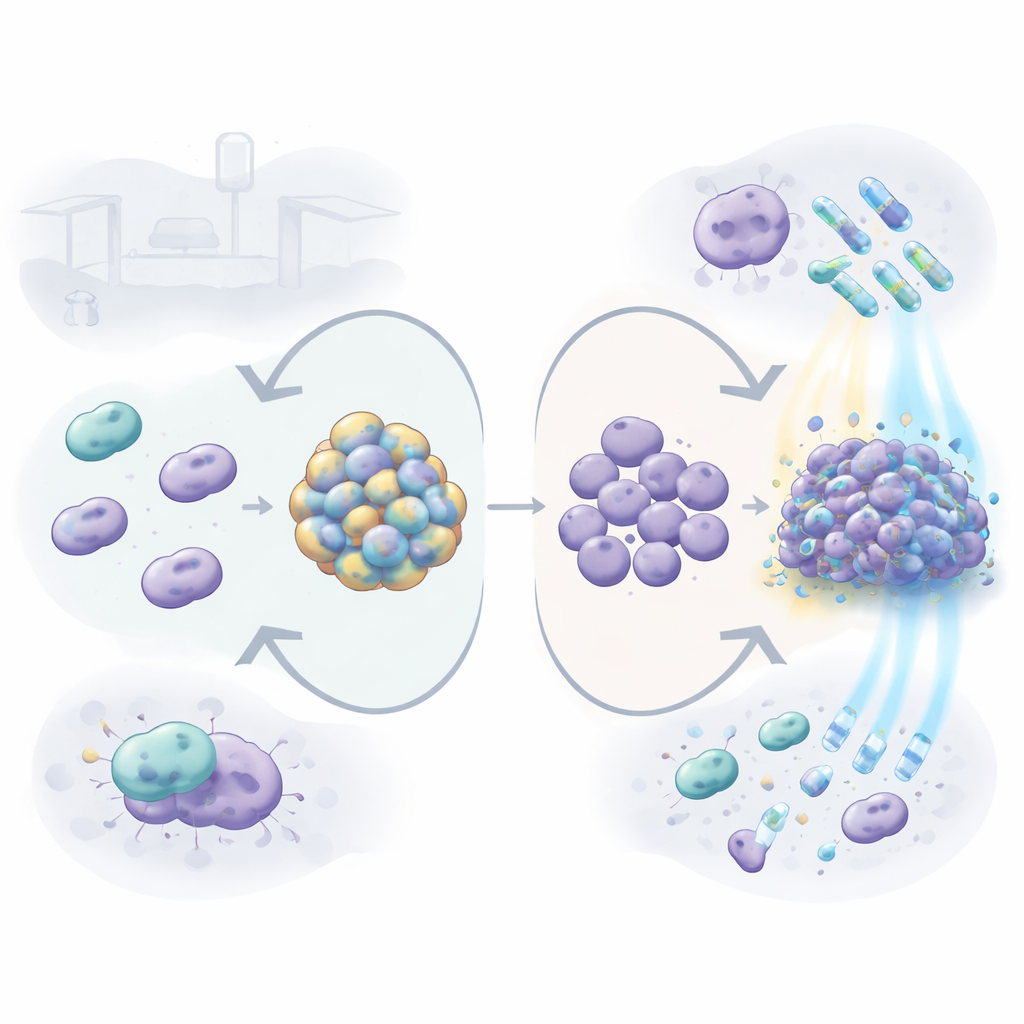
Как покрытие меняет выживаемость на больничных поверхностях
При удалении капсулы свободноплавающие (планктонные) бактерии становились более уязвимыми к ряду лекарств и очистителей, часто используемых в больницах, включая антибиотики гентамицин, тетрациклин и полимиксин (колистин), а также детергент SDS. Иными словами, без капсулы микроб было легче уничтожить. Но картина менялась, когда бактерии формировали биопленки — липкие слои на пластике, похожие на те, что они образуют на катетерах или трубках дыхательных аппаратов. Мутант без капсулы реагировал повышенным образованием более плотной биопленки, богатой внеклеточным материалом, таким как ДНК. Эти плотные сообщества оказывались более устойчивыми к некоторым обработкам, особенно к колистину, хлоргексидину и перекиси водорода, по сравнению с биопленками нормального, покрытого штамма. Это предполагает, что при отсутствии внешней оболочки бактерия может компенсировать потерю, возводя укреплённое коммунальное убежище.
Лечение на основе света и компоненты крови
Команда также проверяла перспективный альтернативный метод — фотодинамическую терапию, которая использует безвредный краситель (хлорофиллин) и синий свет для генерации токсичных молекул кислорода по требованию. И здесь капсула играла роль защитного фактора: бактерии без оболочки были в 10–100 раз более чувствительны к этому световому воздействию как в виде свободных клеток, так и в биопленках. Исследователи затем переходили от поверхностей к более телесно-подобной среде, выращивая бактерии в сыворотке крови и подвергая их воздействию клеток иммунной системы. В активной сыворотке мутант без капсулы почти не рос и формировал слабые биопленки, тогда как покрытый штамм процветал, что указывает на защитную роль капсулы против молекул в крови, обычно помогающих очищать микроорганизмы. При добавлении к макрофагам — профессиональным «пожирателям» иммунной системы — мутант поглощался и уничтожался гораздо легче. При этом ген, ответственный за синтез капсулы, активировался при многих стрессовых условиях, включая воздействие антибиотиков, дезинфектантов, синего света, сыворотки и макрофагов, что свидетельствует о том, что бактерия активно усиливает свою оболочку при угрозе.
Угасание и перенаправление иммунного ответа
Чтобы понять, как капсула влияет на воспаление, авторы инфицировали клетки мыши и человека либо покрытым, либо непокрытым штаммом. Оба вызывали иммунный ответ, но мутант без капсулы в целом провоцировал более сильную выработку провоспалительных сигналов, таких как IL-6 и IL-1β. В макрофагах нормальный покрытый штамм сильнее активировал каспазу-3 — белок, связанный с контролируемой, относительно «тихой» формой клеточной смерти, апоптозом, — тогда как мутант смещал ответы в сторону более воспалительных путей. Когда команда очистила материал капсулы отдельно и добавила его в иммунные клетки в отсутствие бактерий, он неожиданно действовал как стимулятор, стимулируя выработку нескольких провоспалительных молекул и в дозозависимом порядке привлекая человеческие нейтрофилы через мембрану. Крошечные пузырьки внешней мембраны, выделяемые бактериями (везикулы), также были менее воспалительными, когда на их поверхности присутствовала капсула, что позволяет предположить: сахаристая оболочка может маскировать другие, более тревожные бактериальные структуры.
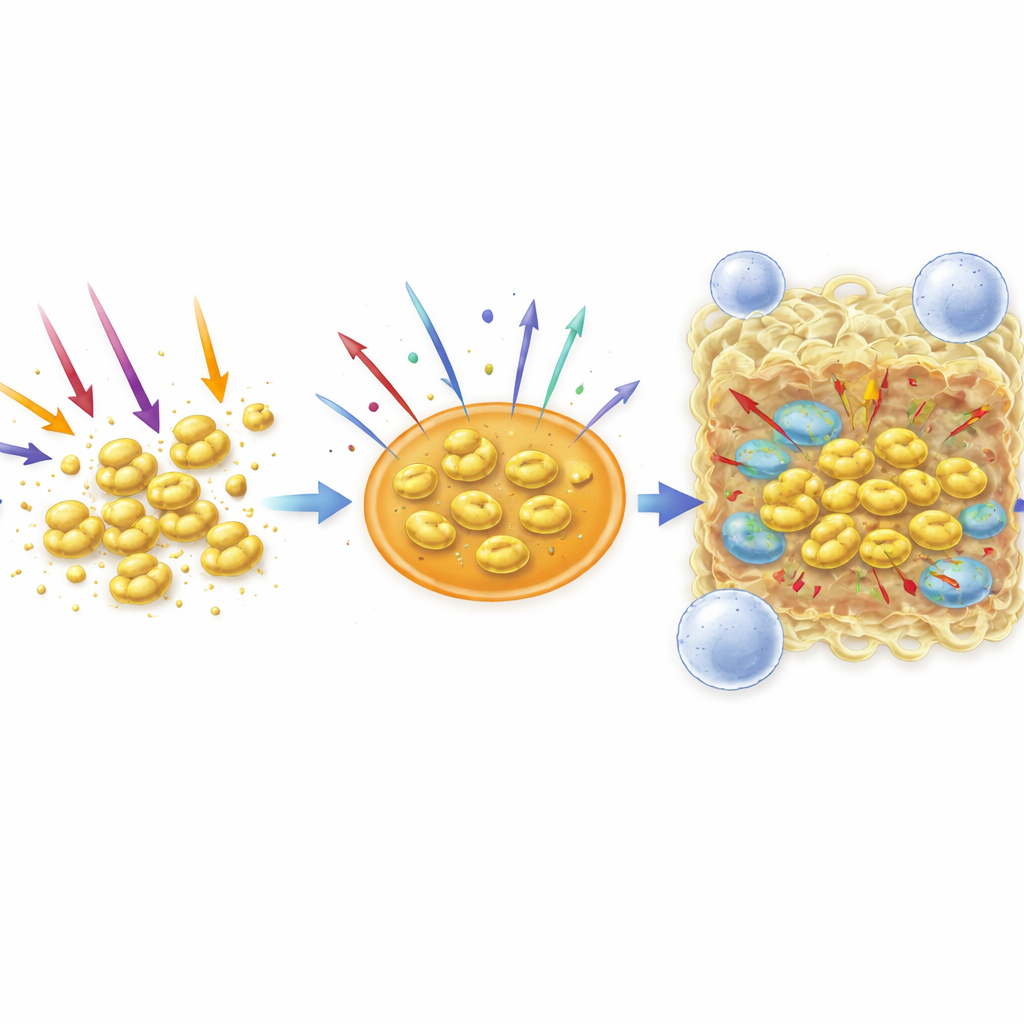
Что это значит для будущих лечений
В целом исследование показывает, что капсула A. baumannii — это не просто пассивная мантия. Она защищает одиночные клетки от антибиотиков, дезинфектантов, компонентов крови, фототерапии с синим светом и атак иммунной системы, одновременно смягчая некоторые воспалительные сигналы и направляя иммунные клетки к более «тихим» формам ответа. В то же время при удалении капсулы бактерии могут формировать более плотные биопленки, устойчивые к определённым агентам, а частицы сброшенной капсулы сами по себе способны привлекать иммунные клетки и усиливать воспаление. Для разработки будущих терапий это означает: лекарства или ферменты, направленные на разрушение капсулы, могут помочь организму устранить такие инфекции — но только если их разумно комбинировать с другими средствами, которые смогут проникнуть через образовавшиеся биопленки и воспользоваться уязвимостью вновь оголённых бактерий.
Цитирование: Klimkaite, L., Kukanauskaite, G., Naujalis, J. et al. Capsular polysaccharides of Acinetobacter baumannii modulate antimicrobial resistance and innate immune response. Sci Rep 16, 14478 (2026). https://doi.org/10.1038/s41598-026-44001-w
Ключевые слова: Acinetobacter baumannii, бактериальная капсула, биотоплоки, устойчивость к антибиотикам, врождённый иммунитет