Clear Sky Science · es
Los polisacáridos capsulares de Acinetobacter baumannii modulan la resistencia a antimicrobianos y la respuesta inmunitaria innata
Por qué los gérmenes hospitalarios llevan un abrigo protector
En los hospitales modernos, un germen persistente se ha convertido en un problema notorio: Acinetobacter baumannii, una bacteria que elude muchos antibióticos y perdura en el material sanitario. Este estudio examina su capa externa viscosa, formada por moléculas de azúcar llamada cápsula, y plantea una pregunta sencilla con grandes consecuencias: ¿esa capa solo oculta al germen o le ayuda activamente a sobrevivir frente a los fármacos y a la primera línea de defensa del organismo?
Un escudo azucarado alrededor de un germen peligroso
A. baumannii suele infectar a personas en unidades de cuidados intensivos, provocando neumonía, infecciones sanguíneas y urinarias. Muchas cepas son resistentes a múltiples antibióticos, por lo que los médicos también recurren a desinfectantes potentes, detergentes e incluso métodos basados en luz para controlarlas. Los investigadores se centraron en la cápsula, una capa espesa y azucarada que rodea a muchas de estas bacterias. Compararon una cepa clínica típica con una versión casi idéntica alterada genéticamente para que ya no pudiera fabricar esa cápsula. Esto les permitió determinar cuánto de la resistencia del germen se debe específicamente a esa capa externa.
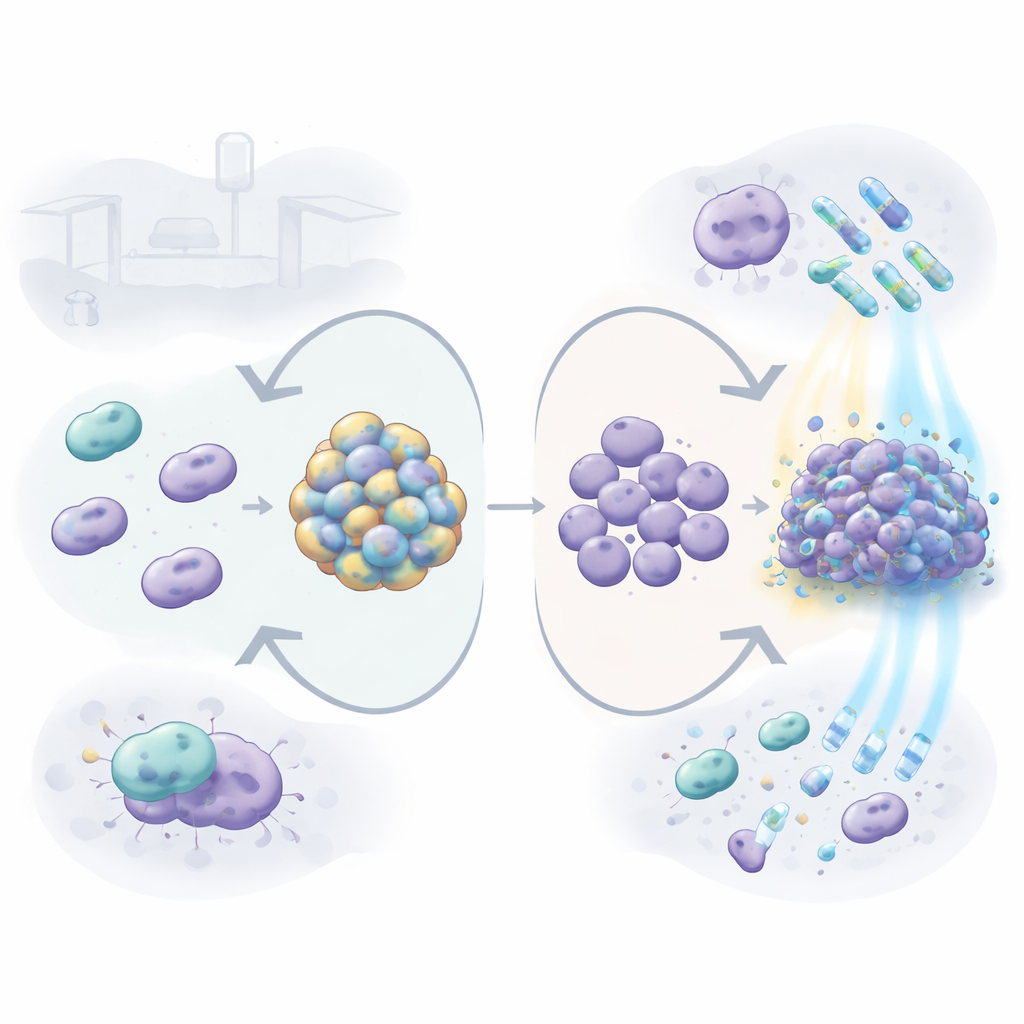
Cómo la capa modifica la supervivencia en superficies hospitalarias
Cuando se eliminó la cápsula, las bacterias libres en suspensión (plactónicas) se volvieron más vulnerables a varios fármacos y limpiadores usados habitualmente en hospitales, incluidos los antibióticos gentamicina, tetraciclina y colistina, y el detergente SDS. En otras palabras, sin su abrigo el germen era más fácil de matar. Pero la historia cambió cuando las bacterias formaron biopelículas: capas pegajosas sobre superficies plásticas similares a las que forman en catéteres o tubos de ventilación. El mutante sin cápsula respondió formando una biopelícula mucho más densa, rica en material extracelular como ADN. Estas comunidades compactas resultaron resistir mejor algunos tratamientos, especialmente colistina, clorhexidina y peróxido de hidrógeno, que las biopelículas de la cepa normal y encapsulada. Esto sugiere que, cuando falta la capa externa, la bacteria puede compensar construyendo un refugio comunitario reforzado.
Tratamiento basado en luz y componentes sanguíneos
El equipo también probó un enfoque alternativo prometedor llamado terapia fotodinámica, que usa un tinte inocuo (clorofilina) y luz azul para generar moléculas de oxígeno tóxicas bajo demanda. Aquí de nuevo la cápsula protegió al germen: las bacterias sin cápsula fueron de 10 a 100 veces más sensibles a este ataque inducido por luz, tanto como células libres como en biopelículas. Luego los investigadores pasaron de las superficies a un entorno más similar al corporal, cultivando las bacterias en suero sanguíneo y exponiéndolas a células inmunitarias. En suero activo, el mutante sin cápsula casi no creció y formó biopelículas débiles, mientras que la cepa encapsulada prosperó, lo que indica que la cápsula protege frente a moléculas en la sangre que normalmente ayudan a eliminar microbios. Al añadirse a macrófagos—las células «comedoras» profesionales del sistema inmune—el mutante fue engullido y eliminado con mucha más facilidad. Al mismo tiempo, el gen necesario para la producción de la cápsula se mostró más activo bajo muchas condiciones de estrés, incluida la exposición a antibióticos, desinfectantes, luz azul, suero y macrófagos, lo que demuestra que la bacteria refuerza activamente su abrigo cuando está amenazada.
Silenciar y redirigir la respuesta inmune
Para entender cómo la cápsula influye en la inflamación, los autores infectaron células de ratón y humanas con la cepa encapsulada o sin cápsula. Ambas desencadenaron reacciones inmunitarias, pero el mutante sin cápsula generalmente provocó señales más fuertes de mensajeros inflamatorios como IL-6 e IL-1β. En macrófagos, la cepa normal y encapsulada activó con mayor intensidad la caspasa-3, una proteína vinculada a una forma controlada y relativamente silenciosa de muerte celular llamada apoptosis, mientras que el mutante pareció inclinar las respuestas hacia vías más inflamatorias. Cuando el equipo purificó material capsular por sí solo y lo añadió a células inmunitarias sin bacterias presentes, actuó inesperadamente como un estimulante, impulsando la producción de varias moléculas inflamatorias y atrayendo neutrófilos humanos a través de una membrana de forma dependiente de la dosis. Pequeñas vesículas de la membrana externa liberadas por las bacterias también resultaron menos inflamatorias cuando llevaban cápsula en su superficie, lo que sugiere que el abrigo azucarado puede enmascarar otras estructuras bacterianas más alarmantes.
Lo que esto significa para tratamientos futuros
En conjunto, el estudio muestra que la cápsula de A. baumannii es más que una capa pasiva. Protege a las células individuales frente a antibióticos, desinfectantes, componentes sanguíneos, la terapia con luz azul y el ataque inmunitario, al tiempo que atenúa algunas señales inflamatorias y orienta a las células inmunes hacia respuestas más silenciosas. Sin embargo, cuando se elimina la cápsula, las bacterias pueden formar biopelículas más gruesas que resisten ciertos agentes, y fragmentos de cápsula desprendida pueden atraer a células inmunitarias y avivar la inflamación. Para terapias futuras, esto implica que fármacos o enzimas diseñados para eliminar la cápsula podrían ayudar al organismo a eliminar estas infecciones, pero solo si se combinan de forma inteligente con otros tratamientos capaces de penetrar las biopelículas resultantes y aprovechar la mayor vulnerabilidad de las bacterias expuestas.
Cita: Klimkaite, L., Kukanauskaite, G., Naujalis, J. et al. Capsular polysaccharides of Acinetobacter baumannii modulate antimicrobial resistance and innate immune response. Sci Rep 16, 14478 (2026). https://doi.org/10.1038/s41598-026-44001-w
Palabras clave: Acinetobacter baumannii, capsula bacteriana, biopelículas, resistencia a antibióticos, inmunidad innata