Clear Sky Science · tr
Kanserle ilişkili fibroblastlar, kolorektal kanser hücrelerinde metabolik heterojenliği yönlendirir: metabolik modellemeden çıkarımlar
Kolon kanserinde komşu hücrelerin önemi neden büyük?
Kolorektal kanser, kendi başına yalnızca kontrolsüz çoğalan hücrelerden oluşan bir kitle değildir. Tümör hücreleri; destek hücreleri, bağ dokusu ve kimyasal sinyallerle dolu sıkışık bir mahallede yaşar; bunların tümü kanserin davranışını ve tedaviye yanıtını şekillendirebilir. Bu çalışma, görünüşte basit bir soruyu soruyor: kanserle ilişkili fibroblastlar (yardımcı hücreler) kolon kanser hücrelerinin besinleri ve enerjiyi kullanma biçimini nasıl değiştiriyor ve bu değişiklikler, bazı tümörlerin metabolizmaya yönelik ilaçlara neden direnç gösterdiğini açıklayabilir mi?
Tümör mahallesindeki gizli yardımcılar
Fibroblastlar normalde bağ dokusunun sessiz yapı taşlarıdır, ancak tümör içinde sıklıkla aktive olup kanserle ilişkili fibroblastlar (CAF'lar) olarak adlandırılırlar. KRAS geninde mutasyon taşıyan—sık görülen ve ilaçla hedeflenmesi zor—kolorektal kanserlerde CAF'lar sadece yapı sağlamakla kalmaz. Metabolitler ve büyüme faktörleri salarak tümör hücrelerini besleyebilir ve onların şeker, amino asitler ve diğer besinleri işleme biçimlerini yeniden düzenlemelerini teşvik edebilirler. Deneyler, kanser hücreleri CAF'ların daha önce bulunduğu sıvıda (CAF-kondisyonlu ortam) büyütüldüğünde, daha çok şeker yakma yolaklarına dayandıklarını ve bazı metabolik ilaçlara karşı direnç işaretleri gösterdiklerini ortaya koymuştur.
Birçok olası geleceği keşfetmek için bilgisayar modelleri kullanmak
Yazarlar, bir kanser hücresinin metabolizmasını çalıştırabileceği tek bir “en iyi” yolu izlemek yerine, besin alımı ve büyüme gibi temel kısıtlarla tutarlı olan binlerce olası metabolik durumu örnekleyen hesaplamalı bir yaklaşım kullandılar. Başlangıç olarak, glukoz ve glutamini işleyen ve büyüme için yapı taşları üreten ana yolakları içeren, KRAS-mutant kolorektal kanser hücrelerinin merkezi karbon metabolizmasına dair deneysel bilgileri içeren mevcut bir modelden yola çıktılar. Ardından çoğunlukla ana şeker parçalanma yolunda ve ilişkili dallanma yolunda yer alan 12 önemli enzimin kısmi veya tam yavaşlamalarını simüle ettiler. Her yavaşlama iki sanal ortamda incelendi: standart kanser hücresi ortamı ve CAF-kondisyonlu ortam.
Metabolik labirentte birçok rota
Her simüle edilmiş koşul için model, akışın—her metabolik reaksiyon boyunca madde akışının—nasıl düzenlenebileceğine dair 1.000 farklı yol üretti. Ekip, bu yüksek boyutlu verilere modern desen tanıma araçları uygulayarak bunları her noktanın bir olası metabolik durumu temsil ettiği iki boyutlu haritalara sıkıştırdı. Nokta kümeleri, hücrelerin benimseyebileceği tipik durumlara karşılık geliyor. Koşullar arasında bu haritaları karşılaştırınca, yazarlar CAF-kondisyonlu ortamda hücrelerin standart ortamdaki hücrelere göre metabolik uzayın daha geniş ve daha çeşitli bir bölgesini işgal ettiğini buldular. Başka bir deyişle, CAF kaynaklı faktörler, enzim müdahalelerinden sonra daha geniş bir metabolik strateji karışımını teşvik etti; farklı gen kapatmalarının aynı duruma sık sık yakınsaması daha az görüldü.
Yolak değişimleri ve stres altındaki büyüme
Çalışma, yolaklardaki akışları toplayarak CAF-kondisyonlu ortamın kolorektal kanser hücrelerini, bu yollar boyunca enzimler kısmen inhibe edilse bile, tutarlı biçimde ana şeker işleme yolunu daha yoğun kullanmaya ve bazı mitokondriyal ile dallanma yol aktivitelerinden uzaklaşmaya ittiğini gösterdi. Bazı müdahaleler, dallanma yolunun bölümlerinde akış yönünü tersine çevirdi; bu durum hücrelerin ara ürünleri büyüme ve strese karşı koruma için gerekli temel molekülleri yeniden üretmek üzere başka yollara yönlendirebileceğini öneriyor. Araştırmacılar modelin hücre büyümesinin vekili olarak kabul edilen biyokütle üretimini incelediklerinde, her enzim yavaşlamasının büyümeyi azalttığını, ancak genellikle CAF-kondisyonlu ortamda bu azalmanın daha az belirgin olduğunu gördüler. Özellikle erken karar noktalarındaki enzimleri engellemede, CAF-kondisyonlu ortamda büyümenin daha dayanıklı olduğu durumlar vardı; bu da tümör mahallesinin koruyucu bir etkisine işaret ediyor.
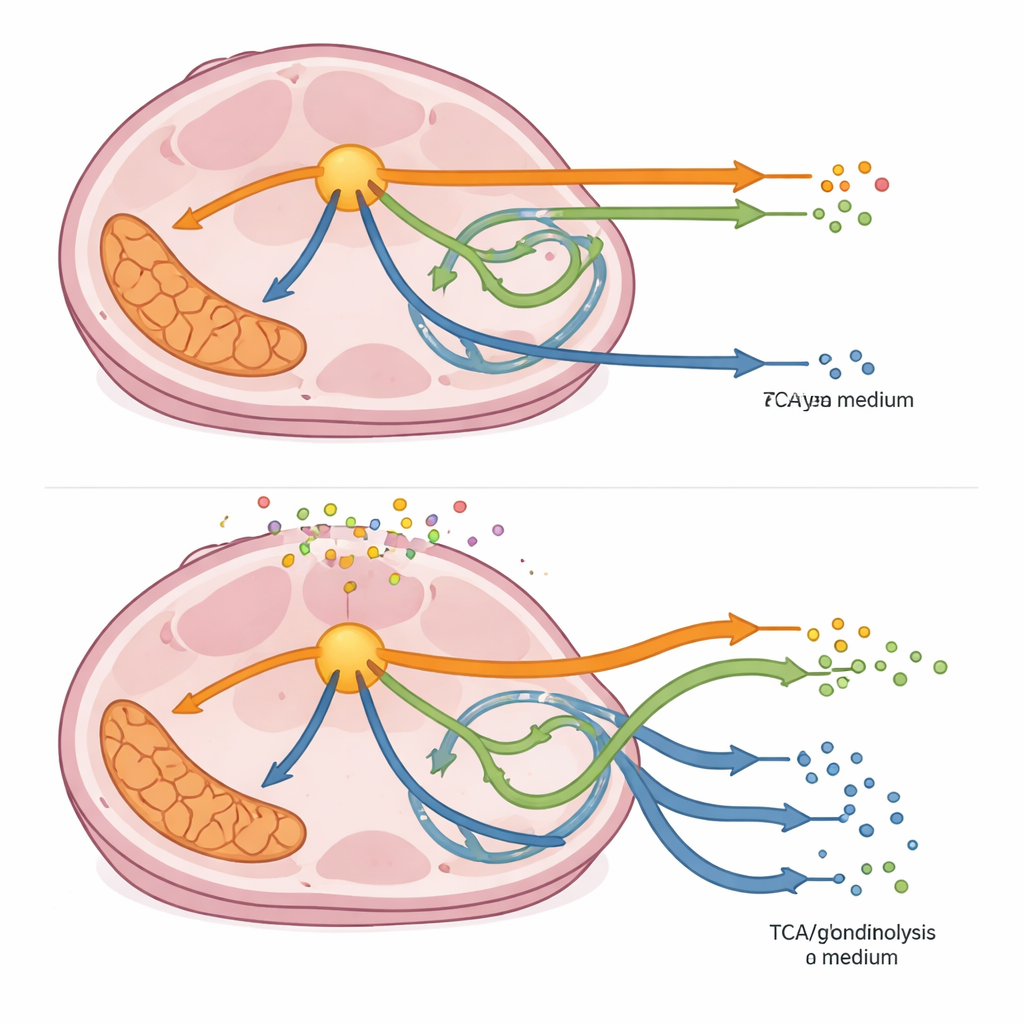
Gelecekteki tedaviler için ne anlama geliyor
Uzman olmayan biri için ana mesaj şudur: kanser hücreleri metabolik ilaçlara izole biçimde yanıt vermez; komşuları ve salgılanan moleküllerin oluşturduğu çevre, hayatta kalmalarına olanak tanıyan yedek yollar açabilir. CAF-kondisyonlu ortam, KRAS-mutant kolorektal kanser hücrelerini metabolik olarak daha çeşitli hale getirdi ve birçok durumda enzim hedefleyen tedavilere karşı simüle edilmiş direnç sağladı, bunu bazı hedeflerin hâlâ büyümeyi güçlü biçimde kısıtlamasına rağmen. Bu çalışma, başarılı metabolik tedavilerin fibroblastların sağladığı desteği dikkate alması veya doğrudan bozması gerektiğini öne sürüyor. Tek bir optimal yolu değil, olası metabolik durumların tüm manzarasını haritalandırarak çalışma; tümörün en zayıf olduğu yerleri ve mikroçevrenin bu zayıf noktaları nasıl kaydırabileceğini daha zengin bir biçimde gösteriyor.
Atıf: Elton, E., Tavakoli, N., Cetin, H. et al. Cancer-associated fibroblasts drive metabolic heterogeneity in colorectal cancer cells: predictions from metabolic modeling. npj Syst Biol Appl 12, 54 (2026). https://doi.org/10.1038/s41540-026-00673-8
Anahtar kelimeler: kolorektal kanser metabolizması, kanserle ilişkili fibroblastlar, tümör mikroçevresi, metabolik heterojenlik, hesaplamalı modelleme