Clear Sky Science · it
I fibroblasti associati al cancro guidano l'eterogeneità metabolica nelle cellule del cancro colorettale: previsioni dal modellamento metabolico
Perché i vicini cellulari contano nel cancro del colon
Il cancro colorettale non è soltanto una massa di cellule ribelli che cresce da sola. Le cellule tumorali vivono in un quartiere affollato, ricco di cellule di supporto, tessuto connettivo e segnali chimici, tutti fattori che possono modellare il comportamento del tumore e la sua risposta alle cure. Questo studio pone una domanda apparentemente semplice: come alterano le cellule di supporto chiamate fibroblasti associati al cancro il modo in cui le cellule del cancro del colon usano nutrienti ed energia, e queste modifiche possono spiegare perché alcuni tumori resistono a farmaci diretti sul metabolismo?
Aiutanti nascosti nel quartiere tumorale
I fibroblasti sono normalmente costruttori silenziosi del tessuto connettivo, ma all'interno dei tumori spesso si attivano e vengono chiamati fibroblasti associati al cancro (CAF). Nel cancro colorettale con mutazioni nel gene KRAS — un driver comune e difficile da colpire — i CAF fanno più che fornire struttura. Secernono metaboliti e fattori di crescita che possono nutrire le cellule tumorali e indurle a riconfigurare il modo in cui processano zuccheri, aminoacidi e altri nutrienti. Esperimenti hanno mostrato che quando le cellule tumorali vengono coltivate in un terreno che ha ospitato precedentemente CAF, detto terreno condizionato da CAF, dipendono maggiormente dalle vie di ossidazione degli zuccheri e mostrano segnali di resistenza ad alcuni farmaci metabolici.
Usare modelli computazionali per esplorare molti futuri possibili
Invece di seguire un unico «miglior» modo in cui una cellula tumorale potrebbe gestire il suo metabolismo, gli autori hanno usato un approccio computazionale che campiona migliaia di stati metabolici possibili coerenti con vincoli di base come l'assorbimento di nutrienti e la crescita. Sono partiti da un modello esistente, informato sperimentalmente, del metabolismo del carbonio centrale in cellule di cancro colorettale con KRAS mutato, includendo le vie chiave che processano glucosio e glutammina e generano i mattoni per la crescita. Hanno quindi simulato rallentamenti parziali o completi di 12 enzimi importanti, per lo più nella principale via di degradazione dello zucchero e in una via ramificata connessa. Ogni rallentamento è stato esplorato in due ambienti virtuali: un mezzo standard per cellule tumorali e il mezzo condizionato da CAF.
Molte strade attraverso il labirinto metabolico
Per ogni condizione simulata, il modello ha prodotto 1.000 modi diversi in cui il flusso — il passaggio di materia attraverso ciascuna reazione metabolica — poteva essere organizzato. Il gruppo ha applicato strumenti moderni di riconoscimento dei pattern a questi dati ad alta dimensionalità, comprimendoli in mappe bidimensionali dove ogni punto rappresenta uno stato metabolico possibile. I cluster di punti corrispondono a stati tipici che le cellule potrebbero adottare. Confrontando queste mappe tra le condizioni, gli autori hanno trovato che le cellule nel mezzo condizionato da CAF occupavano una regione più ampia e più varia dello spazio metabolico rispetto alle cellule in mezzo standard. In altre parole, i fattori derivati dai CAF hanno favorito un ventaglio più ampio di strategie metaboliche dopo le perturbazioni enzimatiche, con meno casi in cui diversi knockdown convergevano sullo stesso stato.
Spostamenti di via e crescita sotto stress
Sommando i flussi attraverso intere vie, lo studio ha rivelato che il mezzo condizionato da CAF spingeva in modo coerente le cellule del cancro colorettale verso un uso più intenso della principale via di processamento degli zuccheri e lontano da certe attività mitocondriali e di vie ramificate, anche quando gli enzimi lungo queste rotte erano parzialmente inibiti. Alcune perturbazioni invertirono la direzione del flusso in parti della via ramificata, suggerendo che le cellule potevano deviare gli intermedi per rigenerare molecole chiave necessarie per la crescita e la protezione dallo stress. Quando i ricercatori hanno esaminato il proxy del modello per la crescita cellulare — la produzione di biomassa — hanno riscontrato che ogni rallentamento enzimatico riduceva la crescita, ma spesso in misura minore nel mezzo condizionato da CAF. In diversi casi, specialmente bloccando enzimi in punti decisionali precoci, la crescita nel mezzo condizionato da CAF è risultata più resistente, evidenziando un effetto protettivo del microambiente tumorale.
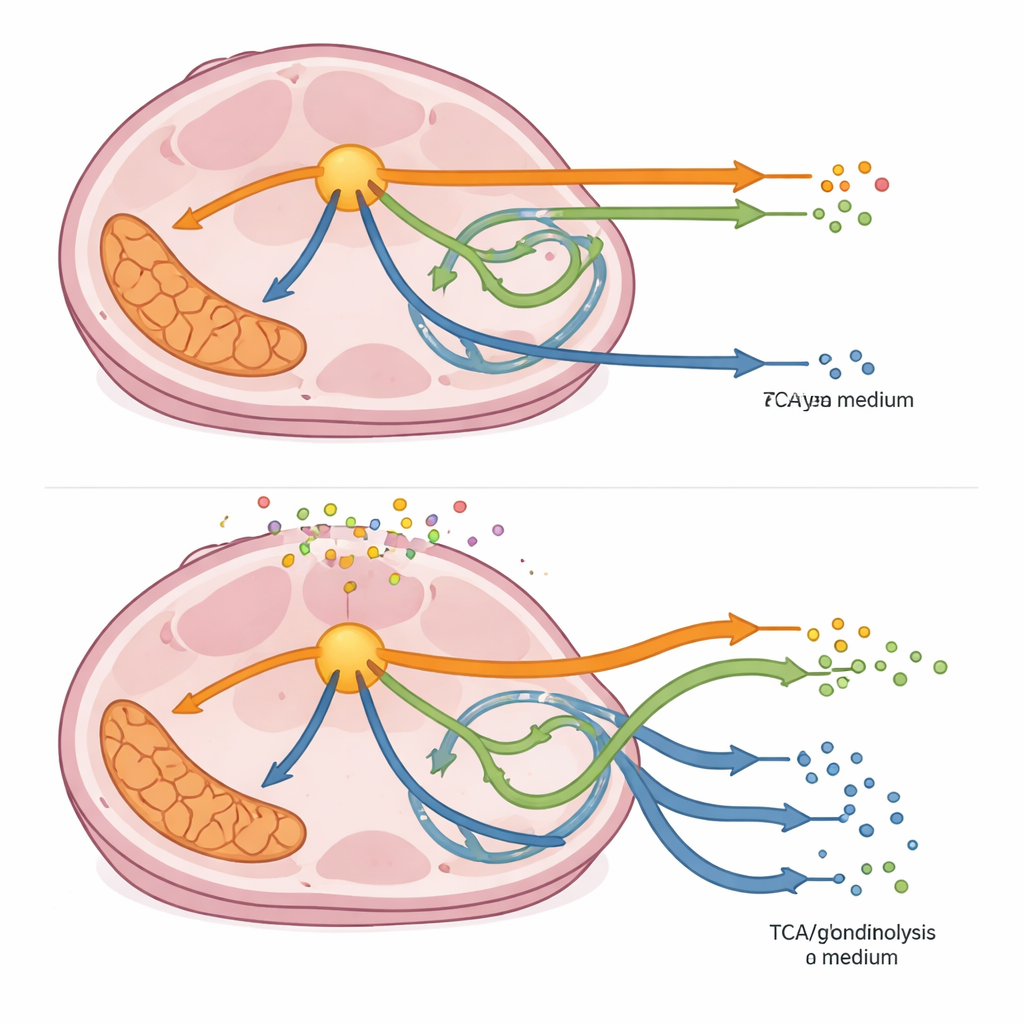
Quali implicazioni per i trattamenti futuri
Per chi non è specialista, il messaggio principale è che le cellule tumorali non rispondono ai farmaci metabolici in isolamento; i loro vicini e la zuppa circostante di molecole secrete possono aprire rotte alternative che permettono loro di sopravvivere. Il mezzo condizionato da CAF ha reso le cellule di cancro colorettale con KRAS mutato più metabolicamente diverse e, in molti casi, più capaci di sopportare terapie simulate mirate agli enzimi, sebbene alcuni bersagli abbiano comunque fortemente limitato la crescita. Questo lavoro suggerisce che trattamenti metabolici efficaci dovranno tenere conto, o addirittura interrompere direttamente, il supporto fornito dai fibroblasti. Mappando non solo una singola via ottimale ma un intero paesaggio di stati metabolici possibili, lo studio offre una visione più ricca di dove il tumore è più vulnerabile — e di come il suo microambiente può spostare questi punti deboli.
Citazione: Elton, E., Tavakoli, N., Cetin, H. et al. Cancer-associated fibroblasts drive metabolic heterogeneity in colorectal cancer cells: predictions from metabolic modeling. npj Syst Biol Appl 12, 54 (2026). https://doi.org/10.1038/s41540-026-00673-8
Parole chiave: metabolismo del cancro colorettale, fibroblasti associati al cancro, microambiente tumorale, eterogeneità metabolica, modellazione computazionale