Clear Sky Science · ar
الخلايا الليفية المرتبطة بالسرطان تقود التغايرية الأيضية في خلايا سرطان القولون: تنبؤات من نمذجة أيضية
لماذا يهم دور الخلايا المجاورة في سرطان القولون
سرطان القولون والمستقيم ليس مجرد كتلة من الخلايا المنفلتة التي تنمو بمعزل. تعيش خلايا الورم في حي مكتظ بخلايا داعمة وأنسجة رابطة وإشارات كيميائية، وكلها تشكل طريقة تصرف السرطان واستجابته للعلاج. تطرح هذه الدراسة سؤالًا يبدو بسيطًا لكنه مهمًا: كيف تغيّر خلايا مساعدة تُدعى الخلايا الليفية المرتبطة بالسرطان طريقة استخدام خلايا سرطان القولون للمغذيات والطاقة، وهل يمكن أن تفسر هذه التغيرات سبب مقاومة بعض الأورام للأدوية التي تستهدف أيضها؟
مساعدون خفيون في حي الورم
عادةً ما تكون الخلايا الليفية بناة هادئون للأنسجة الرابطة، لكن داخل الأورام غالبًا ما تُنشط وتُعرف حينها بالخلايا الليفية المرتبطة بالسرطان (CAFs). في سرطان القولون والمستقيم الحامل لطفرة في جين KRAS—وهي طفرة شائعة وصعبة الاستهداف—تفعل CAFs أكثر من مجرد توفير الهيكل. تطلق هذه الخلايا مستقلبات وعوامل نمو يمكن أن تغذي خلايا الورم وتشجعها على إعادة توصيل طرق معالجة السكر والأحماض الأمينية والمغذيات الأخرى. أظهرت تجارب أن خلايا السرطان المزروعة في وسط سائل كان قد احتضن سابقًا CAFs، ويُسمى الوسط المشروط من CAF، تعتمد بدرجة أكبر على مسارات حرق السكر وتظهر علامات مقاومة لبعض الأدوية الأيضية.
استخدام نماذج حاسوبية لاستكشاف احتمالات كثيرة
بدلاً من تتبع طريقة واحدة «مثلى» قد يعمل بها أيض خلية السرطان، استخدم المؤلفون نهجًا حاسوبيًا يقوم بأخذ عينات لآلاف الحالات الأيضية الممكنة المتوافقة مع قيود أساسية مثل امتصاص المغذيات والنمو. انطلقوا من نموذج قائم معلم تجريبيًا لأيض الكربون المركزي في خلايا سرطان القولون والمستقيم الحاملة لطفرة KRAS، شمل المسارات الأساسية التي تعالج الجلوكوز والغلوتامين وتنتج لبنات البناء للنمو. ثم حاكوا تباطؤًا جزئيًا أو كاملًا في 12 إنزيمًا مهمًا، معظمها في المسار الرئيسي لتفكيك السكر ومسار متفرع مرتبط. استُكشف كل تباطؤ في بيئتين افتراضيتين: وسط قياسي لخلية السرطان ووسط مشروط من CAF.
طرق عديدة عبر متاهة الأيض
لكل حالةٍ مُحاكاة، أنتج النموذج 1000 طريقة مختلفة يمكن أن يُرتب بها التدفق—تدفق المادة عبر كل تفاعل أيضي. طبق الفريق أدوات حديثة للتعرّف على الأنماط على هذه البيانات عالية الأبعاد، مضغّطين إياها إلى خرائط ثنائية الأبعاد حيث تمثل كل نقطة حالة أيضية ممكنة. تشكّل مجموعات النقاط حالات نموذجية قد تتبناها الخلايا. بمقارنة هذه الخرائط عبر الشروط، وجد المؤلفون أن الخلايا في الوسط المشروط من CAF احتلت نطاقًا أوسع وأكثر تنوعًا من الفضاء الأيضي مقارنة بالخلايا في الوسط القياسي. بعبارة أخرى، شجعت العوامل المشتقة من CAF مزيجًا أوسع من الاستراتيجيات الأيضية بعد تعطيل الإنزيمات، مع حالات أقل تقود فيها مختلف التعطيلات إلى نفس الحالة.
تحولات في المسارات والنمو تحت الضغط
من خلال جمع التدفقات عبر مسارات كاملة، كشفت الدراسة أن الوسط المشروط من CAF دفع خلايا سرطان القولون والمستقيم باستمرار نحو استخدام أكبر للمسار الرئيسي لمعالجة السكر والابتعاد عن بعض نشاطات الميتوكوندريا والمسارات المتفرعة، حتى عندما كانت الإنزيمات على امتداد هذه الطرق مثبطة جزئيًا. أعادت بعض الاضطرابات توجيه اتجاه التدفق في أجزاء من المسار المتفرع، مما يوحي بأن الخلايا قد تعيد توجيه الوسائط الوسيطة لإعادة توليد جزيئات رئيسية لازمة للنمو والحماية من الإجهاد. عندما فحص الباحثون وكيل النمو في النموذج—إنتاج الكتلة الحيوية—وجدوا أن كل تباطؤ إنزيمي قلّل النمو، لكن غالبًا بدرجة أقل في الوسط المشروط من CAF. في عدة حالات، خاصة عند حجب إنزيمات عند نقاط قرار مبكرة، كان النمو في الوسط المشروط من CAF أكثر مرونة، مما يبرز تأثيرًا وقائيًا لبيئة الورم المحيطة.
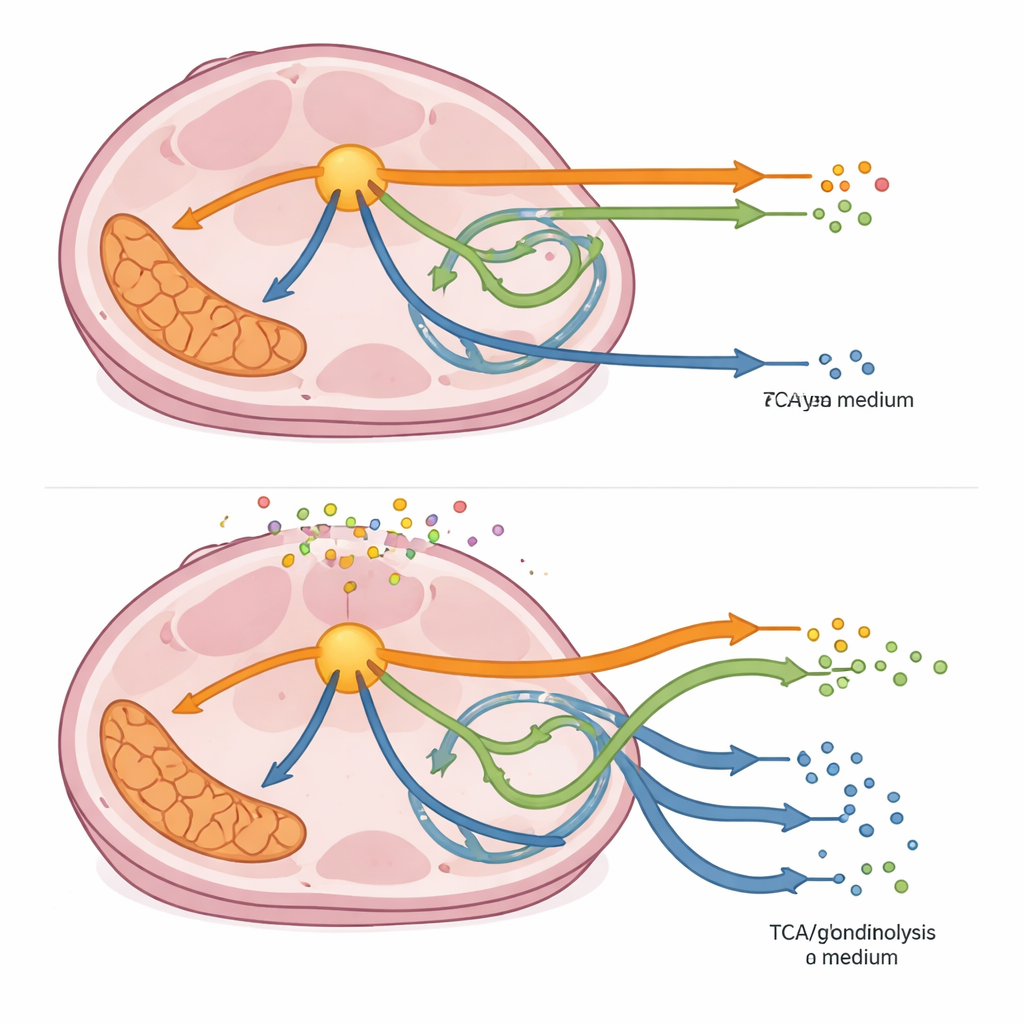
ماذا يعني هذا للعلاجات المستقبلية
بالنسبة لغير المتخصصين، الرسالة الرئيسية هي أن خلايا السرطان لا تستجيب للأدوية الأيضية بمعزل؛ فقد تفتح الخلايا المجاورة والحساء المحيط من الجزيئات المفرزة طرقًا احتياطية تتيح لها البقاء. جعل الوسط المشروط من CAF خلايا سرطان القولون والمستقيم الحاملة لطفرة KRAS أكثر تنوعًا أيضيًا وفي كثير من الحالات أكثر قدرة على الصمود أمام علاجات محاكاة تستهدف الإنزيمات، رغم أن بعض الأهداف ما تزال تقوّض النمو بشدة. تشير هذه الدراسة إلى أن العلاجات الأيضية الناجحة ستحتاج إلى حساب دعم الخلايا الليفية أو حتى تعطيله مباشرة. من خلال رسم ليس مسارًا مثاليًا واحدًا فحسب بل كامل مشهد الحالات الأيضية الممكنة، تقدم الدراسة رؤية أغنى لنقاط الضعف الأكثر احتمالًا في الورم—وكيف يمكن لميكروبيئته أن تغيّر تلك النقاط الضعيفة.
الاستشهاد: Elton, E., Tavakoli, N., Cetin, H. et al. Cancer-associated fibroblasts drive metabolic heterogeneity in colorectal cancer cells: predictions from metabolic modeling. npj Syst Biol Appl 12, 54 (2026). https://doi.org/10.1038/s41540-026-00673-8
الكلمات المفتاحية: أيض سرطان القولون والمستقيم, الخلايا الليفية المرتبطة بالسرطان, بيئة الورم المحيطة, تغايرية أيضية, النمذجة الحاسوبية