Clear Sky Science · de
Faserzellen in der Tumorumgebung treiben die metabolische Heterogenität von kolorektalen Krebszellen voran: Vorhersagen aus Stoffwechselmodellierung
Warum die Nachbarn der Zelle im Darmkrebs wichtig sind
Kolorektaler Krebs ist nicht einfach eine Ansammlung entarteter Zellen, die für sich allein wachsen. Tumorzellen leben in einer dichten Nachbarschaft aus Stütz‑ und Bindegewebszellen sowie chemischen Signalen, die alle beeinflussen können, wie sich der Krebs verhält und auf Therapien reagiert. Diese Studie stellt eine auf den ersten Blick einfache Frage: Wie verändern Helferzellen, sogenannte tumor‑assoziierte Fibroblasten, die Art und Weise, wie Kolonkarzinomzellen Nährstoffe und Energie nutzen, und könnten diese Veränderungen erklären, warum einige Tumoren gegen Stoffwechsel‑gerichtete Wirkstoffe resistent sind?
Versteckte Helfer in der Tumornachbarschaft
Fibroblasten sind normalerweise ruhige Baumeister des Bindegewebes, doch innerhalb von Tumoren werden sie häufig aktiviert und dann als tumor‑assoziierte Fibroblasten (TAFs oder CAFs) bezeichnet. Bei kolorektalen Tumoren mit KRAS‑Mutationen — einem häufigen und schwer zu behandelnden Treiber des Tumorwachstums — leisten CAFs mehr als nur strukturelle Unterstützung. Sie geben Metaboliten und Wachstumsfaktoren ab, die Tumorzellen nähren und sie dazu anregen können, ihren Umgang mit Zucker, Aminosäuren und anderen Nährstoffen umzubauen. Experimente haben gezeigt, dass Krebszellen, die in einem Medium wachsen, das zuvor CAFs beherbergt hat (sogenanntes CAF‑konditioniertes Medium), stärker auf zuckerverarbeitende Wege angewiesen sind und Anzeichen von Resistenz gegen bestimmte metabolische Wirkstoffe zeigen.
Mit Computermodellen viele mögliche Zukünfte erkunden
Anstatt einen einzelnen „besten“ Weg zu verfolgen, wie eine Krebszelle ihren Stoffwechsel betreiben könnte, verwendeten die Autoren einen rechnerischen Ansatz, der Tausende möglicher Stoffwechselzustände durchprobiert, die mit grundlegenden Beschränkungen wie Nährstoffaufnahme und Wachstum vereinbar sind. Sie begannen mit einem bereits vorhandenen, experimentell informierten Modell des zentralen Kohlenstoffstoffwechsels in KRAS‑mutierten kolorektalen Krebszellen, das Schlüsselwege umfasst, die Glukose und Glutamin verarbeiten und Bausteine für Wachstum erzeugen. Anschließend simulierten sie teilweise oder vollständige Verlangsamungen von 12 wichtigen Enzymen, überwiegend im Hauptweg des Zuckerabbaus und in einem angeschlossenen Verzweigungsweg. Jede Verlangsamung wurde in zwei virtuellen Umgebungen untersucht: Standard‑Krebszellmedium und CAF‑konditioniertes Medium.
Zahlreiche Routen durch das metabolische Labyrinth
Für jede simulierte Bedingung erzeugte das Modell 1.000 verschiedene Möglichkeiten, wie der Fluss — die Strömung von Material durch jede Stoffwechselreaktion — organisiert sein könnte. Das Team wandte moderne Mustererkennungswerkzeuge auf diese hochdimensionalen Daten an und komprimierte sie in zweidimensionale Karten, in denen jeder Punkt einen möglichen Stoffwechselzustand repräsentiert. Punkteansammlungen entsprechen typischen Zuständen, die Zellen einnehmen könnten. Beim Vergleich dieser Karten über die Bedingungen hinweg fanden die Autoren, dass sich Zellen im CAF‑konditionierten Medium in einem weiteren und vielfältigeren Bereich des metabolischen Raums bewegten als Zellen im Standardmedium. Anders gesagt förderten CAF‑abgeleitete Faktoren nach Enzymstörungen eine breitere Mischung metabolischer Strategien, mit weniger Fällen, in denen unterschiedliche Deaktivierungen zum selben Zustand konvergierten.
Verschiebungen von Wegen und Wachstum unter Stress
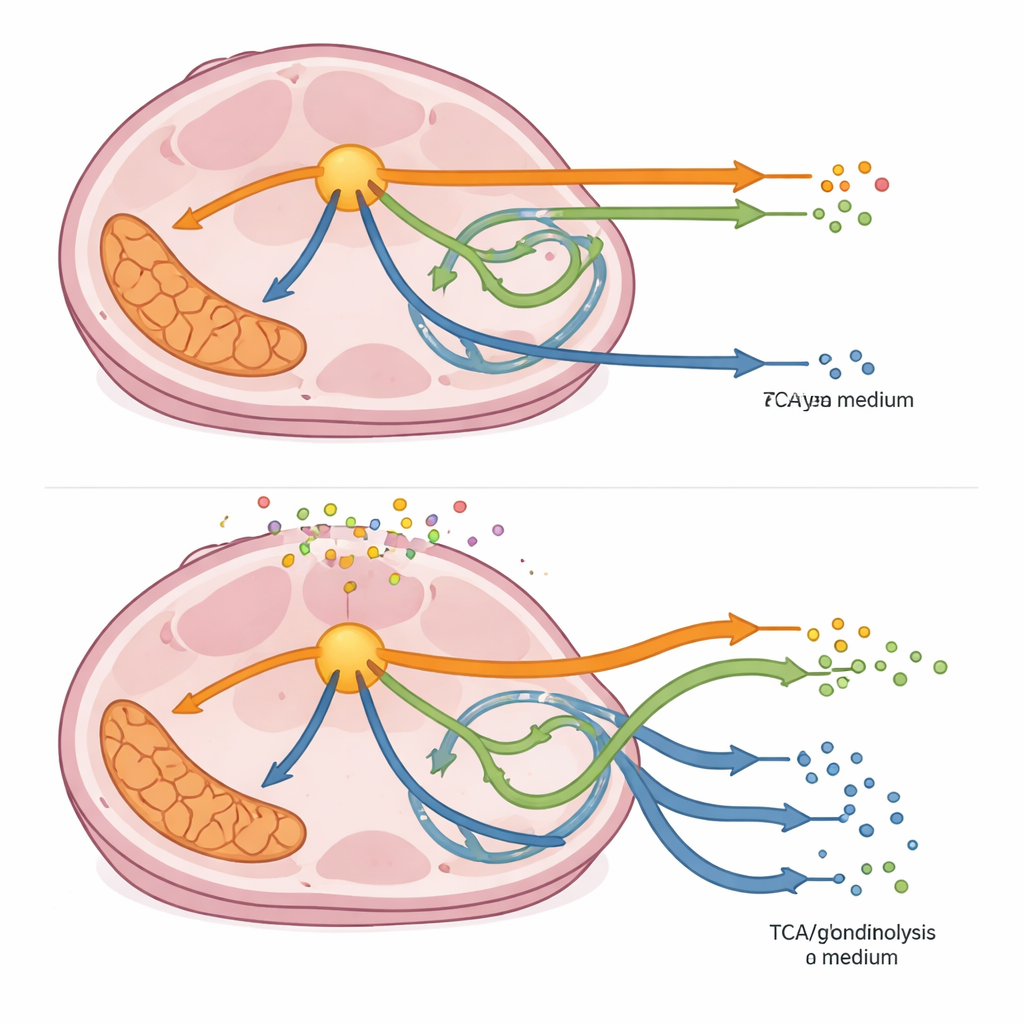
Durch das Summieren von Flüssen über gesamte Wege zeigte die Studie, dass das CAF‑konditionierte Medium die kolorektalen Krebszellen konsistent zu einer stärkeren Nutzung des Hauptwegs der Zuckerverarbeitung und weg von bestimmten mitochondrialen und verzweigten Wegaktivitäten drängte, selbst wenn Enzyme entlang dieser Wege teilweise gehemmt waren. Manche Störungen kehrten die Flussrichtung in Teilen des Verzweigungswegs um, was darauf hindeutet, dass Zellen Zwischenprodukte umleiten könnten, um Schlüsselmoleküle für Wachstum und Stressschutz zu regenerieren. Als die Forschenden den Wachstums‑Proxy des Modells — die Biomasseproduktion — betrachteten, stellten sie fest, dass jede Enzymverlangsamung das Wachstum verringerte, jedoch häufig weniger stark im CAF‑konditionierten Medium. In mehreren Fällen, insbesondere bei Blockaden an frühen Entscheidungsstellen, war das Wachstum im CAF‑konditionierten Medium widerstandsfähiger, was einen schützenden Effekt der Tumornachbarschaft unterstreicht.
Was das für künftige Behandlungen bedeutet
Für Nicht‑Spezialisten lautet die Hauptbotschaft: Krebszellen reagieren auf Stoffwechselmedikamente nicht isoliert; ihre Nachbarn und die umgebende Suppe aus ausgeschiedenen Molekülen können Ausweichrouten öffnen, die ihr Überleben ermöglichen. CAF‑konditioniertes Medium machte KRAS‑mutierte kolorektale Krebszellen metabolisch vielfältiger und in vielen Fällen besser in der Lage, simulierten Enzym‑gerichteten Therapien standzuhalten, obwohl einige Ziele das Wachstum dennoch stark einschränkten. Diese Arbeit legt nahe, dass erfolgreiche metabolische Behandlungen die Unterstützung durch Fibroblasten berücksichtigen oder gezielt stören müssen. Indem sie nicht nur einen einzelnen optimalen Weg, sondern eine ganze Landschaft möglicher Stoffwechselzustände abbildet, bietet die Studie einen reichhaltigeren Blick darauf, wo der Tumor am verwundbarsten ist — und wie seine Mikroumgebung diese Schwachstellen verschieben kann.
Zitation: Elton, E., Tavakoli, N., Cetin, H. et al. Cancer-associated fibroblasts drive metabolic heterogeneity in colorectal cancer cells: predictions from metabolic modeling. npj Syst Biol Appl 12, 54 (2026). https://doi.org/10.1038/s41540-026-00673-8
Schlüsselwörter: Stoffwechsel von kolorektalem Krebs, tumorassoziierte Fibroblasten, Tumormikroumgebung, metabolische Heterogenität, computationale Modellierung