Clear Sky Science · nl
Fibroblasten geassocieerd met kanker drijven metabole heterogeniteit in colorectale kankercellen: voorspellingen uit metabolisch modelleren
Waarom buren van cellen ertoe doen bij dikkedarmkanker
Colorectale kanker is niet zomaar een kluwen van losgeslagen cellen die op zichzelf groeien. Tumorcellen leven in een drukke buurt vol ondersteunende cellen, bindweefsel en chemische signalen, die allemaal kunnen bepalen hoe de kanker zich gedraagt en reageert op behandeling. Deze studie stelt een ogenschijnlijk eenvoudige vraag: op welke manier veranderen hulpcellen, zogenaamde kanker‑geassocieerde fibroblasten, de manier waarop colonkankercellen voedingsstoffen en energie gebruiken, en kunnen die veranderingen helpen verklaren waarom sommige tumoren resistent zijn tegen geneesmiddelen die op hun metabolisme gericht zijn?
Verborgen helpers in de tumorbuurt
Fibroblasten zijn van nature stille bouwers van bindweefsel, maar in tumoren worden ze vaak geactiveerd en dan aangeduid als kanker‑geassocieerde fibroblasten (CAF's). In colorectale kanker met mutaties in het KRAS‑gen — een veelvoorkomende en lastig te remmen motor van tumorgroei — doen CAF's meer dan alleen structuur bieden. Ze geven metabolieten en groeifactoren af die tumorcellen kunnen voeden en hen aanmoedigen hun verwerking van suiker, aminozuren en andere voedingsstoffen te herprogrammeren. Experimenten hebben aangetoond dat wanneer kankercellen worden gekweekt in het vloeibare medium waarin eerder CAF's hebben gezeten, het zogenoemde CAF‑geconditioneerde medium, ze zwaarder leunen op suiververbrandingsroutes en tekenen van resistentie tegen sommige metabole geneesmiddelen vertonen.
Met computermodellen veel mogelijke toekomsten verkennen
In plaats van één "beste" manier te volgen waarop een kankercel zijn metabolisme zou kunnen draaien, gebruikten de auteurs een computationele aanpak die duizenden mogelijke metabole toestanden bemonstert die in overeenstemming zijn met basisbeperkingen zoals nutriëntopname en groei. Ze vertrokken van een bestaand, experimenteel geïnformeerd model van centraal koolstofmetabolisme in KRAS‑gemuteerde colorectale kankercellen, inclusief sleutelroutes die glucose en glutamine verwerken en bouwstenen voor groei genereren. Vervolgens simuleerden ze gedeeltelijke of volledige vertragingen van 12 belangrijke enzymen, voornamelijk in de voornaamste suikerafbraakroute en een verbonden vertakking. Elke vertraging werd onderzocht in twee virtuele omgevingen: standaard kankercelmedium en CAF‑geconditioneerd medium.
Veel routes door het metabole doolhof
Voor elke gesimuleerde conditie produceerde het model 1.000 verschillende manieren waarop flux — de stroom van materiaal door elke metabole reactie — kon worden verdeeld. Het team paste moderne patroonherkenningstools toe op deze hoogdimensionale gegevens en perste ze samen tot tweedimensionale kaarten waarbij elk punt één mogelijke metabole toestand voorstelt. Clusters van punten komen overeen met typische toestanden die cellen kunnen aannemen. Door deze kaarten tussen condities te vergelijken, vonden de auteurs dat cellen in CAF‑geconditioneerd medium een wijder en gevarieerder gebied van metabole ruimte innamen dan cellen in standaard medium. Met andere woorden, door factoren afkomstig van CAF's werden na enzymperturbaties een breder scala aan metabole strategieën aangemoedigd, met minder gevallen waarin verschillende knockdowns op dezelfde toestand uitkwamen.
Verschuivingen in routes en groei onder stress
Door fluxen door hele paden op te tellen, toonde de studie aan dat CAF‑geconditioneerd medium colorectale kankercellen consequent richting zwaarder gebruik van de hoofdroute voor suikerverwerking duwde en weg van bepaalde mitochondriale en vertakkings‑padactiviteiten, zelfs wanneer enzymen langs deze routes gedeeltelijk werden geremd. Sommige perturbaties keerden de stroomrichting door delen van de vertakking om, wat suggereert dat cellen tussenproducten kunnen omleiden om sleutelmoleculen te regenereren die nodig zijn voor groei en bescherming tegen stress. Toen de onderzoekers de proxy van het model voor celdeling — biomassa‑productie — bekeken, vonden ze dat elke enzymvertraging de groei verminderde, maar vaak minder sterk in CAF‑geconditioneerd medium. In meerdere gevallen, vooral bij blokkade van enzymen op vroege beslispunten, was de groei in CAF‑geconditioneerd medium veerkrachtiger, wat het beschermende effect van de tumorbuurt benadrukt.
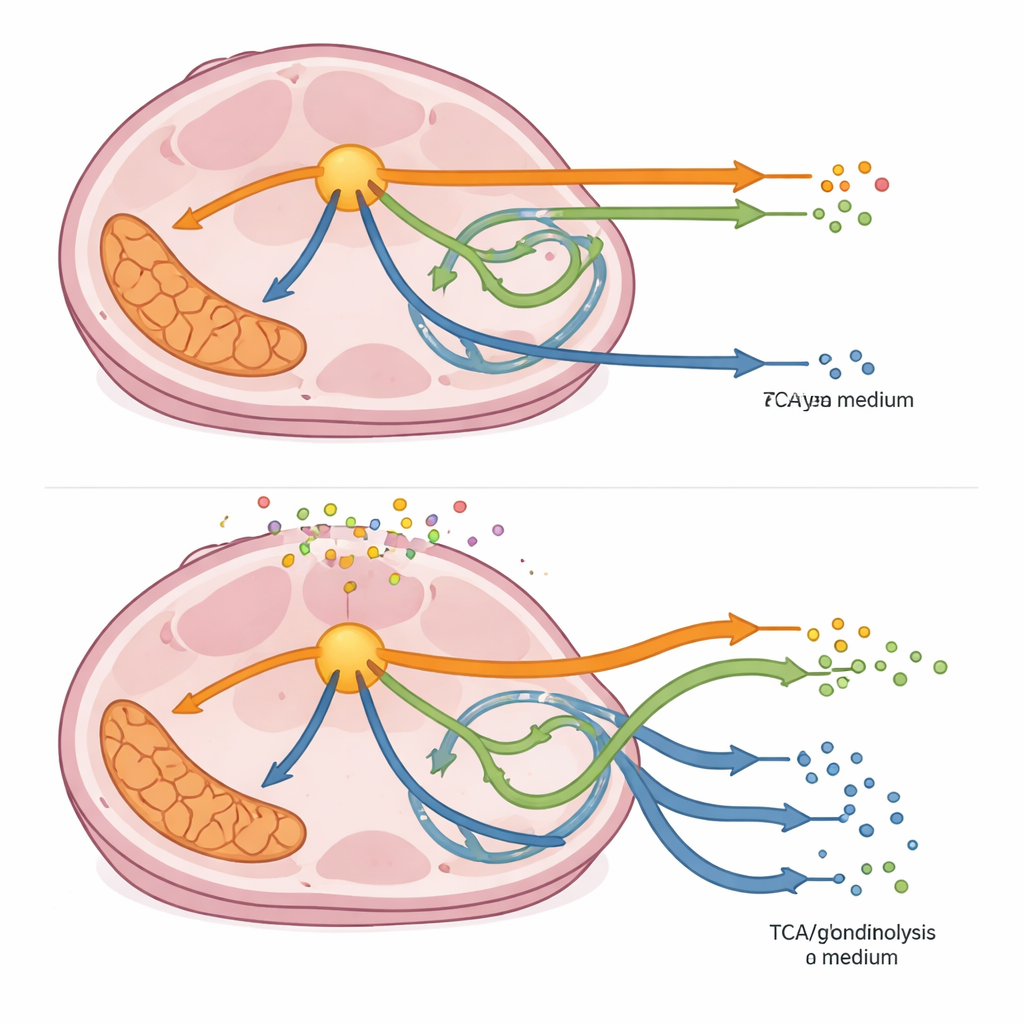
Wat dit betekent voor toekomstige behandelingen
Voor niet‑specialisten is de kernboodschap dat kankercellen niet losstaand reageren op metabole geneesmiddelen; hun buren en de omringende soep van uitgescheiden moleculen kunnen alternatieve routes openen die hen laten overleven. CAF‑geconditioneerd medium maakte KRAS‑gemuteerde colorectale kankercellen metabool diverser en in veel gevallen beter bestand tegen gesimuleerde enzymgerichte therapieën, hoewel sommige doelen nog steeds de groei sterk afremden. Dit werk suggereert dat succesvolle metabole behandelingen rekening moeten houden met, of zelfs direct het ondersteunende netwerk van fibroblasten moeten verstoren. Door niet slechts één optimale route in kaart te brengen maar een heel landschap van mogelijke metabole toestanden, biedt de studie een rijker beeld van waar de tumor het meest kwetsbaar is — en hoe zijn micro‑omgeving die zwakke plekken kan verschuiven.
Bronvermelding: Elton, E., Tavakoli, N., Cetin, H. et al. Cancer-associated fibroblasts drive metabolic heterogeneity in colorectal cancer cells: predictions from metabolic modeling. npj Syst Biol Appl 12, 54 (2026). https://doi.org/10.1038/s41540-026-00673-8
Trefwoorden: metabolisme van colorectale kanker, fibroblasten geassocieerd met kanker, tumormicro-omgeving, metabole heterogeniteit, computationeel modelleren