Clear Sky Science · es
Los fibroblastos asociados al cáncer impulsan la heterogeneidad metabólica en las células de cáncer colorrectal: predicciones a partir de modelos metabólicos
Por qué importan los vecinos celulares en el cáncer de colon
El cáncer colorrectal no es solo una masa de células rebeldes que crece por su cuenta. Las células tumorales viven en un vecindario concurrido lleno de células de soporte, tejido conectivo y señales químicas, todo lo cual puede moldear cómo se comporta el cáncer y cómo responde al tratamiento. Este estudio plantea una pregunta aparentemente simple: ¿cómo cambian las células auxiliares llamadas fibroblastos asociados al cáncer la forma en que las células de cáncer de colon usan nutrientes y energía, y podrían esos cambios ayudar a explicar por qué algunos tumores resisten fármacos dirigidos a su metabolismo?
Ayudantes ocultos en el vecindario tumoral
Los fibroblastos son constructores tranquilos del tejido conectivo, pero dentro de los tumores a menudo se activan y entonces se les denomina fibroblastos asociados al cáncer (CAF). En el cáncer colorrectal que presenta mutaciones en el gen KRAS —un impulsor del crecimiento tumoral habitual y difícil de atacar— los CAF hacen más que aportar estructura. Liberan metabolitos y factores de crecimiento que pueden alimentar a las células tumorales y animarlas a reconfigurar cómo procesan la glucosa, los aminoácidos y otros nutrientes. Experimentos han mostrado que cuando las células cancerosas se cultivan en el líquido que previamente albergó a CAF —llamado medio condicionado por CAF— dependen más de las vías de quema de azúcar y presentan signos de resistencia a algunos fármacos metabólicos.
Usar modelos informáticos para explorar muchos futuros posibles
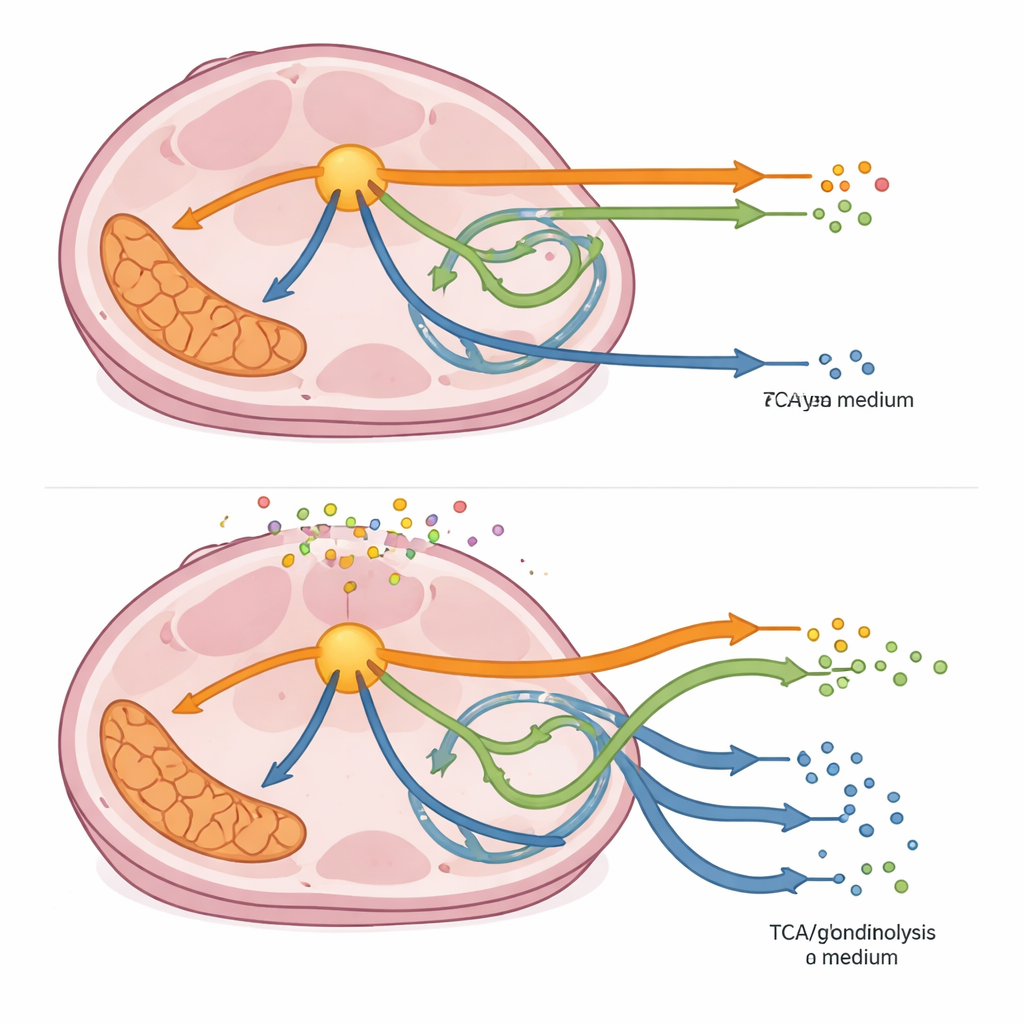
En lugar de seguir una sola «mejor» forma en que una célula cancerosa podría ejecutar su metabolismo, los autores emplearon un enfoque computacional que muestrea miles de estados metabólicos posibles consistentes con restricciones básicas como la captación de nutrientes y el crecimiento. Partieron de un modelo existente, informado experimentalmente, del metabolismo central del carbono en células de cáncer colorrectal con mutación KRAS, incluyendo vías clave que procesan glucosa y glutamina y generan bloques de construcción para el crecimiento. Luego simularon desaceleraciones parciales o completas de 12 enzimas importantes, principalmente en la ruta principal de descomposición de azúcares y una vía ramificada conectada. Cada desaceleración se exploró en dos entornos virtuales: medio estándar para células cancerosas y medio condicionado por CAF.
Muchas rutas a través del laberinto metabólico
Para cada condición simulada, el modelo produjo 1.000 formas diferentes en que el flujo —el paso de material a través de cada reacción metabólica— podría organizarse. El equipo aplicó herramientas modernas de reconocimiento de patrones a estos datos de alta dimensión, comprimiéndolos en mapas bidimensionales donde cada punto representa un posible estado metabólico. Los conglomerados de puntos corresponden a estados típicos que las células podrían adoptar. Al comparar estos mapas entre condiciones, los autores hallaron que las células en medio condicionado por CAF ocuparon una región de espacio metabólico más amplia y variada que las células en medio estándar. En otras palabras, los factores derivados de CAF fomentaron una mezcla más amplia de estrategias metabólicas tras las perturbaciones enzimáticas, con menos casos en los que diferentes inhibiciones convergían en el mismo estado.
Cambios en vías y crecimiento bajo estrés
Sumando los flujos a través de vías enteras, el estudio reveló que el medio condicionado por CAF empujaba de forma consistente a las células de cáncer colorrectal hacia un uso mayor de la ruta principal de procesamiento de azúcares y alejándolas de ciertas actividades mitocondriales y de vías ramificadas, incluso cuando las enzimas a lo largo de esas rutas estaban parcialmente inhibidas. Algunas perturbaciones invirtieron la dirección del flujo a través de partes de la vía ramificada, lo que sugiere que las células podrían redirigir intermediarios para regenerar moléculas clave necesarias para el crecimiento y la protección contra el estrés. Cuando los investigadores examinaron el proxy del modelo para el crecimiento celular —la producción de biomasa— encontraron que toda desaceleración enzimática reducía el crecimiento, pero a menudo en menor medida en medio condicionado por CAF. En varios casos, especialmente al bloquear enzimas en puntos de decisión tempranos, el crecimiento en medio condicionado por CAF fue más resistente, destacando un efecto protector del vecindario tumoral.
Qué significa esto para tratamientos futuros
Para un no especialista, el mensaje principal es que las células cancerosas no responden a los fármacos metabólicos de forma aislada; sus vecinos y la sopa circundante de moléculas secretadas pueden abrir rutas alternativas que les permiten sobrevivir. El medio condicionado por CAF hizo que las células de cáncer colorrectal con mutación KRAS fueran más diversas metabólicamente y, en muchos casos, mejor capaces de soportar terapias simuladas dirigidas a enzimas, aunque algunos objetivos aún reducían drásticamente el crecimiento. Este trabajo sugiere que los tratamientos metabólicos exitosos deberán tener en cuenta, o incluso interrumpir directamente, el apoyo que proporcionan los fibroblastos. Al mapear no solo una vía óptima sino todo un paisaje de estados metabólicos posibles, el estudio ofrece una visión más rica de dónde el tumor es más vulnerable —y cómo su microambiente puede desplazar esos puntos débiles.
Cita: Elton, E., Tavakoli, N., Cetin, H. et al. Cancer-associated fibroblasts drive metabolic heterogeneity in colorectal cancer cells: predictions from metabolic modeling. npj Syst Biol Appl 12, 54 (2026). https://doi.org/10.1038/s41540-026-00673-8
Palabras clave: metabolismo del cáncer colorrectal, fibroblastos asociados al cáncer, microambiente tumoral, heterogeneidad metabólica, modelado computacional