Clear Sky Science · tr
Perinatal dönemde uygun motor fonksiyonları LAT1 amino asit taşıyıcısı koordine eder
Hareket ve çocukluk hastalıkları için bunun önemi
Akıcı hareket etmeyi öğrenmek, yeni doğmuş bir sinir sisteminin ustalaşması gereken en büyük görevlerden biridir. Bu çalışma, amino asitleri sinir hücrelerine taşıyan tek bir proteinin, yeni doğmuş farelerin omuriliğinin kaslarını kontrol etmesini sağlayan devreleri nasıl kurup korumalarına yardımcı olduğunu ortaya koyuyor. Benzer devrelerin insan motor nöron hastalıklarında, örneğin spinal müsküler atrofide hasar gördüğü düşünüldüğünde, bu iş erken dönem beslenme ve hücresel taşıma sistemlerinin uzun vadeli motor sağlığı nasıl etkileyebileceğine dair yeni bir bakış açısı sunuyor. 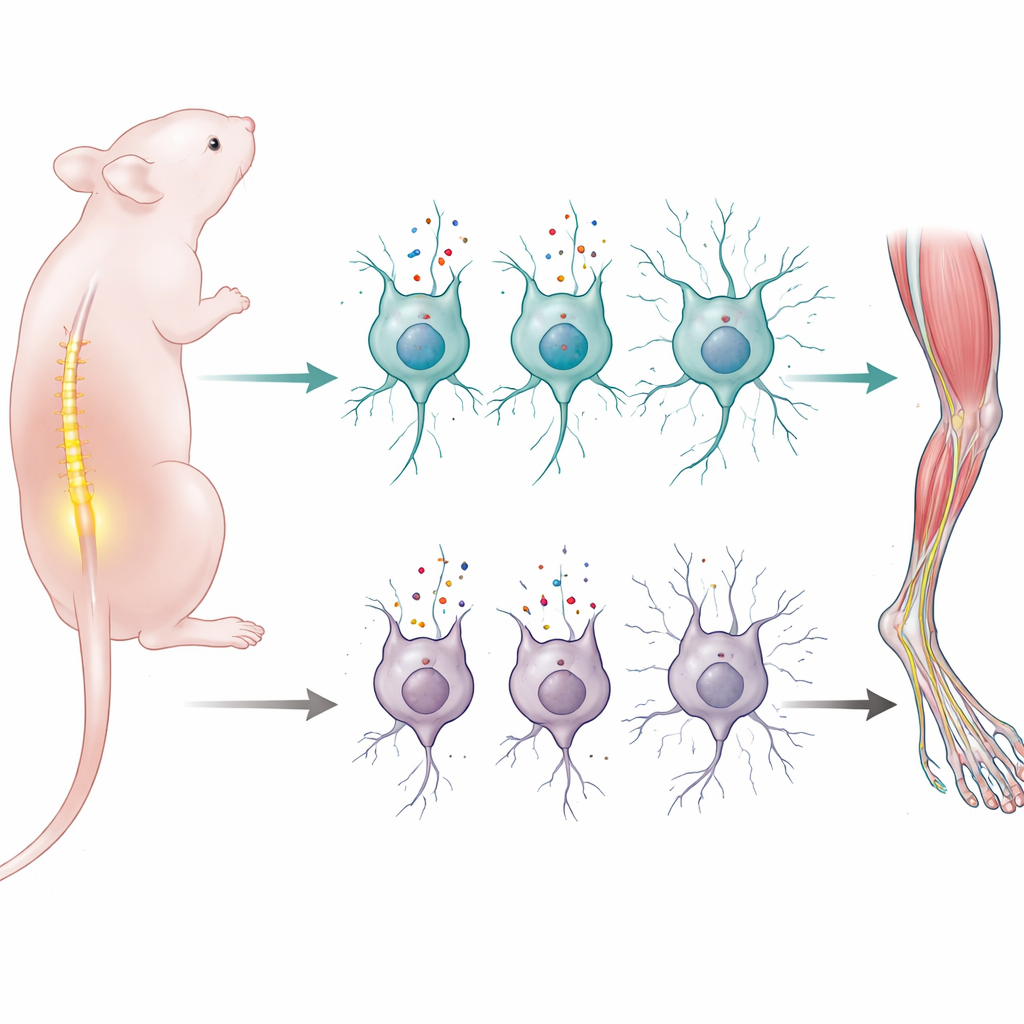
Sinir hücrelerinde bir besin kapısı
Araştırmacılar LAT1 adlı bir proteine odaklandı; bu protein büyük nötr amino asitler—birçok hücresel sürecin yapı taşları ve yakıtı—için belirli sinir hücrelerine açılan bir kapı görevi görür. LAT1 tüm vücuda eşit dağılmaz: belirli dokularda ve belirli zamanlarda, doğum çevresi de dahil olmak üzere güçlü şekilde etkinleştirilir. Önceki çalışmalar, LAT1 geninin farelerde tamamen ortadan kaldırılmasının ciddi beyin gelişim sorunlarına ve doğumdan önce veya kısa süre sonra ölüme yol açtığını göstermişti, ancak hangi sinir hücresi tiplerinin bu taşıyıcıya kesinlikle bağımlı olduğu net değildi.
LAT1’i belirli nöronlarda kapatmak
LAT1’in rolünü belirlemek için ekip, LAT1 genini (Slc7a5) yalnızca sinapsin 1 adlı yaygın bir sinir hücresi proteinini ifade eden nöronlarda ortadan kaldıran fareler üretti. Bu fareler doğumda normal görünüyordu ve beklenen sayıda doğdular; bu da erken beyin oluşumunun yine de gerçekleşebildiğini gösteriyordu. Ancak yaşamın ilk iki haftası içinde genç farelerde çarpıcı motor sorunlar gelişti: zayıf, denge ve koordinasyonu ölçen testlerde sakar ve normal kilo alamadılar. Üç haftadan fazla yaşamayan hiçbir birey kalmadı; bu da motor devrelerin rafine edildiği perinatal dönemde LAT1’e kritik bir bağımlılık olduğunu düşündürdü.
Omurilik hasarı ama beyin korunmuş
Bilim insanları sinir sistemini mikroskop altında incelediklerinde en çarpıcı hasarın alt omurilikte olduğunu gördüler; burada doğrudan uzuv kaslarını sürdüren motor nöronlar bulunur. İki haftalıkken mutant farelerde bu motor nöronların yaklaşık yarısı yok olmuştu; özellikle güçlü kas liflerini kontrol eden daha büyük hücreler kaybolmuştu. Hücre öz-yıkımı belirtileri ve aşırı hücresel “öz-temizleme” (otofaji) belirtileri daha da erken ortaya çıktı; bu da hücre ölümüne götüren bir stres yolunu işaret ediyordu. Omurilikteki çevreleyici destek hücreleri—astroglia, mikroglia ve miyelin üreten hücreler—de güçlü reaktif değişiklikler gösterdi; bu yerel yaralanmanın bir işaretiydi. Buna karşılık, hareket kontrolüne katkıda bulunan beyin bölgeleri olan motor korteks ve serebellum yapısal olarak normal görünüyordu; belirgin nöron kaybı veya skarlaşma yoktu; bu da asıl hasarın alt motor nöronlarda yoğunlaştığını vurguluyor. 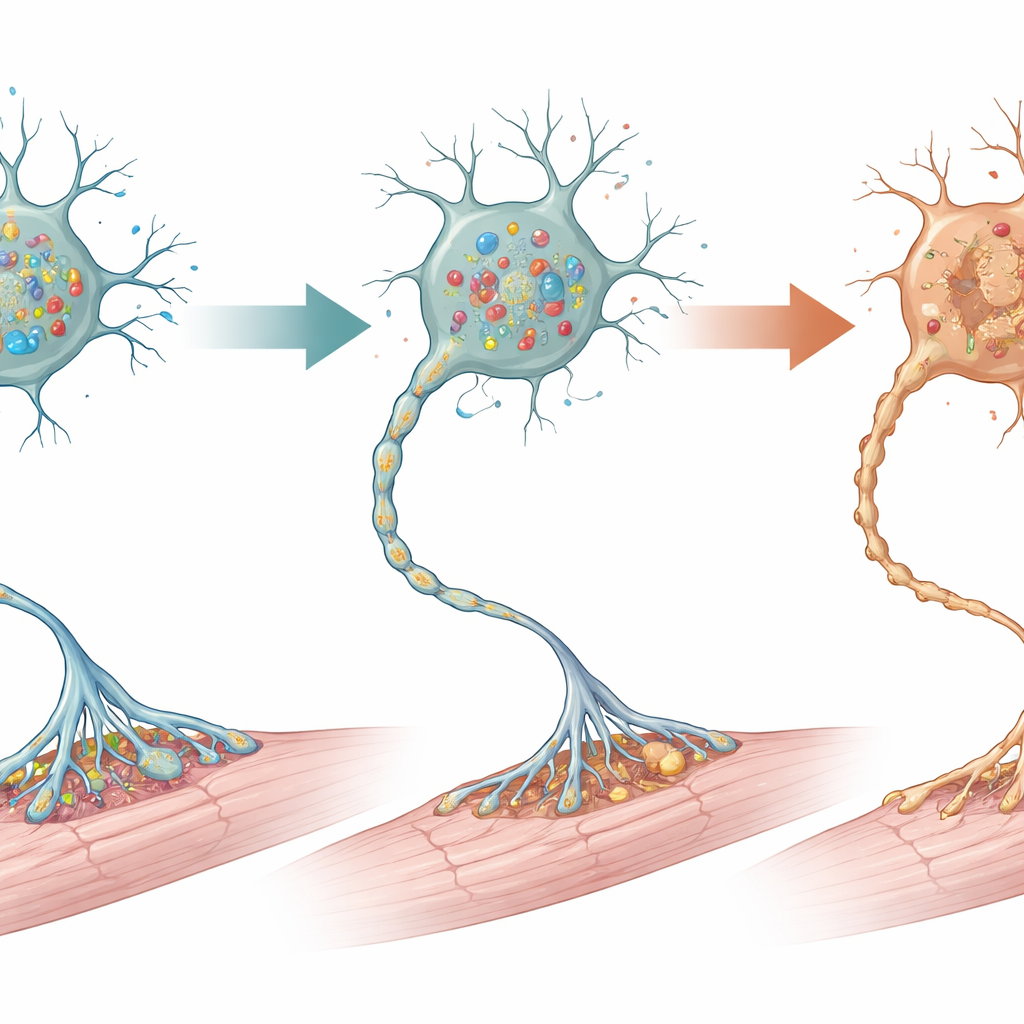
Kaslar, bağlantılar ve kısmi bir kurtarma
Omurilik motor nöron kaybının sonuçları kaslara doğru genişledi. Erken dönemde kas lifleri normal görünürken, ikinci haftaya gelindiğinde küçülmüşlerdi; bu bariz bir atrofi işaretiydi. Sinir–kas bağlantı noktaları, yani nöromüsküler kavşaklar, alışılmış karmaşık şekillerini kaybetti ve birçoğu yalnızca kısmen sinir lifleriyle beslenir hale geldi veya tamamen bağlantısını yitirdi. Hücre ölümü yollarının bu düşüşe yol açıp açmadığını test etmek için ekip, genç farelere programlı hücre ölümü biçimini baskılayan calpeptin adlı bir ilaç verdi. Tedavi edilen hayvanlar daha uzun yaşadı, daha fazla omurilik motor nöronunu korudu ve tedavi edilmeyen mutantlara göre daha iyi oluşmuş nöromüsküler kavşaklara sahip oldu; ancak tedavi hastalığı tamamen engellemedi.
Çocukluk dönemi motor nöron hastalıklarıyla bağlantılar
Erken alt motor nöron kaybı ve başarısız nöromüsküler kavşak deseninin spinal müsküler atrofiye benzediği göz önüne alındığında, araştırmacılar bu hastalığın fare modellerinden gelen birkaç büyük genetik veri kümesini de incelediler. Birden fazla bağımsız çalışmada amino asit taşıması ve metabolizmasıyla ilgili genlerin, Slc7a5 dahil, etkilenen motor nöronlarda aşağı doğru düzenlendiğini; hücre ölümü ve glial aktivasyonla ilişkili genlerin ise yukarı doğru düzenlendiğini buldular. Bu yakınsama, zayıflamış amino asit taşınmasının erken başlangıçlı motor nöron bozukluklarında ortak bir ipucu olabileceğini ve hassas omurilik motor nöronlarında LAT1 işlevinin korunması veya artırılmasının bu tür durumların tanısı veya tedavisinde umut verici bir strateji olabileceğini gösteriyor.
Hareket sağlığı için çıkarılacak mesaj
Basitçe söylemek gerekirse, bu çalışma yeni doğmuş farelerde belirli omurilik motor nöronlarının hayatta kalmak ve kasla güçlü bağlantılar kurmak için özel bir amino asit “tedarik kapısına” bağımlı olduğunu gösteriyor. Bu kapı LAT1’in uzaklaştırılmasıyla kapandığında, nöronlar kritik besinlerden yoksun kalıyor, strese giriyor ve ölüyor; bu da zayıf, eriyen kaslara ve erken ölüme yol açıyor. Bu yolu spinal müsküler atrofi modellerinde görülen desenlerle ilişkilendirerek çalışma, amino asit taşınmasını—özellikle LAT1 proteinini—ciddi erken dönem hareket bozukluklarını anlamak ve nihayetinde müdahale etmek için potansiyel bir yeni hedef olarak öne çıkarıyor.
Atıf: Sadamori, K., Hiraiwa, M., Horie, T. et al. The amino acid transporter LAT1 coordinates proper motor function at the perinatal stage. Cell Death Dis 17, 345 (2026). https://doi.org/10.1038/s41419-026-08663-8
Anahtar kelimeler: motor nöronlar, amino asit taşınması, LAT1, spinal müsküler atrofi, nöromüsküler bağlantı