Clear Sky Science · ar
ناقِل الأحماض الأمينية LAT1 ينسق الوظيفة الحركية السليمة في مرحلة حول الولادة
لماذا يهم هذا للحركة وأمراض الطفولة
تعلم الحركة بانسيابية هو أحد أكبر المهام التي يجب على جهاز الأعصاب لدى المولود إتقانها. تكشف هذه الدراسة كيف يساعد بروتين واحد ينقل الأحماض الأمينية إلى الخلايا العصبية فئران المولودة على بناء وصيانة الدارات التي تُمكّن الحبل الشوكي من التحكم بعضلاتها. وبما أن شبكات مماثلة تتعرض للضرر في أمراض الخلايا العصبية الحركية لدى الإنسان مثل ضمور العضلات الشوكي، يشير هذا العمل إلى طريقة جديدة للتفكير في كيفية تأثير التغذية المبكرة وأنظمة نقل الخلايا على الصحة الحركية الطويلة الأمد. 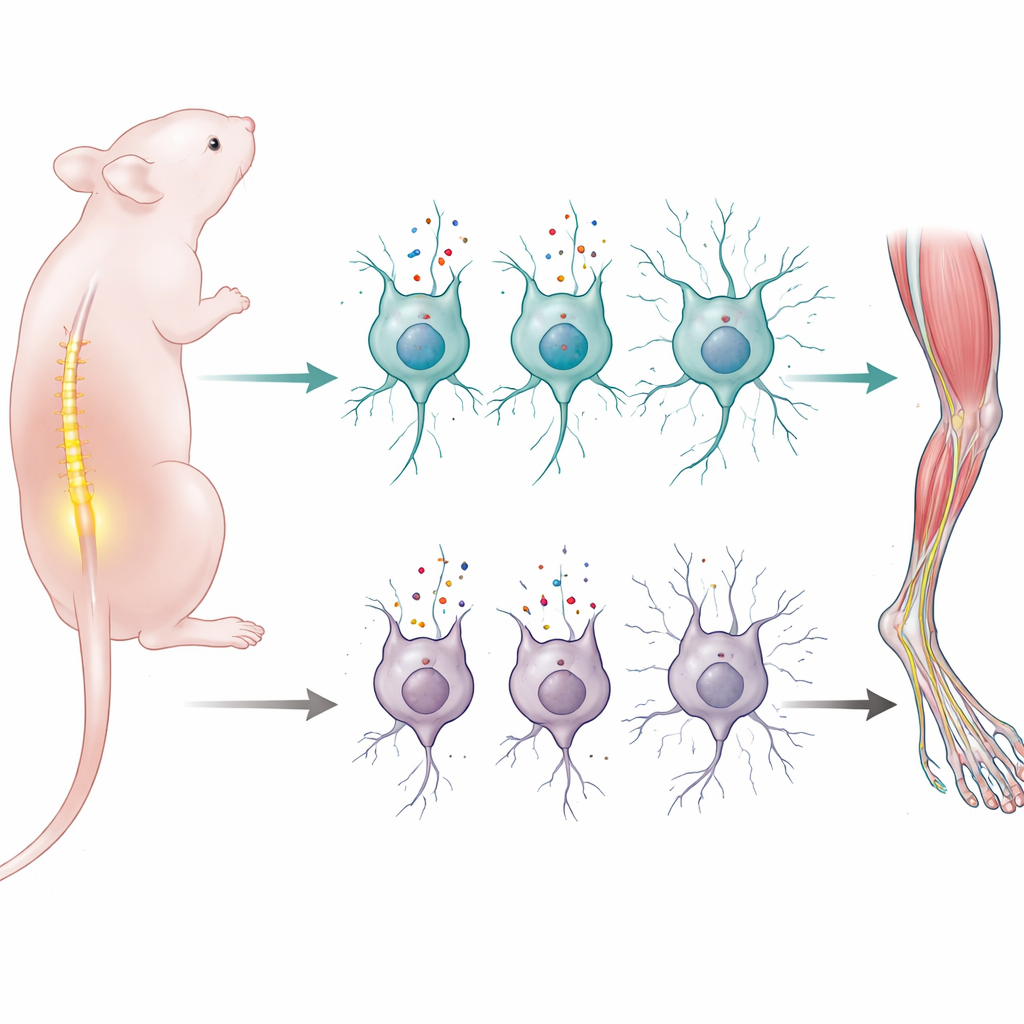
بوابة مغذّية في الخلايا العصبية
ركّز الباحثون على بروتين يُسمى LAT1، الذي يعمل كبوابة للأحماض الأمينية المتعادلة الكبيرة — اللبنات والوقود للعديد من العمليات الخلوية — إلى أنواع معينة من الخلايا العصبية. لا ينتشر LAT1 بشكل متساوٍ في الجسم: يُعبّر عنه بقوة في أنسجة وأوقات محددة، بما في ذلك حول وقت الولادة. أظهرت أعمال سابقة أن حذف جين LAT1 تمامًا في الفئران يسبب مشاكل شديدة في نمو الدماغ والموت قبل أو بعد الولادة بقليل، لكن لم يتضح أي أنواع الخلايا العصبية تعتمد بشكل حاسم على هذا الناقل لتعمل.
إيقاف LAT1 في نيورونات محددة
لتحديد دور LAT1 بدقة، تربّى الفريق فئرانًا حُذِف فيها جين LAT1 (Slc7a5) فقط في الخلايا العصبية التي تعبّر عن بروتين شائع للخلايا العصبية يُدعىسينابسيسن 1. ظهر أن هذه الفئران طبيعية عند الولادة ووُلدت بالأعداد المتوقعة، ما يعني أن تكون الدماغ المبكر يمكن أن يحدث. لكن خلال الأسبوعين الأولين من العمر طوّرت الفئران الصغيرة مشاكل حركية واضحة: كانت ضعيفة، أخرق في الاختبارات التي تقيس التوازن والتنسيق، وفشلت في اكتساب الوزن الطبيعي. لم ينجُ أحد منها بعد ثلاثة أسابيع، مما يشير إلى اعتماد حاسم على LAT1 خلال الفترة المحيطة بالولادة حين تُصقل دوائر الحركة.
ضرر في الحبل الشوكي لكن دماغ محمي
عندما فحص العلماء الجهاز العصبي تحت المجهر، وجدوا أن الضرر الأكثر درامية كان في الجزء السفلي من الحبل الشوكي، حيث توجد الخلايا العصبية الحركية التي تُحرّك العضلات الطرفية مباشرة. بحلول الأسبوع الثاني، اختفت نحو نصف هذه الخلايا العصبية الحركية في الفئران المعدّلة، وخاصة الخلايا الأكبر حجمًا التي تتحكم عادة في ألياف العضلات القوية. ظهرت علامات تحلل ذاتي للخلايا وزيادة في «التنظيف الذاتي» الخلوي (الالتهام الذاتي) في وقت أبكر، مما يلمح إلى مسار إجهاد يقود إلى موت الخلايا. كما أبدت خلايا الدعم المحيطة في الحبل الشوكي — الخلايا النجمية، والماكروفاجات الدقيقة، وخلايا المايلين — تغيّرات تفاعلية قوية، وهو علامة مميزة للإصابة المحلية. بالمقابل، بدا قشرة الحركة والمخيخ في الدماغ سليمين من الناحية البنيوية، دون فقد واضح للخلايا العصبية أو ندب، مما يؤكد أن الضرر الرئيسي كان مركزًا في الخلايا العصبية الحركية السفلية. 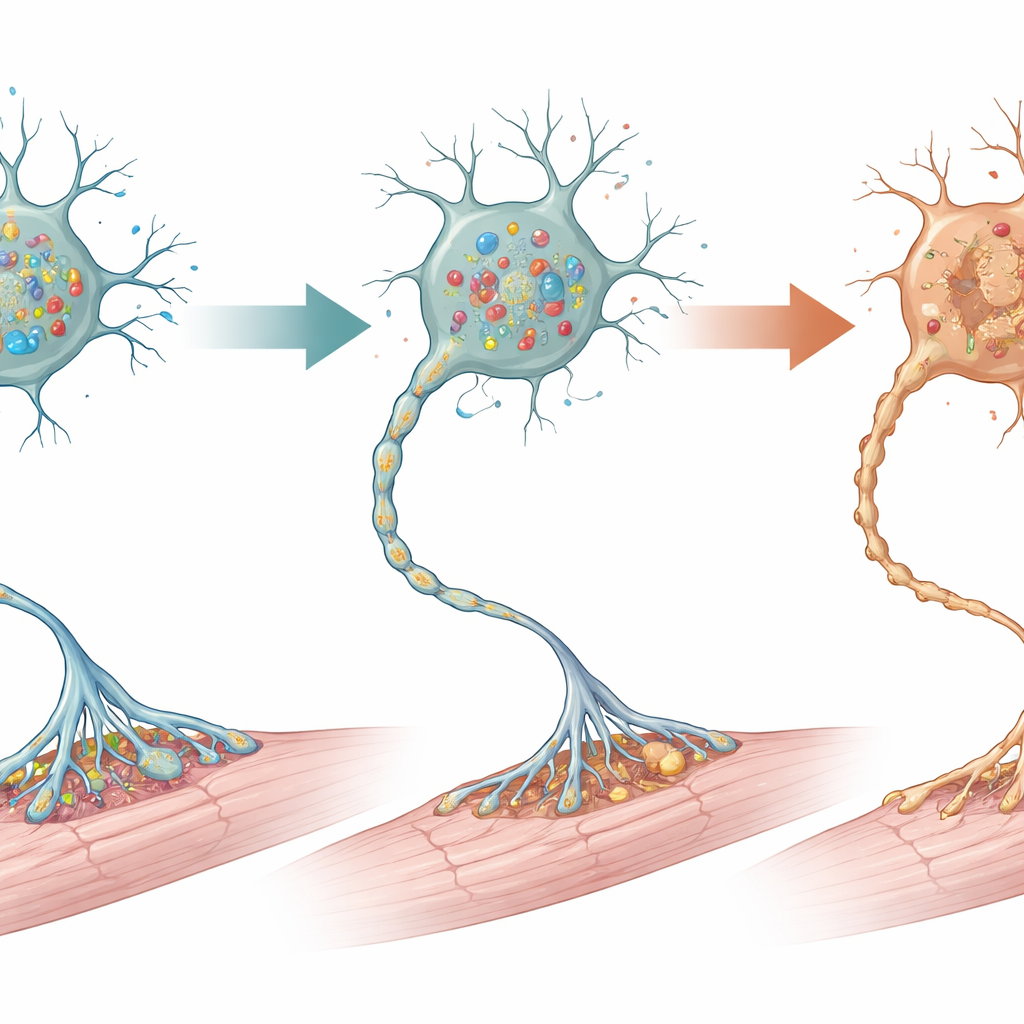
العضلات والتشابك العصبي-العضلي وإنقاذ جزئي
امتد تأثير فقدان الخلايا العصبية الحركية الشوكية إلى العضلات. في المراحل المبكرة بدت ألياف العضلات طبيعية، لكن بحلول الأسبوع الثاني تقلصت، وهو علامة واضحة على الضمور. فقدت نقاط الاتصال بين العصب والعضلة، المعروفة بالتشابكات العصبية-العضلية، شكلها المعقد الاعتيادي وكثير منها أصبح مزودًا جزئيًا فقط أو منفصلاً تمامًا عن الألياف العصبية. لاختبار ما إذا كانت مسارات موت الخلايا تدفع هذا التدهور، عالج الفريق الفئران الصغيرة بكالفبتين، دواء يخفف شكلًا من أشكال الموت الخلوي المبرمج. عاشت الحيوانات المعالجة لفترة أطول، واحتفظت بعدد أكبر من الخلايا العصبية الحركية الشوكية، وكانت تشابكاتها العصبية-العضلية أفضل تكوّنًا مقارنةً بالطفرة غير المعالجة، رغم أن العلاج لم يوقِف المرض تمامًا.
روابط مع مرض الخلايا العصبية الحركية لدى الأطفال
لأن نمط فقدان الخلايا العصبية الحركية السفلية المبكر وفشل التشابكات العصبية-العضلية شابه ضمور العضلات الشوكي، فحص الباحثون أيضًا عدة مجموعات بيانات وراثية كبيرة من نماذج الفئران لذلك المرض. عبر دراسات مستقلة متعددة، وجدوا أن الجينات المشاركة في نقل الأحماض الأمينية و أيضها، بما في ذلك Slc7a5، كانت منخفضة التعبير في الخلايا العصبية المتأثرة، بينما كانت الجينات المرتبطة بموت الخلايا وتنشيط الخلايا الدبقية مرتفعة التعبير. تشير هذه التقاطعات إلى أن ضعف نقل الأحماض الأمينية قد يكون خيطًا مشتركًا في اضطرابات الخلايا العصبية الحركية المبكرة، وأن حفظ أو تعزيز وظيفة LAT1 في الخلايا العصبية الحركية الشوكية المعرضة للخطر قد يكون استراتيجية واعدة مستقبلًا لتشخيص أو معالجة مثل هذه الحالات.
الرسالة الأساسية لصحة الحركة
بعبارة بسيطة، تُظهر هذه الدراسة أن خلايا عصبية حركية شوكية معينة في الفئران المولودة تعتمد على «باب توريد» متخصص للأحماض الأمينية للبقاء وتشكيل وصلات قوية مع العضلات. عندما يُغلق هذا الباب بحذف LAT1، تنفد الخلايا من المواد المغذية الأساسية، فتتعرض للإجهاد وتموت، مما يؤدي إلى ضعف العضلات وضمورها والموت المبكر. بربط هذا المسار بأنماط مرصودة في نماذج ضمور العضلات الشوكي، تبرز الدراسة نقل الأحماض الأمينية — وبروتين LAT1 على وجه الخصوص — كمقبض جديد محتمل لفهم التدخل يومًا ما في اضطرابات الحركة الشديدة في الحياة المبكرة.
الاستشهاد: Sadamori, K., Hiraiwa, M., Horie, T. et al. The amino acid transporter LAT1 coordinates proper motor function at the perinatal stage. Cell Death Dis 17, 345 (2026). https://doi.org/10.1038/s41419-026-08663-8
الكلمات المفتاحية: خلايا الأعصاب الحركية, نقل الأحماض الأمينية, LAT1, ضمور العضلات الشوكي, وصل عصبي-عضلي