Clear Sky Science · sv
Aminosyretransportören LAT1 samordnar korrekt motorisk funktion i perinatalstadiet
Varför detta spelar roll för rörelse och barndomssjukdom
Att lära sig röra sig smidigt är en av de största uppgifterna ett nyfött nervsystem måste klara. Denna studie avslöjar hur ett enda protein som transporterar aminosyror in i nervceller hjälper nyfödda möss att bygga och upprätthålla den koppling som låter ryggmärgen kontrollera musklerna. Eftersom liknande kopplingar skadas vid mänskliga motorneuronsjukdomar som spinal muskelatrofi, pekar arbetet på ett nytt sätt att tänka på hur tidig näring och cellulära transportsystem kan påverka långsiktig motorisk hälsa. 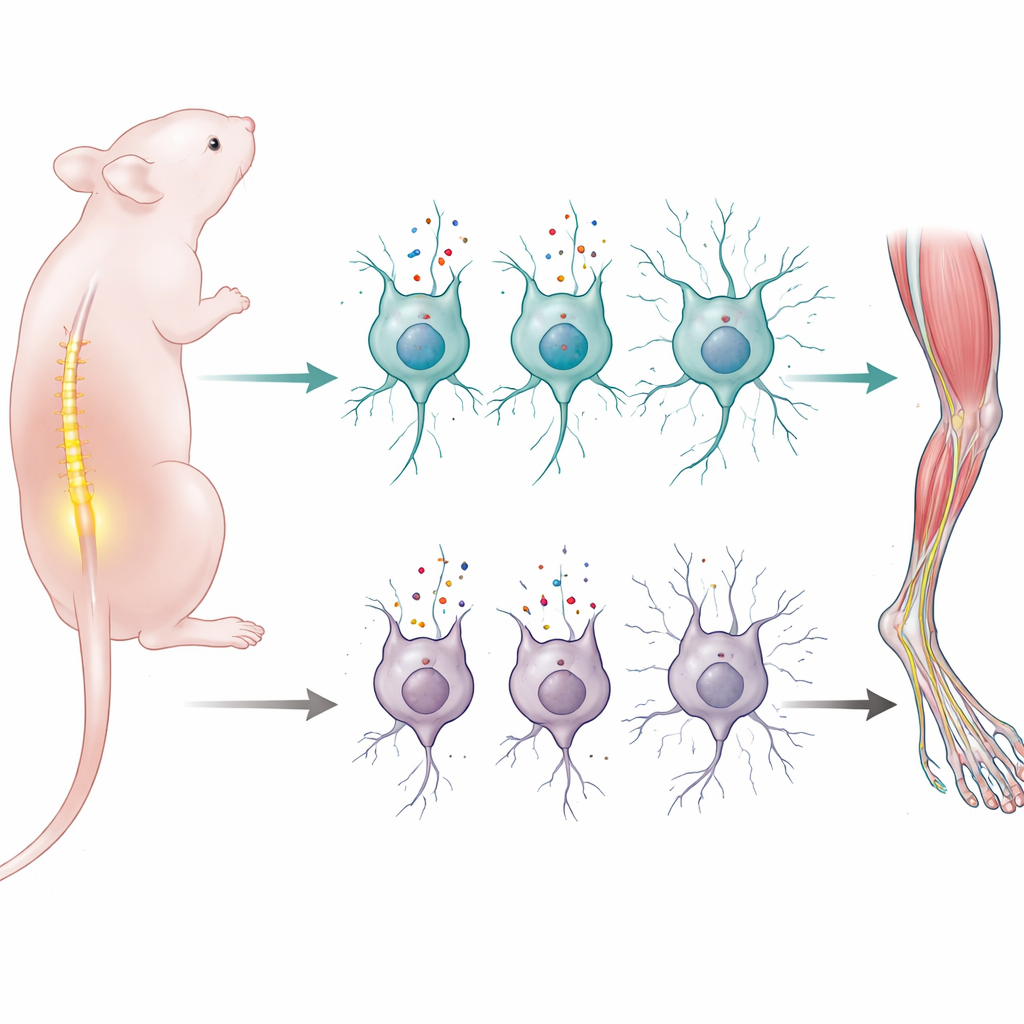
En näringsport i nervcellerna
Forskarna fokuserade på ett protein kallat LAT1, som fungerar som en port för stora neutrala aminosyror — byggstenar och bränsle för många cellulära processer — in i vissa nervceller. LAT1 är inte jämt fördelat i kroppen: det aktiveras starkt i särskilda vävnader och vid särskilda tidpunkter, bland annat runt födseln. Tidigare arbete hade visat att att ta bort LAT1-genen helt hos möss ger allvarliga problem i hjärnans utveckling och död före eller strax efter födseln, men det var inte klart vilka nervcellstyper som absolut var beroende av denna transportör för att fungera.
Stänga av LAT1 i specifika neuroner
För att precisera LAT1:s roll avlade teamet fram möss där LAT1-genen (Slc7a5) togs bort endast i neuroner som uttrycker ett vanligt nervcellsprotein kallat synapsin 1. Dessa möss såg normala ut vid födseln och föddes i förväntade antal, vilket innebar att tidig hjärnbildning fortfarande kunde ske. Men inom de första två veckorna utvecklade ungarna markanta motoriska problem: de var svaga, klumpiga i tester som mätte balans och koordination, och gick inte upp i normal vikt. Ingen överlevde längre än tre veckor, vilket tyder på ett kritiskt beroende av LAT1 under den perinatala perioden när motoriska kretsar finslipas.
Skador i ryggmärgen men bevarad hjärna
När forskarna undersökte nervsystemet i mikroskop fann de att den mest dramatiska skadan fanns i nedre delen av ryggmärgen, där motorneuroner som direkt driver lemmuskelatur sitter. Vid två veckors ålder var cirka hälften av dessa motorneuroner förlorade i de mutanta mössen, särskilt de större cellerna som vanligtvis kontrollerar kraftfulla muskelfibrer. Tecken på celldestruktion och överdriven cellulär ”självrengöring” (autofagi) dök upp ännu tidigare, vilket antyder en stressväg som leder till celldöd. Omgivande stödjeceller i ryggmärgen — astrocyter, mikroglia och myelinskidproducerande celler — visade också kraftiga reaktiva förändringar, ett kännetecken för lokal skada. I kontrast såg motorcortex och cerebellum i hjärnan, som också deltar i rörelsekontroll, strukturellt normala ut utan uppenbar förlust av neuroner eller ärrbildning, vilket understryker att den centrala skadan koncentrerades till nedre motorneuroner. 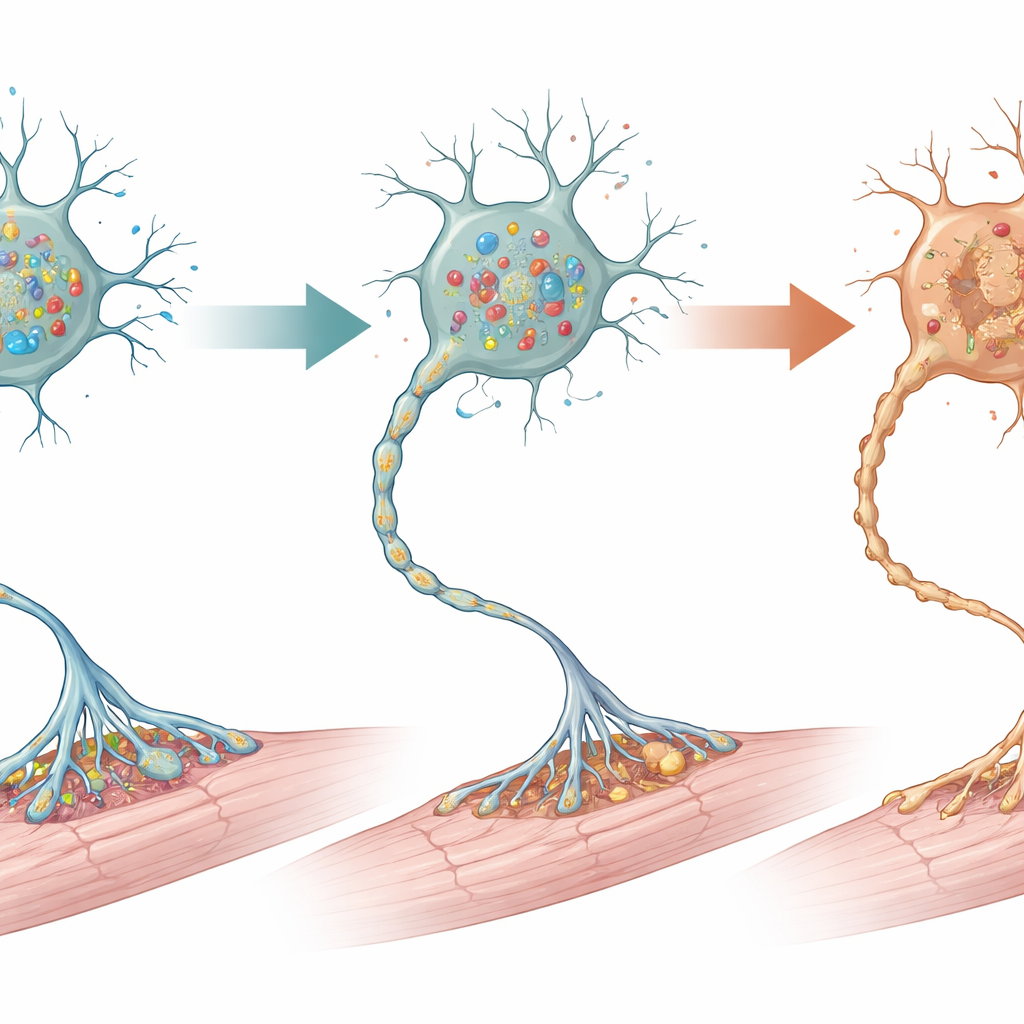
Muskler, kopplingar och en partiell räddning
Konsekvenserna av förlust av spinala motorneuroner spred sig ut till musklerna. Tidigt såg muskelfibrerna normala ut, men under den andra veckan hade de krympt, ett tydligt tecken på atrofi. Nerv–muskel-kopplingspunkterna, kallade neuromuskulära synapser, förlorade sin vanliga invecklade form och många blev bara delvis försörjda eller helt frånkopplade från sina nervfibrer. För att testa om celldödsprocesser drev denna nedgång behandlade teamet unga möss med kalpeptin, ett läkemedel som dämpar en form av programmerad celldöd. Behandlade djur levde längre, behöll fler spinala motorneuroner och hade bättre formade neuromuskulära kopplingar än obehandlade mutanter, även om behandlingen inte helt förhindrade sjukdomen.
Kopplingar till barndomens motorneuronsjukdom
Eftersom mönstret med tidig förlust av nedre motorneuroner och försämrade neuromuskulära förbindelser liknade spinal muskelatrofi, granskade forskarna också flera stora genetiska dataset från musmodeller av den sjukdomen. I flera oberoende studier fann de att gener involverade i aminosyratransport och metabolism, inklusive Slc7a5, var nedreglerade i drabbade motorneuroner, medan gener kopplade till celldöd och glial aktivering var uppreglerade. Denna konvergens tyder på att försvagad aminosyratransport kan vara en gemensam nämnare i tidigt debuterande motorneurondisordrar och att bevarande eller förstärkning av LAT1-funktionen i sårbara spinala motorneuroner kan vara en lovande framtida strategi för att diagnostisera eller behandla sådana tillstånd.
Sammanfattning för rörelsehälsa
Enkelt uttryckt visar detta arbete att vissa spinala motorneuroner hos nyfödda möss är beroende av en specialiserad aminosyre-”leveransdörr” för att överleva och bilda starka kopplingar med muskler. När den dörren stängs genom att ta bort LAT1 får neuronerna brist på viktiga näringsämnen, blir stressade och dör, vilket leder till svaga, förtvining av muskler och tidig död. Genom att koppla denna väg till mönster som ses i modeller av spinal muskelatrofi framhäver studien aminosyratransport — och LAT1-proteinet i synnerhet — som ett potentiellt nytt grepp för att förstå och så småningom ingripa i svåra tidiga rörelsestörningar.
Citering: Sadamori, K., Hiraiwa, M., Horie, T. et al. The amino acid transporter LAT1 coordinates proper motor function at the perinatal stage. Cell Death Dis 17, 345 (2026). https://doi.org/10.1038/s41419-026-08663-8
Nyckelord: motoriska neuron, aminosyratransport, LAT1, spinal muskelatrofi, neuromuskulär koppling