Clear Sky Science · pl
Transporter aminokwasów LAT1 koordynuje prawidłową funkcję ruchową w okresie okołoporodowym
Dlaczego ma to znaczenie dla ruchu i chorób wieku dziecięcego
Nauka płynnego poruszania się to jedno z najważniejszych zadań, które musi opanować noworodkowy układ nerwowy. Badanie ujawnia, jak pojedyncze białko transportujące aminokwasy do komórek nerwowych pomaga nowo narodzonym myszy budować i utrzymywać okablowanie umożliwiające rdzeniowi kontrolę mięśni. Ponieważ podobne obwody są uszkadzane w ludzkich chorobach neuronów ruchowych, takich jak rdzeniowy zanik mięśni, praca ta wskazuje nowe spojrzenie na to, jak wczesne odżywianie i systemy transportu komórkowego mogą wpływać na długoterminowe zdrowie ruchowe. 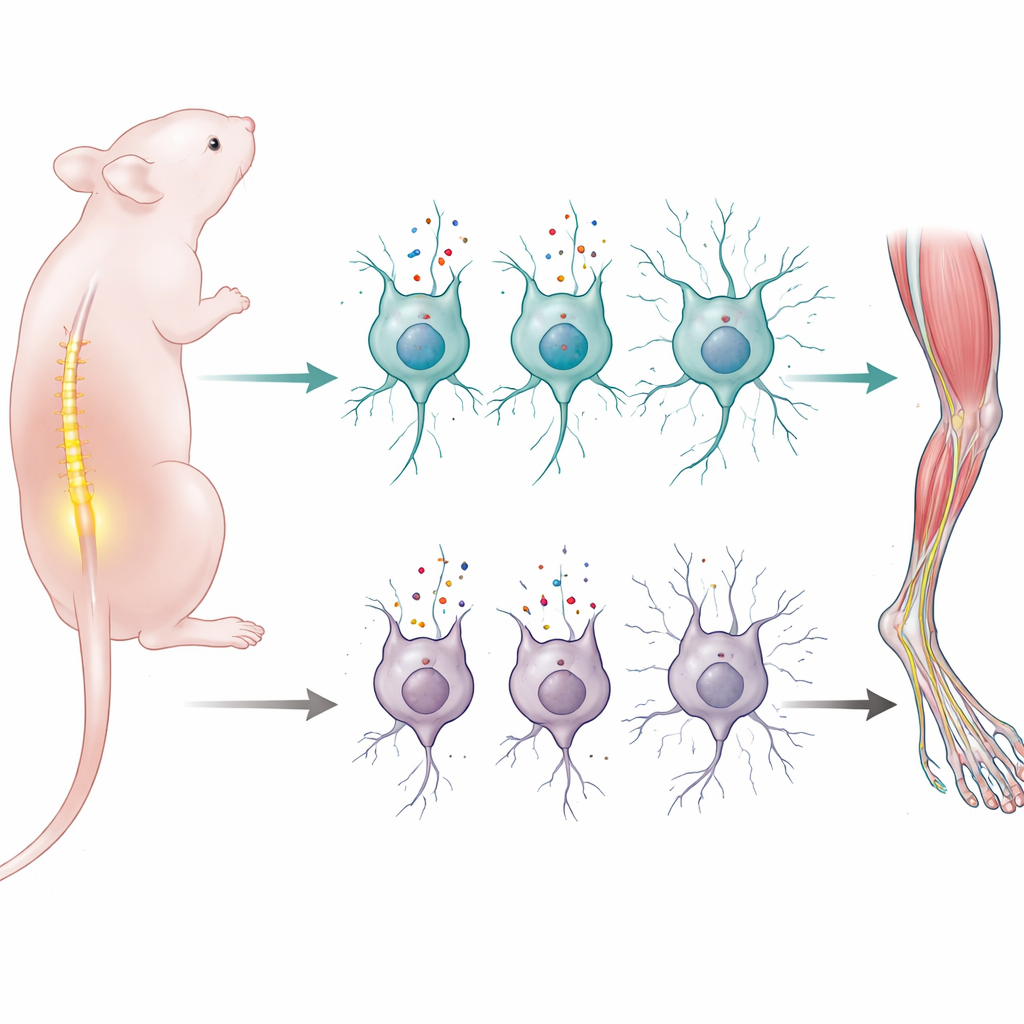
Brama odżywcza w komórkach nerwowych
Naukowcy skupili się na białku zwanym LAT1, które działa jak brama dla dużych obojętnych aminokwasów — budulca i paliwa dla wielu procesów komórkowych — do określonych komórek nerwowych. LAT1 nie jest równomiernie rozłożony w całym organizmie: jest silnie aktywowany w konkretnych tkankach i w określonych momentach, także w okresie okołoporodowym. Wcześniejsze prace wykazały, że całkowite usunięcie genu LAT1 u myszy powoduje poważne zaburzenia rozwoju mózgu i śmierć przed lub krótko po porodzie, lecz nie było jasne, które typy komórek nerwowych bezwzględnie potrzebują tego transportera do funkcjonowania.
Wyłączanie LAT1 w określonych neuronach
Aby precyzyjnie określić rolę LAT1, zespół wyhodował myszy, u których gen LAT1 (Slc7a5) został usunięty tylko w neuronach wyrażających powszechne białko komórek nerwowych zwane synapsyną 1. Te myszy wyglądały normalnie przy urodzeniu i pojawiały się w spodziewanej liczbie, co sugerowało, że wczesne formowanie mózgu mogło przebiegać prawidłowo. Jednak w ciągu pierwszych dwóch tygodni życia młode myszy rozwinęły wyraźne problemy ruchowe: były słabe, niezgrabne w testach równowagi i koordynacji oraz nie przybierały normalnie na wadze. Żadna z nich nie przeżyła ponad trzy tygodnie, co sugeruje krytyczne zapotrzebowanie na LAT1 w okresie okołoporodowym, gdy obwody ruchowe ulegają dopracowaniu.
Uszkodzenie rdzenia kręgowego, przy zachowanym mózgu
Analiza układu nerwowego pod mikroskopem wykazała, że najbardziej dramatyczne uszkodzenia występowały w dolnej części rdzenia kręgowego, gdzie leżą neurony ruchowe bezpośrednio napędzające mięśnie kończyn. W wieku dwóch tygodni około połowa tych neuronów ruchowych zniknęła u mutantów, szczególnie większe komórki typowo kontrolujące silne włókna mięśniowe. Objawy autodestrukcji komórek i nadmiernej „autoczyszczącej” aktywności komórkowej (autofagii) pojawiły się jeszcze wcześniej, co wskazuje na szlak stresowy prowadzący do śmierci komórek. Otaczające komórki wspierające w rdzeniu — astrocyty, mikroglej i komórki produkujące mielinę — również wykazywały silne reakcje, będące znamieniem miejscowego urazu. W przeciwieństwie do tego kora ruchowa i móżdżek w mózgu, które również uczestniczą w kontroli ruchu, wyglądały strukturalnie normalnie, bez wyraźnej utraty neuronów czy bliznowacenia, co podkreśla, że kluczowe uszkodzenia skoncentrowane były w dolnych neuronach ruchowych. 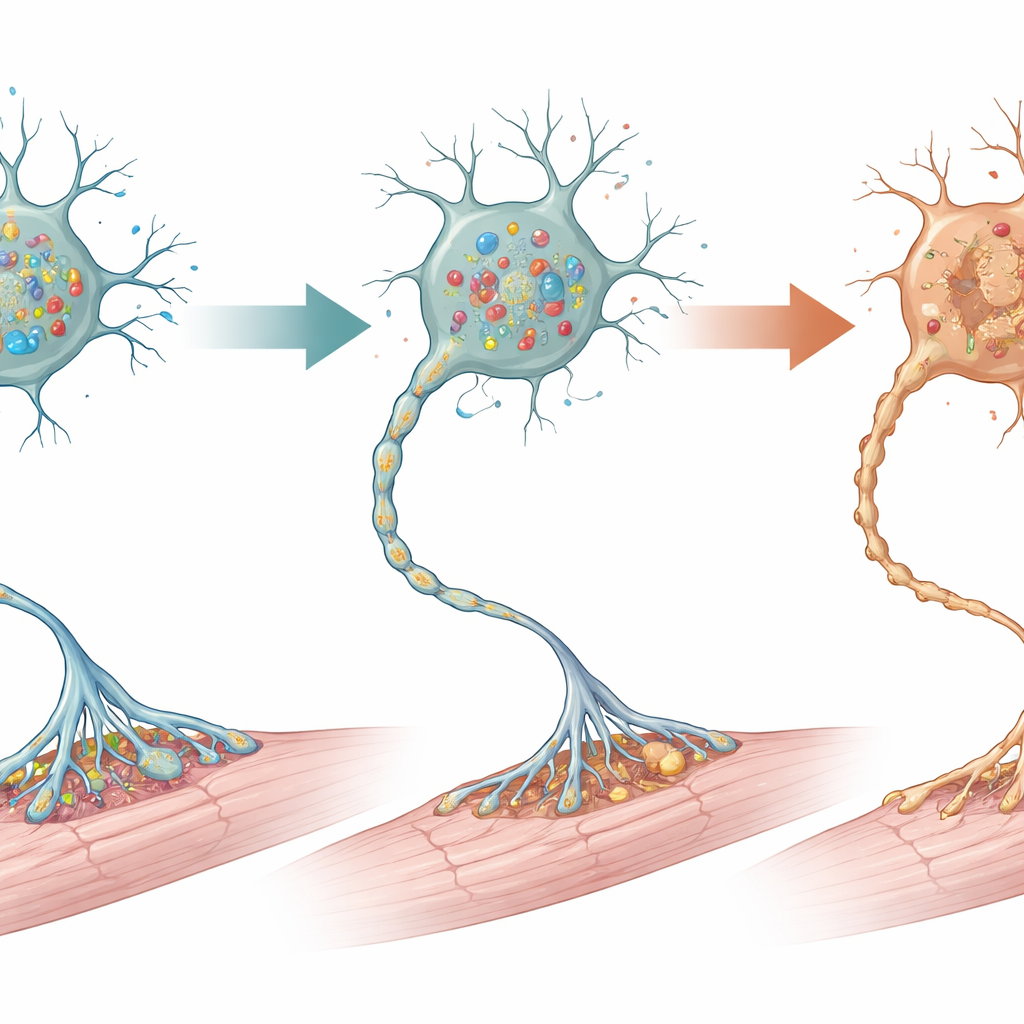
Mięśnie, złącza i częściowe uratowanie
Konsekwencje utraty neuronów ruchowych rdzenia rozciągały się na mięśnie. Na początku włókna mięśniowe wyglądały prawidłowo, ale do drugiego tygodnia uległy skurczeniu, co jest wyraźnym znakiem atrofii. Punkty połączeń nerw–mięsień, zwane złączami nerwowo‑mięśniowymi, straciły swój zwykły skomplikowany kształt, wiele z nich zostało częściowo unerwionych lub całkowicie odłączonych od włókien nerwowych. Aby sprawdzić, czy ścieżki prowadzące do śmierci komórkowej napędzały ten spadek, zespół leczył młode myszy kalpeptyną, lekiem tłumiącym pewną formę zaprogramowanej śmierci komórkowej. Leczone zwierzęta żyły dłużej, zachowały więcej neuronów ruchowych w rdzeniu i miały lepiej uformowane złącza nerwowo‑mięśniowe niż nieleczone mutanty, choć leczenie nie zapobiegło chorobie całkowicie.
Powiązania z dziecięcą chorobą neuronów ruchowych
Ponieważ wzorzec wczesnej utraty dolnych neuronów ruchowych i niewydolnych złączy nerwowo‑mięśniowych przypominał rdzeniowy zanik mięśni, badacze przeanalizowali również kilka dużych zestawów danych genetycznych z modeli mysich tej choroby. W wielu niezależnych badaniach zaobserwowali, że geny zaangażowane w transport i metabolizm aminokwasów, w tym Slc7a5, były osłabione w dotkniętych neuronach ruchowych, natomiast geny powiązane ze śmiercią komórek i aktywacją gleju były zwiększone. To zbieżne wskazanie sugeruje, że osłabiony transport aminokwasów może być wspólnym elementem wczesnodziałających zaburzeń neuronów ruchowych i że zachowanie albo wzmocnienie funkcji LAT1 w podatnych neuronach rdzeniowych może być obiecującą strategią diagnostyczną lub terapeutyczną w przyszłości.
Wnioski dla zdrowia ruchowego
Mówiąc prościej, praca pokazuje, że pewne neurony ruchowe rdzenia u nowo narodzonych myszy zależą od wyspecjalizowanej „drzwi dostarczających” aminokwasy, aby przetrwać i tworzyć solidne połączenia z mięśniem. Gdy te drzwi zostają zamknięte wskutek usunięcia LAT1, neurony cierpią z powodu niedoboru kluczowych substancji odżywczych, stresują się i umierają, prowadząc do słabości, wyniszczenia mięśni i wczesnej śmierci. Powiązanie tego szlaku z wzorcami obserwowanymi w modelach rdzeniowego zaniku mięśni podkreśla transport aminokwasów — a w szczególności białko LAT1 — jako potencjalny nowy punkt uchwytu dla zrozumienia i ewentualnej interwencji w ciężkie zaburzenia ruchowe występujące we wczesnym życiu.
Cytowanie: Sadamori, K., Hiraiwa, M., Horie, T. et al. The amino acid transporter LAT1 coordinates proper motor function at the perinatal stage. Cell Death Dis 17, 345 (2026). https://doi.org/10.1038/s41419-026-08663-8
Słowa kluczowe: neurony ruchowe, transport aminokwasów, LAT1, rdzeniowy zanik mięśni, złącze nerwowo-mięśniowe