Clear Sky Science · sv
Katalytisk asymmetrisk aktivering av bicyklobutaner
Varför små, spända ringar spelar roll
Kemister söker ständigt nya sätt att omforma enkla, oljeliknande molekyler till de komplexa, tredimensionella strukturer som finns i läkemedel och avancerade material. Några av de mest lovande byggstenarna är små, kraftigt spända kolringar som lagrar mycket kemisk "fjär"-energi. Problemet är att när den fjädern väl påverkas brister den ofta upp på många olika sätt samtidigt, vilket gör det svårt att styra den slutgiltiga formen. Denna artikel beskriver ett sätt att tygla en av de mest svårhanterliga av dessa ringar och omvandla den till användbara, entydiga (kirala) produkter med anmärkningsvärd precision.
En kemisk fjäder under kontroll
Studien fokuserar på bicyklobutaner, extremt kompakta fyrkolsringar som liknar två sammanfogade trianglar. Eftersom deras bindningar är böjda långt från sina föredragna vinklar är de redo att spricka upp och frigöra lagrad spänningsenergi. Tidigare arbete hade visat hur besläktade spända strukturer kunde tvingas att bilda nya ringar eller bioaktiva former, men bicyklobutaner bestående endast av kol och väte betraktades som särskilt svårhanterliga: de saknar hjälpsamma "handtag" som syre- eller kväveatomer som vanligtvis styr reaktioner, och de tenderar att sönderfalla eller omorganisera sig på flera konkurrerande sätt.
En skräddarsydd katalysatorficka
För att lösa detta designade författarna en familj av starka organiska syror som fungerar lite som konstgjorda enzymfickor. Dessa katalysatorer, kallade iminoimidodifosforsyror (iIDP), är både mycket sura och tredimensionellt trångbodda. När en bicyklobutan och en alkohol går in i denna ficka tillsammans protonerar (försyrar) katalysatorn tillfälligt den lilla ringen, vilket knuffar den mot öppning, medan det trånga utrymmet runt styr hur den öppningen sker. Under optimerade förhållanden — med en noggrant avstämd iIDP, låga temperaturer och ett enkelt kolväte som lösningsmedel — omvandlar teamet bicyklobutaner till tertiära cyklopropylkarbinyletrar: molekyler som fortfarande innehåller en kompakt treledsring, nu försedd med en fäst alkoholfragment.
Från spända ringar till läkemedelsfärdiga byggstenar
En av de viktigaste bedrifterna är kontroll över handedhet. Många bioaktiva molekyler finns i vänster- och högerhänta former, och ofta fungerar bara en av dem som avsett. Den nya reaktionen ger konsekvent ena handen med hög preferens och når enantiomerselektioner ända upp till 98:2. Metoden fungerar för ett brett spektrum av bicyklobutan-startmaterial och alkoholpartnrar, inklusive enkla alkoholer som metanol och butanol, mer komplexa fragment relaterade till naturliga doftämnen (citronellol) och andra. Eterprodukterna kan sedan smidigt omvandlas till kirala tertiära alkoholer — högt eftertraktade komponenter inom läkemedels- och materialkemi — utan att tappa sin noggrant inställda handedhet.
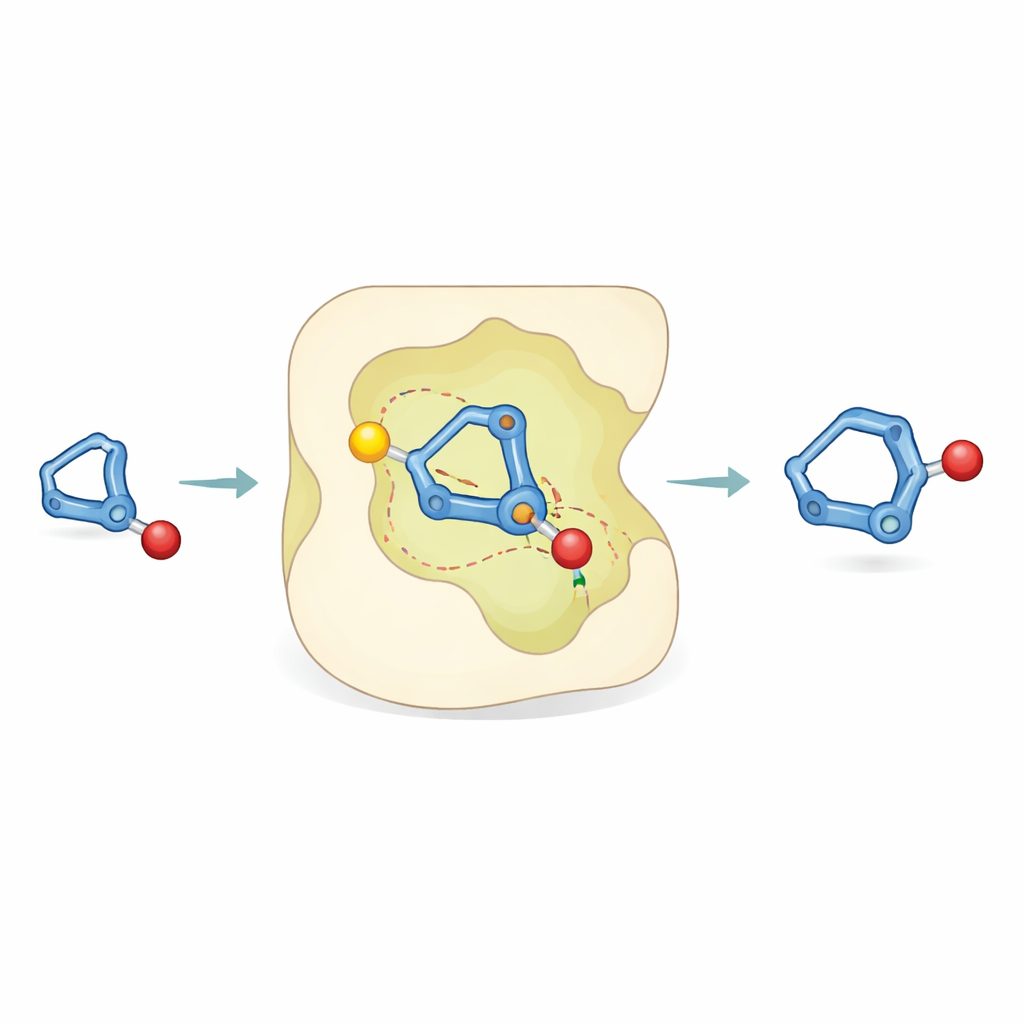
En inblick i reaktionen
För att förstå hur sådan noggrannhet är möjlig kombinerade forskarna experiment med datorsimuleringar. Labbstudier med märkta väteatomer visade att protoneringen av bicyklobutanen sker på ett föredraget sätt, och att oönskat sönderfall sker parallellt snarare än som en väg in i den önskade produkten. Beräkningskemi visade sedan att nyckelsteget är en "asynkron samkörd" process: protonering av den spända ringen och bindningsbildning till alkoholen sker nästan samtidigt. Inom katalysatorfickan bildar det växande positivt laddade intermediäret specifika, riktade kontakter — vätebindningsliknande attraktioner — mellan sina kol–väte‑bindningar och en Lewis-basisk (elektronrik) region av katalysatorn. Dessa icke-kovalenta interaktioner stabiliserar en övergångsform mer än dess spegelbild, vilket förklarar varför ena handen av produkten dominerar.
Vad detta betyder för framtida molekyler
Enkelt uttryckt har forskarna byggt en konstgjord kemisk handske som kan gripa en särskilt spänd kolring, låta den slappna av på ett kontrollerat sätt och koppla en alkohol i en enda, föredragen orientering. Detta visar att även de mest reaktiva, fjäderladdade kolvätena kan styras med enzymlik precision med noggrant formade organiska katalysatorer, utan att förlita sig på metaller eller förinstallerade styrgrupper. Strategin öppnar en väg till en mängd kompakta, tredimensionella, kirala byggstenar som kan användas i läkemedelsupptäckt, polymerer och andra avancerade material — allt genom att lära sig dirigera hur molekylära fjädrar frigör sin energi.
Citering: Shi, F., Frank, N., Leutzsch, M. et al. Catalytic asymmetric activation of bicyclobutanes. Nat. Synth 5, 527–533 (2026). https://doi.org/10.1038/s44160-025-00951-z
Nyckelord: strain-release- kemi, aktivering av bicyklobutan, asymmetrisk katalys, kirala tertiära alkoholer, design av organokatalysator