Clear Sky Science · it
Attivazione asimmetrica catalitica dei bicicclobutani
Perché contano gli anelli piccoli e tesi
I chimici cercano continuamente nuovi modi per trasformare molecole semplici, simili al petrolio, in strutture complesse e tridimensionali presenti nei farmaci e nei materiali avanzati. Alcuni dei blocchi costruttivi più promettenti sono piccoli anelli di carbonio altamente tensionati che immagazzinano una grande quantità di energia chimica, come una molla. Il problema è che, una volta azionata quella molla, tende ad aprirsi in molte direzioni diverse contemporaneamente, rendendo difficile controllare la forma finale. Questo articolo descrive un modo per domare uno dei più indisciplinati di questi anelli e trasformarlo in prodotti chirali utili con straordinaria precisione.
Una molla chimica sotto controllo
Lo studio si concentra sui bicicclobutani, anelli estremamente compatti a quattro atomi di carbonio che ricordano due triangoli fusi. Poiché i loro legami sono piegati lontano dagli angoli preferiti, sono pronti ad aprirsi, liberando l’energia di tensione immagazzinata. Lavori precedenti avevano mostrato come strutture affini tensionate potessero essere indotte a formare nuovi anelli o forme bioattive, ma i bicicclobutani composti solo da carbonio e idrogeno erano considerati particolarmente difficili: mancano di «maniglie» utili come atomi di ossigeno o azoto che solitamente guidano le reazioni, e tendono a frammentarsi o riarrangiarsi in modi multipli e concorrenti.
Una tasca catalitica su misura
Per risolvere questo problema, gli autori hanno progettato una famiglia di acidi organici forti che agiscono un po’ come tasche enzimatiche artificiali. Questi catalizzatori, chiamati acidi iminoimidodifosforici (iIDP), sono sia molto acidi sia molto ingombranti in tre dimensioni. Quando un bicicclobutano e un alcol entrano insieme in questa tasca, il catalizzatore protona brevemente (acidifica) il piccolo anello, spingendolo verso l’apertura, mentre lo spazio ristretto intorno a esso indirizza il modo in cui avviene tale apertura. In condizioni ottimizzate — usando un iIDP finemente sintonizzato, temperature basse e un solvente idrocarburico semplice — il gruppo converte i bicicclobutani in eteri terziari ciclopropilcarbinilici: molecole che conservano un anello compatto a tre termini, ora portando frammento alcolico attaccato.
Dagli anelli tensionati ai mattoni pronti per la medicina
Uno dei risultati chiave è il controllo della mano (enantioselectività). Molte molecole biologicamente attive esistono in forme sinistrorse e destrorse, e spesso funziona solo una delle due. La nuova reazione fornisce costantemente una delle due mani con alta preferenza, raggiungendo valori di enantioselettività fino a 98:2. Il metodo funziona per un’ampia gamma di bicicclobutani di partenza e partner alcolici, inclusi alcoli semplici come metanolo e butanolo, frammenti più complessi correlati a fragranze naturali (citronellolo) e altri. Gli eteri ottenuti possono quindi essere trasformati agevolmente in alcoli terziari chirali — componenti molto ricercati nella chimica farmaceutica e dei materiali — senza perdere la mano accuratamente impostata.
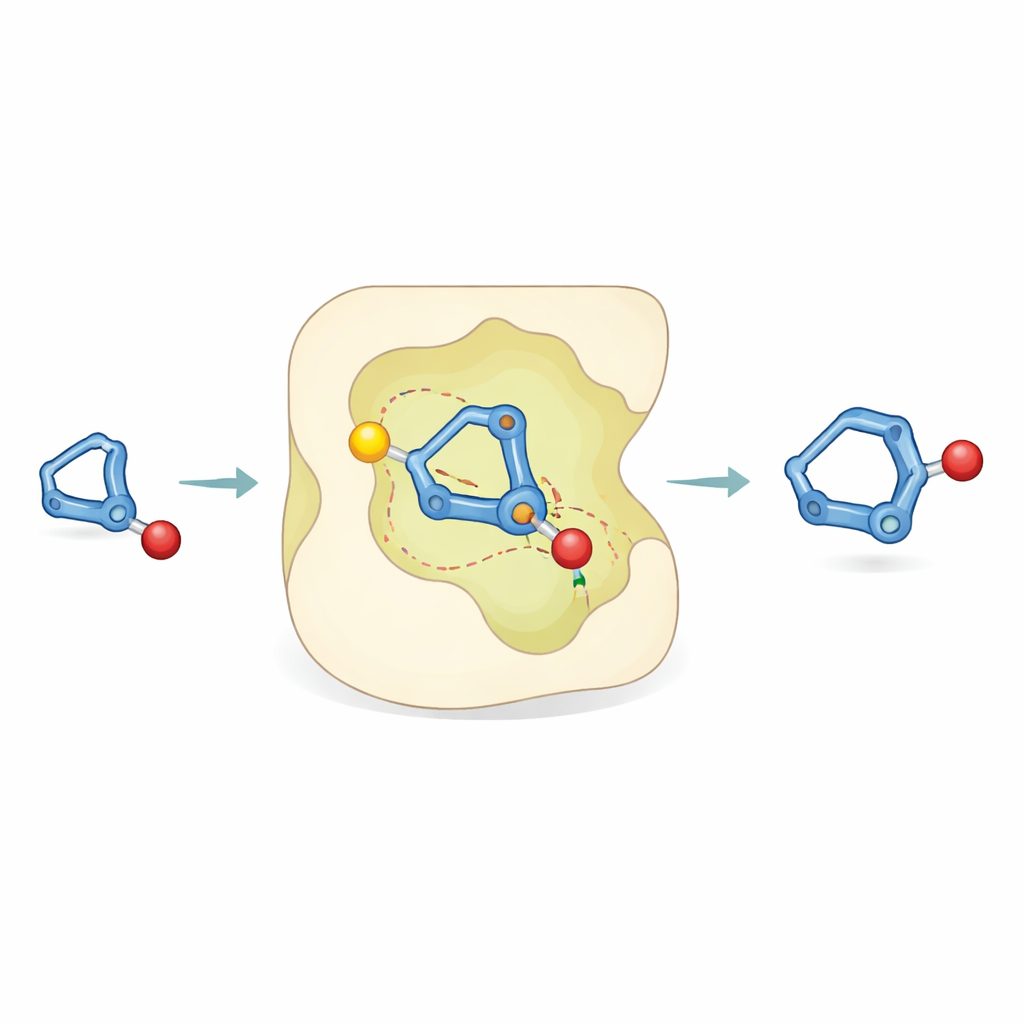
Uno sguardo all’interno della reazione
Per capire come sia possibile tale accuratezza, i ricercatori hanno combinato esperimenti con simulazioni al computer. Studi di laboratorio con atomi di idrogeno etichettati hanno mostrato che la protonazione del bicicclobutano avviene in modo preferenziale, e che le decomposizioni indesiderate procedono in parallelo piuttosto che alimentare il prodotto desiderato. La chimica computazionale ha poi rivelato che il passaggio chiave è un processo «concertato asincrono»: la protonazione dell’anello tensionato e la formazione del legame con l’alcol avvengono quasi contemporaneamente. All’interno della tasca catalitica, l’intermedio a carica positiva che si sviluppa forma contatti specifici e direzionali — attrazioni simili a legami a idrogeno — tra i suoi legami carbonio–idrogeno e una regione di tipo Lewis-basico (ricca di elettroni) del catalizzatore. Queste interazioni non covalenti stabilizzano una geometria di transizione più della sua immagine speculare, spiegando perché una mano del prodotto prevale.
Cosa significa per le molecole future
In termini semplici, i ricercatori hanno costruito un guanto chimico artificiale in grado di afferrare un anello di carbonio particolarmente teso, lasciarlo rilassare in modo controllato e attaccare un alcol in un’unica orientazione preferita. Ciò dimostra che anche gli idrocarburi più reattivi e caricati a molla possono essere guidati con precisione simile a quella degli enzimi usando catalizzatori organici sagomati con cura, senza fare affidamento su metalli o gruppi guida preinstallati. La strategia apre la strada a una grande varietà di blocchi costruttivi compatti, tridimensionali e chirali che potrebbero alimentare la scoperta di farmaci, polimeri e altri materiali avanzati, imparando a dirigere come le molle molecolari rilasciano la loro energia.
Citazione: Shi, F., Frank, N., Leutzsch, M. et al. Catalytic asymmetric activation of bicyclobutanes. Nat. Synth 5, 527–533 (2026). https://doi.org/10.1038/s44160-025-00951-z
Parole chiave: chimica dello scarico di tensione, attivazione dei bicicclobutani, catalsi asimmetrica, alcoli terziari chirali, progettazione di organocatalizzatori