Clear Sky Science · nl
Katalytische asymmetrische activatie van bicyclobutanen
Waarom kleine, gespannen ringen ertoe doen
Chemici zoeken voortdurend naar nieuwe manieren om eenvoudige, olieachtige moleculen om te vormen tot de complexe, driedimensionale structuren die in geneesmiddelen en geavanceerde materialen voorkomen. Een van de veelbelovende bouwstenen zijn kleine, sterk gespannen koolstofringen die veel chemische "veer"energie opslaan. Het probleem is dat zodra je aan die veer trekt, ze meestal op meerdere manieren tegelijk openspringt, waardoor het moeilijk is de uiteindelijke structuur te beheersen. Dit artikel beschrijft een manier om een van de meest ongehoorzame van deze ringen te temmen en om te zetten in nuttige, eénduidige (chirale) producten met opmerkelijke precisie.
Een chemische veer onder controle
De studie richt zich op bicyclobutanen, extreem compacte vierkoolstofringen die lijken op twee samengesmolten driehoeken. Omdat hun bindingen ver van hun voorkeurshoeken afgebogen zijn, staan ze op springen en kunnen ze hun opgebouwde spanningsenergie vrijgeven. Eerder werk toonde aan hoe verwante gespannen structuren gemotiveerd konden worden tot het vormen van nieuwe ringen of bioactieve vormen, maar bicyclobutanen die alleen uit koolstof en waterstof bestaan werden als bijzonder lastig beschouwd: ze missen handige "grepen" zoals zuurstof- of stikstofatomen die reacties meestal sturen, en ze hebben de neiging uiteen te vallen of te herschikken op meerdere, concurrerende manieren.
Een op maat gemaakte katalysatorbinding
Om dit op te lossen ontwierpen de auteurs een familie van sterke organische zuren die zich een beetje gedragen als kunstmatige enzymenpoeken. Deze katalysatoren, iminoimidodifosforzuren (iIDP's), zijn zowel zeer zuur als ruimtelijk sterk afgeschermd. Wanneer een bicyclobutaan en een alcohol samen deze poek binnengaan, protonereert (verzuurt) de katalysator de kleine ring kortstondig en duwt hem richting opening, terwijl de nauwe ruimte de manier van openen stuurt. Onder geoptimaliseerde omstandigheden—met een zorgvuldig afgestemde iIDP, lage temperaturen en een eenvoudig koolwaterstofoplosmiddel—zet het team bicyclobutanen om in tertiaire cyclopropylcarbinylethers: moleculen die nog steeds een compacte drieledige ring bevatten, maar nu met een eraan gebonden alcoholfragment.
Van gespannen ringen naar geneesmiddelklare bouwstenen
Een van de belangrijkste successen is controle over handigheid. Veel biologisch actieve moleculen bestaan in links- en rechtsdraaiende vormen, en vaak werkt slechts één daarvan naar wens. De nieuwe reactie levert consequent één hand met een sterke voorkeur, met enantioselectiviteitswaarden tot 98:2. De methode werkt voor een breed scala aan bicyclobutaan uitgangsmaterialen en alcoholpartners, inclusief eenvoudige alcoholen zoals methanol en butanol, complexere fragmenten gerelateerd aan natuurlijke geurstoffen (citronellol) en anderen. De etherproducten kunnen vervolgens vlot worden omgezet in chirale tertiaire alcoholen—zeer gezochte componenten in de farmaceutische en materiaalkunde—zonder hun zorgvuldig ingestelde handigheid te verliezen.
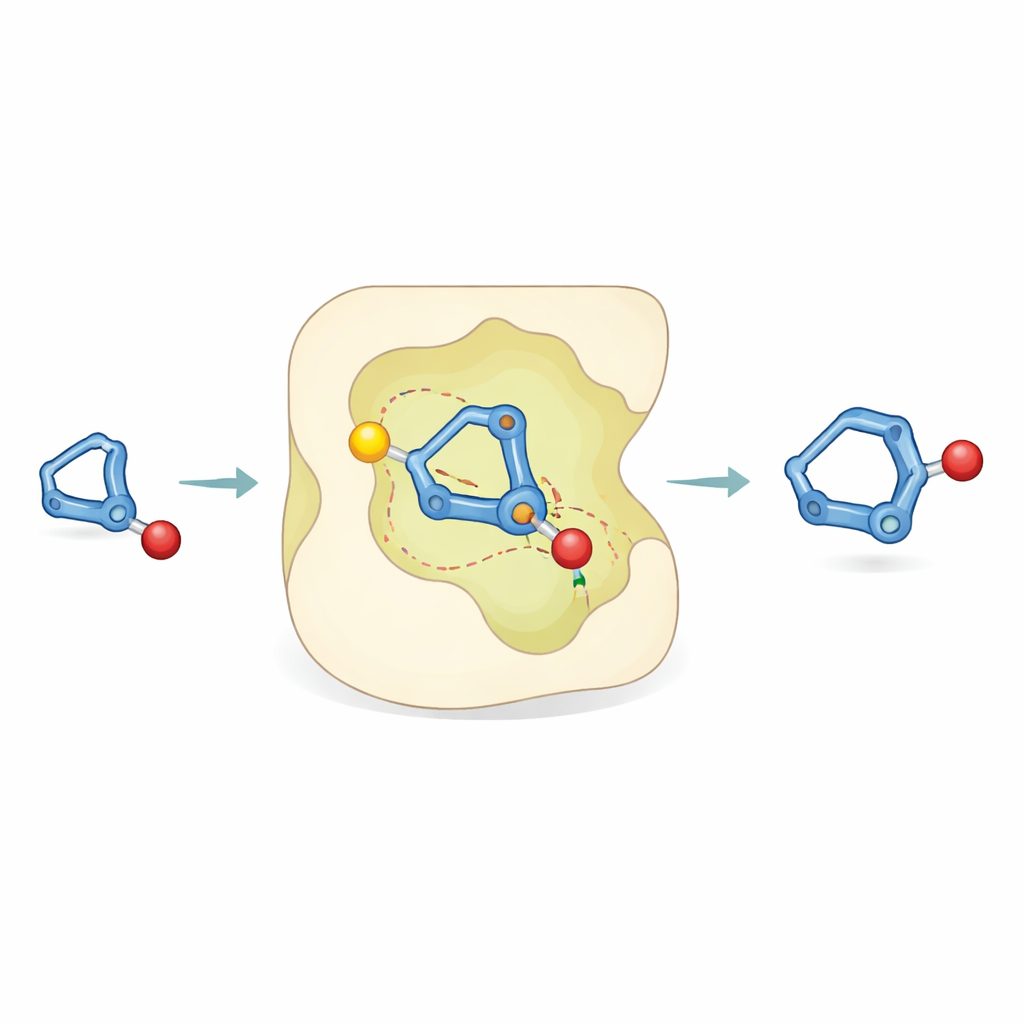
Een blik in de reactie
Om te begrijpen hoe zo veel nauwkeurigheid mogelijk is, combineerden de onderzoekers experimenten met computersimulaties. Laboratoriumstudies met gelabelde waterstofatomen toonden aan dat de protonering van het bicyclobutaan op een geprefereerde manier plaatsvindt, en dat ongewenste afbraak parallel optreedt in plaats van te voeden naar het gewenste product. Computationele chemie liet vervolgens zien dat de sleutelstap een "asynchroon concert"-proces is: protonering van de gespannen ring en het vormen van een binding met de alcohol gebeuren bijna gelijktijdig. Binnen de katalysatorpoek vormt het zich ontwikkelende positief geladen intermediair specifieke, richtinggevende contacten—waterstofbindingachtige aantrekking—tussen zijn koolstof–waterstofbindingen en een Lewis-basische (elektronenrijke) regio van de katalysator. Deze niet-covalente interacties stabiliseren één overgangstoestand meer dan zijn spiegelbeeld, wat verklaart waarom één hand van het product domineert.
Wat dit betekent voor toekomstige moleculen
In eenvoudige termen hebben de onderzoekers een kunstmatige chemische handschoen gebouwd die een bijzonder gespannen koolstofring kan grijpen, hem gecontroleerd laat ontspannen en een alcohol in één voorkeursoriëntatie vasthecht. Dit toont aan dat zelfs de meest reactieve, veerbelaste koolwaterstoffen met enzymachtige precisie gestuurd kunnen worden met zorgvuldig gevormde organische katalysatoren, zonder te vertrouwen op metalen of vooraf aangebrachte gidsgroepen. De strategie opent een pad naar een breed scala aan compacte, driedimensionale, chirale bouwstenen die gebruikt kunnen worden in medicijnontwikkeling, polymeren en andere geavanceerde materialen, simpelweg door te leren hoe moleculaire veren hun energie vrijlaten.
Bronvermelding: Shi, F., Frank, N., Leutzsch, M. et al. Catalytic asymmetric activation of bicyclobutanes. Nat. Synth 5, 527–533 (2026). https://doi.org/10.1038/s44160-025-00951-z
Trefwoorden: strain-release chemie, activatie van bicyclobutaan, asymmetrische katalyse, chirale tertiaire alcoholen, ontwerp van organokatalysatoren