Clear Sky Science · fr
Activation asymétrique catalytique des bicyclobutanes
Pourquoi les petits cycles tendus comptent
Les chimistes cherchent sans cesse de nouvelles façons de transformer des molécules simples, proches des hydrocarbures, en structures tridimensionnelles complexes présentes dans les médicaments et les matériaux avancés. Parmi les blocs de construction les plus prometteurs figurent de minuscules cycles carbonés très contraints qui emmagasinent une grande quantité d’énergie « de ressort » chimique. Le problème est que dès qu’on actionne ce ressort, il a tendance à s’ouvrir de multiples façons simultanément, rendant difficile le contrôle de la forme finale. Cet article décrit une méthode pour maîtriser l’un des plus indisciplinés de ces cycles et le convertir, avec une remarquable précision, en produits utiles et chiraux (à main unique).
Un ressort chimique sous contrôle
L’étude se concentre sur les bicyclobutanes, des cycles extrêmement compacts à quatre carbones qui ressemblent à deux triangles fusionnés. Comme leurs liaisons sont fortement déformées par rapport aux angles préférentiels, ils sont prêts à éclater pour libérer l’énergie de contrainte stockée. Des travaux antérieurs avaient montré comment des structures contraintes apparentées pouvaient être amenées à former de nouveaux cycles ou des formes bioactives, mais les bicyclobutanes composés uniquement de carbone et d’hydrogène étaient considérés comme particulièrement difficiles : ils manquent de « poignées » utiles comme l’oxygène ou l’azote qui guident habituellement les réactions, et ils ont tendance à se rompre ou à se réarranger selon des voies multiples et concurrentes.
Une poche catalytique sur mesure
Pour résoudre ce problème, les auteurs ont conçu une famille d’acides organiques puissants qui jouent un peu le rôle de poches enzymatiques artificielles. Ces catalyseurs, appelés acides iminoimidodiphosphoriques (iIDP), sont à la fois très acides et très encombrés en trois dimensions. Lorsqu’un bicyclobutane et un alcool pénètrent ensemble dans cette poche, le catalyseur protonne provisoirement (acidifie) le petit cycle, l’incitant à s’ouvrir, tandis que l’espace étroit autour oriente la manière dont cette ouverture se produit. Dans des conditions optimisées — en utilisant un iIDP finement ajusté, des températures froides et un solvant hydrocarboné simple — l’équipe convertit les bicyclobutanes en éthers cyclopropylcarbinyles tertiaires : des molécules qui conservent un cycle compact à trois atomes, portant désormais un fragment alcool fixé.
Des cycles contraints aux blocs prêts pour la pharmacie
Parmi les réalisations clés figure le contrôle de la main (énantiomérie). De nombreuses molécules d’intérêt biologique existent sous formes gauches et droites, et souvent une seule est active. La nouvelle réaction fournit systématiquement une main avec une forte préférence, atteignant des valeurs d’énantiosélectivité allant jusqu’à 98:2. La méthode fonctionne pour une large gamme de bicyclobutanes et de partenaires alcooliques, y compris des alcools simples comme le méthanol et le butanol, des fragments plus complexes liés à des parfums naturels (citronellol), et d’autres. Les produits éther peuvent ensuite être transformés de manière fluide en alcools tertiaires chiraux — des composants très recherchés en chimie pharmaceutique et des matériaux — sans perdre la chiralité soigneusement installée.
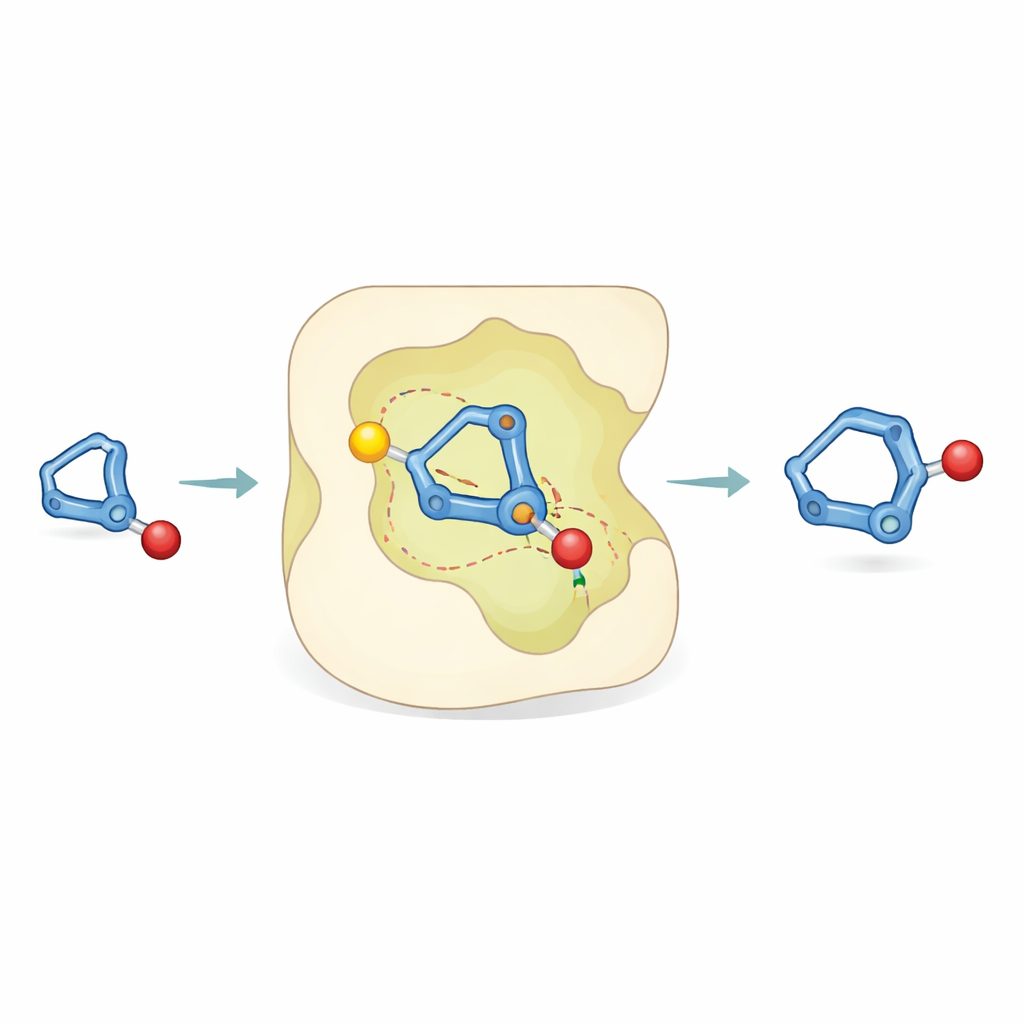
Plongée dans la réaction
Pour comprendre comment une telle précision est possible, les chercheurs ont combiné expériences et simulations informatiques. Des études en laboratoire utilisant des atomes d’hydrogène marqués ont montré que la protonation du bicyclobutane se produit de manière préférentielle, et que les dégradations indésirables surviennent en parallèle plutôt que d’alimenter le produit souhaité. La chimie computationnelle a ensuite révélé que l’étape clé est un processus « concerté asynchrone » : la protonation du cycle contraint et la formation de la liaison avec l’alcool se produisent presque simultanément. Dans la poche catalytique, l’intermédiaire chargé positivement en formation établit des contacts directionnels spécifiques — des attractions de type liaison hydrogène — entre ses liaisons carbone–hydrogène et une région basique de Lewis (riche en électrons) du catalyseur. Ces interactions non covalentes stabilisent une géométrie de transition plus qu’une autre, expliquant pourquoi un énantiomère domine.
Ce que cela signifie pour les molécules de demain
En termes simples, les chercheurs ont construit un gant chimique artificiel capable d’agripper un cycle carboné particulièrement tendu, de le laisser se détendre de manière contrôlée et d’y fixer un alcool selon une orientation unique et préférée. Cela montre que même les hydrocarbures les plus réactifs et chargés comme des ressorts peuvent être dirigés avec une précision voisine de celle des enzymes en utilisant des catalyseurs organiques finement profilés, sans recourir aux métaux ni à des groupes guides préinstallés. La stratégie ouvre la voie à une grande variété de blocs compacts, tridimensionnels et chiraux qui pourraient alimenter la découverte de médicaments, les polymères et d’autres matériaux avancés, simplement en apprenant à orienter la libération d’énergie des ressorts moléculaires.
Citation: Shi, F., Frank, N., Leutzsch, M. et al. Catalytic asymmetric activation of bicyclobutanes. Nat. Synth 5, 527–533 (2026). https://doi.org/10.1038/s44160-025-00951-z
Mots-clés: chimie du relâchement de tension, activation des bicyclobutanes, catalyse asymétrique, alcools tertiaires chiraux, conception d'organocatalyseur