Clear Sky Science · es
Activación asimétrica catalítica de biciclobutanos
Por qué importan los anillos diminutos y tensos
Los químicos buscan constantemente nuevas formas de transformar moléculas simples derivadas del petróleo en estructuras tridimensionales complejas propias de fármacos y materiales avanzados. Algunos de los bloques de construcción más prometedores son anillos de carbono muy pequeños y altamente tensionados que almacenan una gran cantidad de energía «elástica» química. El problema es que, una vez que se activa esa energía, el anillo tiende a abrirse de muchas maneras simultáneas, lo que dificulta controlar la forma final. Este artículo describe una manera de domesticar uno de los anillos más indómitos y convertirlo en productos útiles y de una sola mano (quirales) con notable precisión.
Un resorte químico bajo control
El estudio se centra en los biciclobutanos, anillos de cuatro carbonos extremadamente compactos que recuerdan a dos triángulos fusionados. Debido a que sus enlaces están curvados más allá de sus ángulos preferidos, están predispuestos a estallar, liberando la energía de tensión almacenada. Trabajos anteriores habían mostrado cómo estructuras tensionadas relacionadas podían inducirse a formar nuevos anillos o formas bioactivas, pero los biciclobutanos compuestos solo por carbono e hidrógeno se consideraban especialmente difíciles: carecen de «asideros» útiles como oxígeno o nitrógeno que habitualmente guían las reacciones, y tienden a romperse o reorganizarse por múltiples vías competitivas.
Un bolsillo catalítico hecho a medida
Para resolver esto, los autores diseñaron una familia de ácidos orgánicos fuertes que actúan algo así como bolsillos de enzima artificial. Estos catalizadores, denominados ácido iminoimidodifosfórico (iIDP), son a la vez muy ácidos y muy recargados en tres dimensiones. Cuando un biciclobutano y un alcohol entran juntos en este bolsillo, el catalizador protona (acidifica) brevemente el pequeño anillo, empujándolo hacia la apertura, mientras que el espacio ajustado a su alrededor dirige cómo ocurre esa apertura. Bajo condiciones optimizadas —usando un iIDP cuidadosamente ajustado, temperaturas frías y un disolvente hidrocarbonado simple— el equipo convierte biciclobutanos en éteres terciarios ciclopropilcarbinílicos: moléculas que conservan un anillo compacto de tres miembros y ahora llevan un fragmento alcohólico unido.
De anillos tensionados a bloques de construcción listos para la medicina
Uno de los logros clave es el control de la manoquía (enantioselectividad). Muchas moléculas bioactivas existen en formas izquierda y derecha, y a menudo solo una funciona como se desea. La nueva reacción entrega con consistencia una de las manos con alta preferencia, alcanzando valores de enantioselectividad de hasta 98:2. El método funciona para una amplia gama de biciclobutanos como materiales de partida y de socios alcohólicos, incluidos alcoholes simples como metanol y butanol, fragmentos más complejos relacionados con fragancias naturales (citronelol) y otros. Los productos éter pueden luego transformarse de forma fluida en alcoholes terciarios quirales —componentes muy buscados en química farmacéutica y de materiales— sin perder la quiralidad cuidadosamente establecida.
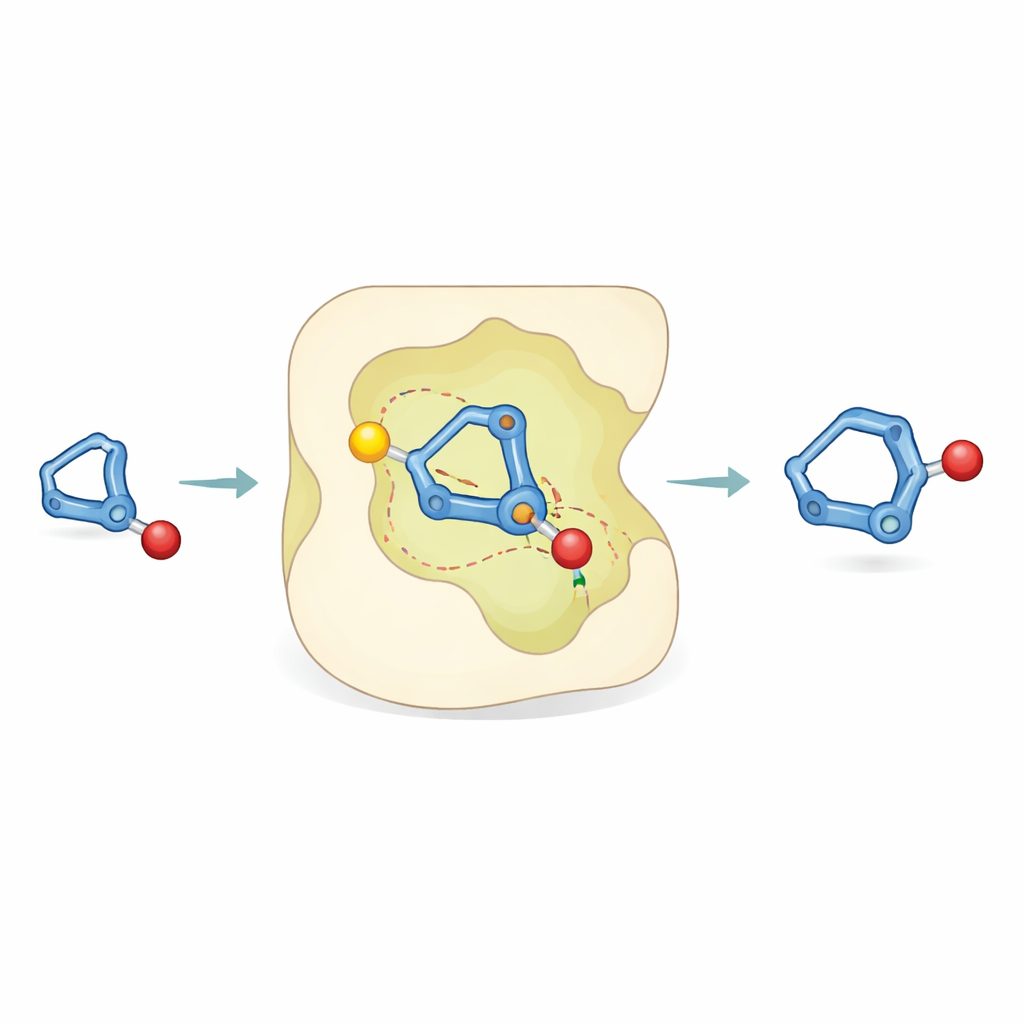
Escrutando el interior de la reacción
Para entender cómo es posible tal precisión, los investigadores combinaron experimentos con simulaciones por computadora. Estudios de laboratorio usando átomos de hidrógeno marcados mostraron que la protonación del biciclobutano ocurre de una manera preferente, y que las descomposiciones no deseadas suceden en paralelo en lugar de alimentar al producto deseado. La química computacional reveló entonces que el paso clave es un proceso «concertado asincrónico»: la protonación del anillo tensionado y la formación del enlace con el alcohol ocurren casi al mismo tiempo. Dentro del bolsillo catalítico, el intermedio con carga positiva en desarrollo establece contactos específicos y direccionales —atracciones semejantes a puentes de hidrógeno— entre sus enlaces carbono–hidrógeno y una región básica de Lewis (rica en electrones) del catalizador. Estas interacciones no covalentes estabilizan una forma de transición más que su imagen especular, lo que explica por qué domina una de las manos del producto.
Qué significa esto para futuras moléculas
En términos simples, los investigadores han construido un guante químico artificial capaz de sujetar un anillo de carbono especialmente tenso, dejarlo relajarse de forma controlada y unir un alcohol en una única orientación preferida. Esto demuestra que incluso los hidrocarburos más reactivos y cargados por tensión pueden ser dirigidos con precisión semejante a la enzimática mediante catalizadores orgánicos cuidadosamente conformados, sin depender de metales ni de grupos directores preinstalados. La estrategia abre la vía a una amplia variedad de bloques de construcción compactos, tridimensionales y quirales que podrían alimentar el descubrimiento de fármacos, polímeros y otros materiales avanzados, todo aprendiendo a dirigir cómo los resortes moleculares liberan su energía.
Cita: Shi, F., Frank, N., Leutzsch, M. et al. Catalytic asymmetric activation of bicyclobutanes. Nat. Synth 5, 527–533 (2026). https://doi.org/10.1038/s44160-025-00951-z
Palabras clave: química de liberación de tensión, activación de biciclobutano, catálisis asimétrica, alcoholes terciarios quirales, diseño de organocatalizadores