Clear Sky Science · de
Katalytische asymmetrische Aktivierung von Bicyclobutanen
Warum winzige, angespannte Ringe wichtig sind
Chemiker suchen ständig nach neuen Wegen, einfache, ölartige Moleküle in die komplexen, dreidimensionalen Strukturen zu verwandeln, die in Arzneimitteln und Hochleistungsmaterialien vorkommen. Zu den vielversprechendsten Bausteinen zählen winzige, stark gespannte Kohlenstoffringe, die viel chemische "Feder"energie speichern. Das Problem ist, dass sich diese Feder beim Anstoßen meist auf viele verschiedene Arten gleichzeitig öffnet, wodurch es schwierig wird, die endgültige Form zu kontrollieren. Dieser Artikel beschreibt einen Weg, einen der widerspenstigsten dieser Ringe zu bändigen und mit bemerkenswerter Präzision in nützliche, einhändige (chirale) Produkte zu überführen.
Eine chemische Feder unter Kontrolle
Die Studie konzentriert sich auf Bicyclobutane, extrem kompakte Vier-Kohlenstoff-Ringe, die zwei verschmolzenen Dreiecken ähneln. Weil ihre Bindungen weit von ihren bevorzugten Winkeln abgewinkelt sind, sind sie bereit, aufzubrechen und gespeicherte Spannungsenergie freizusetzen. Frühere Arbeiten zeigten, wie verwandte gespannte Strukturen dazu gebracht werden konnten, neue Ringe oder bioaktive Formen zu bilden, aber reine Kohlenstoff‑Wasserstoff‑Bicyclobutane galten als besonders schwierig: Ihnen fehlen hilfreiche „Griffe“ wie Sauerstoff‑ oder Stickstoffatome, die Reaktionen normalerweise lenken, und sie neigen dazu, aufzuspalten oder sich auf mehreren konkurrierenden Wegen umzustrukturieren.
Eine maßgeschneiderte Katalysator‑Tasche
Um das zu lösen, entwarfen die Autoren eine Familie starker organischer Säuren, die ein wenig wie künstliche Enzymtaschen wirken. Diese Katalysatoren, genannt iminoimidodiphosphorsäuren (iIDPs), sind sowohl sehr sauer als auch räumlich sehr überfüllt. Wenn ein Bicyclobutan und ein Alkohol gemeinsam in diese Tasche eintreten, protoniert (säuert) der Katalysator den winzigen Ring kurz an und schiebt ihn zum Öffnen, während der enge Raum um ihn herum steuert, wie dieses Öffnen abläuft. Unter optimierten Bedingungen — mit einem sorgfältig abgestimmten iIDP, niedrigen Temperaturen und einem einfachen Kohlenwasserstofflösungsmittel — wandelt das Team Bicyclobutane in tertiäre Cyclopropylcarbinyl‑ether um: Moleküle, die weiterhin einen kompakten Drei‑Glieder‑Ring enthalten, an dem nun ein Alkoholfagment hängt.
Von gespannten Ringen zu arzneimittelbereiten Bausteinen
Einer der wichtigsten Erfolge ist die Kontrolle über die Händigkeit. Viele biologisch aktive Moleküle existieren in links‑ und rechtsdrehenden Formen, und oft wirkt nur eine davon wie beabsichtigt. Die neue Reaktion liefert konstante eine Händigkeit mit hoher Präferenz und erreicht Enantioselektivitäten von bis zu 98:2. Die Methode funktioniert für eine breite Palette von Bicyclobutan‑Ausgangsmaterialien und Alkoholpartnern, einschließlich einfacher Alkohole wie Methanol und Butanol, komplexerer Fragmente, die mit natürlichen Düften verwandt sind (z. B. Citronellol), und anderer. Die Ether‑Produkte lassen sich dann reibungslos in chirale tertiäre Alkohole umwandeln — hochgefragte Bausteine in der pharmazeutischen und Materialchemie — ohne die sorgfältig eingestellte Händigkeit zu verlieren.
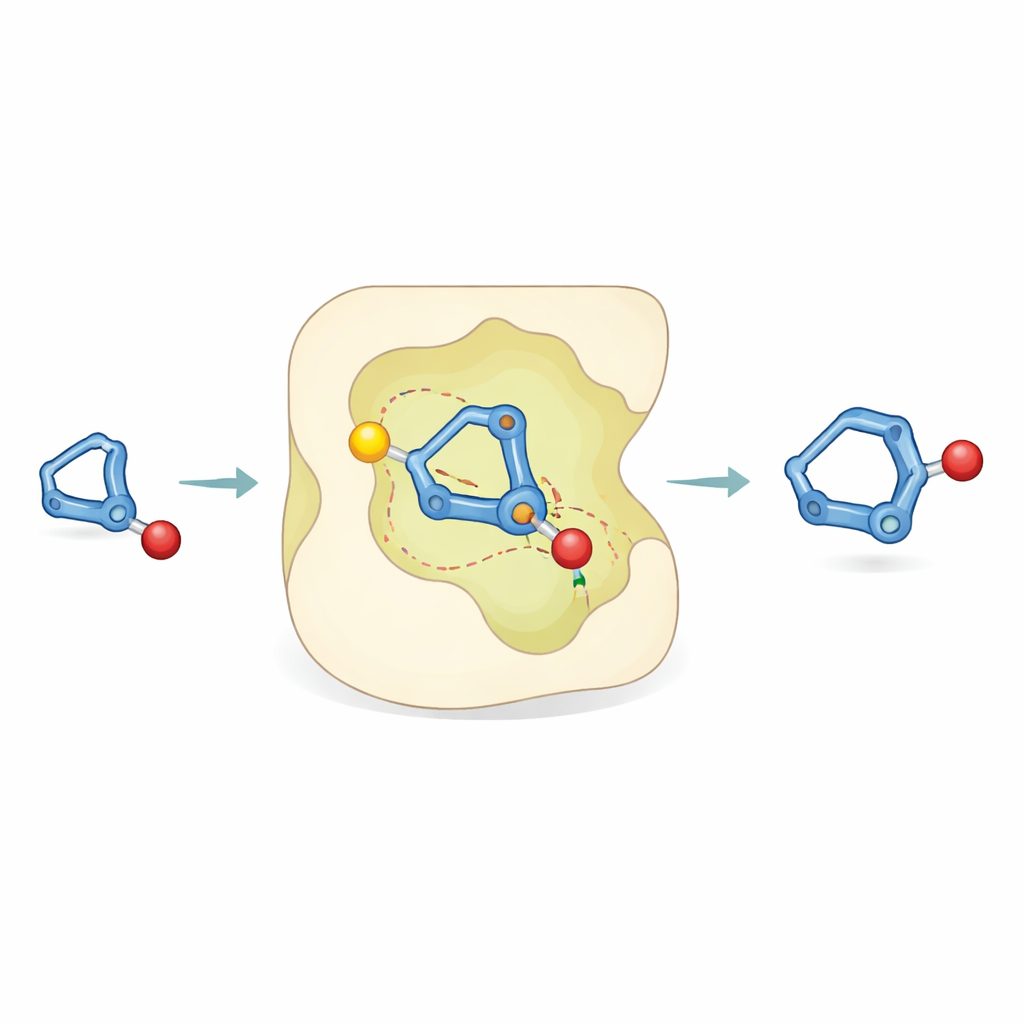
Ein Blick in die Reaktion
Um zu verstehen, wie eine solche Genauigkeit möglich ist, kombinierten die Forschenden Experimente mit Computersimulationen. Laborstudien mit markierten Wasserstoffatomen zeigten, dass die Protonierung des Bicyclobutans in einer bevorzugten Weise erfolgt und dass unerwünschter Zerfall parallel abläuft, anstatt in das gewünschte Produkt zu münden. Die theoretische Chemie zeigte dann, dass der Schlüsselschritt ein „asynchron konzertierter“ Prozess ist: Die Protonierung des gespannten Rings und die Bindungsbildung zum Alkohol erfolgen beinahe gleichzeitig. Innerhalb der Katalysator‑Tasche bildet das entstehende positiv geladene Zwischenprodukt spezifische, gerichtete Kontakte — wasserstoffbrückenähnliche Anziehungen — zwischen seinen C–H‑Bindungen und einer Lewis‑basischen (elektronenreichen) Region des Katalysators. Diese nichtkovalenten Wechselwirkungen stabilisieren eine Übergangsstruktur stärker als ihr Spiegelbild und erklären so, warum eine Händigkeit des Produkts dominiert.
Was das für künftige Moleküle bedeutet
Einfach ausgedrückt haben die Forschenden eine künstliche chemische Hand gebaut, die einen besonders angespannten Kohlenstoffring greifen, ihn kontrolliert entspannen und in einer einzigen, bevorzugten Orientierung einen Alkohol anfügen kann. Das zeigt, dass selbst die reaktivsten, federbelasteten Kohlenwasserstoffe mit enzymähnlicher Präzision durch sorgfältig geformte organische Katalysatoren gelenkt werden können, ohne auf Metalle oder vorinstallierte Führungsgruppen zurückzugreifen. Die Strategie eröffnet einen Weg zu einer Vielzahl kompakter, dreidimensionaler, chiraler Bausteine, die in die Wirkstoffforschung, Polymere und andere Hochleistungsmaterialien einfließen könnten — alles durch das Lernen, wie molekulare Federn ihre Energie freisetzen.
Zitation: Shi, F., Frank, N., Leutzsch, M. et al. Catalytic asymmetric activation of bicyclobutanes. Nat. Synth 5, 527–533 (2026). https://doi.org/10.1038/s44160-025-00951-z
Schlüsselwörter: Spannungsfreisetzungs-Chemie, Aktivierung von Bicyclobutanen, asymmetrische Katalyse, chirale tertiäre Alkohole, Design von Organokatalysatoren