Clear Sky Science · sv
Multimodala datadrivna grafkonvolutionella nätverk för att förutsäga utfall vid äggstockscancer som får neoadjuvant cytostatikabehandling
Varför denna forskning är betydelsefull för patienter
För kvinnor med avancerad äggstockscancer kan valet av behandlingsväg vara avgörande. Många får cytostatika före operation för att krympa tumörer och göra ingreppet säkrare, men läkare har fortfarande svårt att förutsäga vilka som kommer att ha störst nytta och vilka som kan behöva en annan strategi. Denna studie presenterar ett nytt, mer träffsäkert sätt att förutse både överlevnad och kirurgiskt resultat med hjälp av information som sjukhus redan samlar in, vilket kan göra mer skräddarsydd vård tillgänglig i vanliga kliniker.
Att se hela patienten, inte bara en siffra
Traditionellt har läkare lutat sig mot några få enskilda mätvärden för att vägleda behandling före operation. Ett välanvänt exempel är ett blodtestmönster kallat KELIM‑poäng, som följer hur snabbt tumörmarkören CA‑125 sjunker under tidig cytostatikabehandling. Andra verktyg utgår från röntgenfynd eller enkla laboratoriekvoter som vita blodkroppars nivåer. Dessa är användbara, men var och en fokuserar på endast en del av patientens berättelse. Den nya metoden utgår från att verkliga patienter är mer komplexa: blodprover, röntgendifferenser, ålder och tumöregenskaper samverkar på subtila sätt som kan påverka hur någon svarar på behandling.
Koppla liknande patienter i ett lärande nätverk
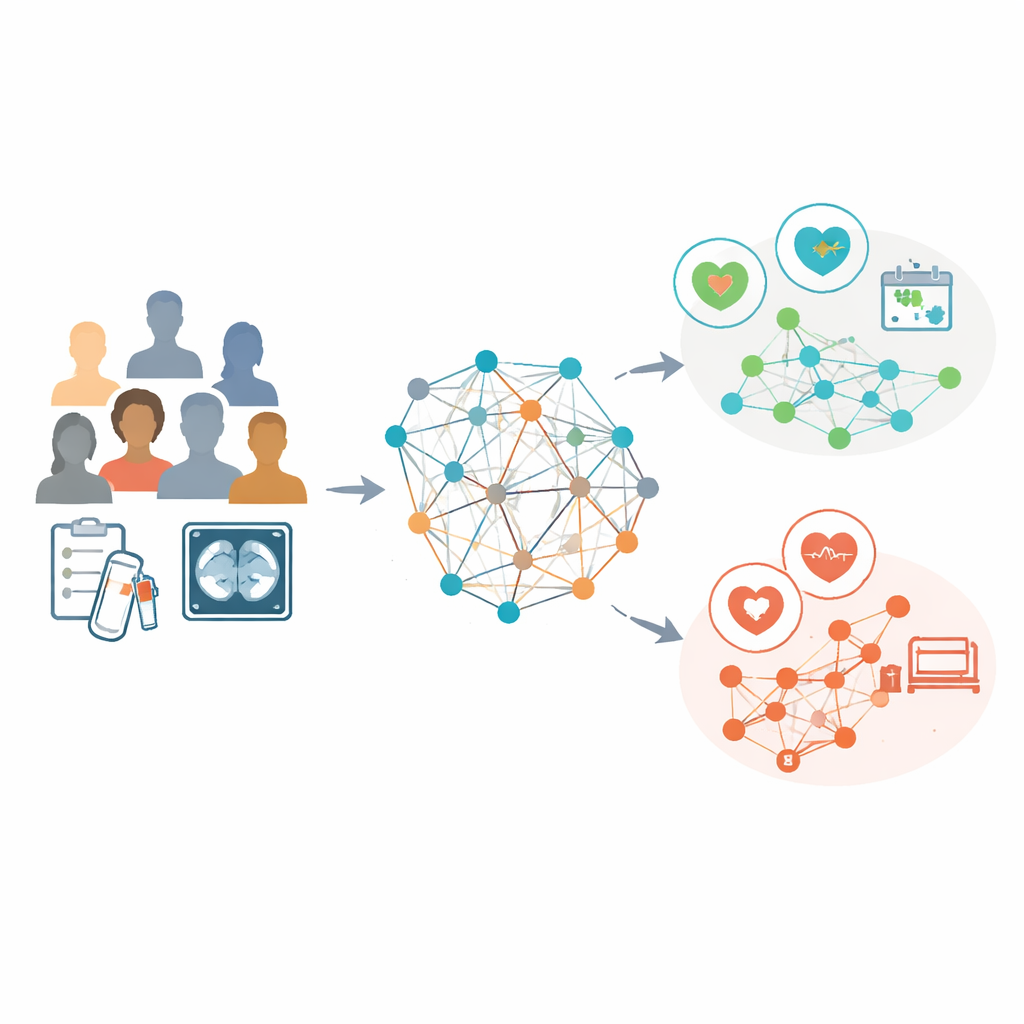
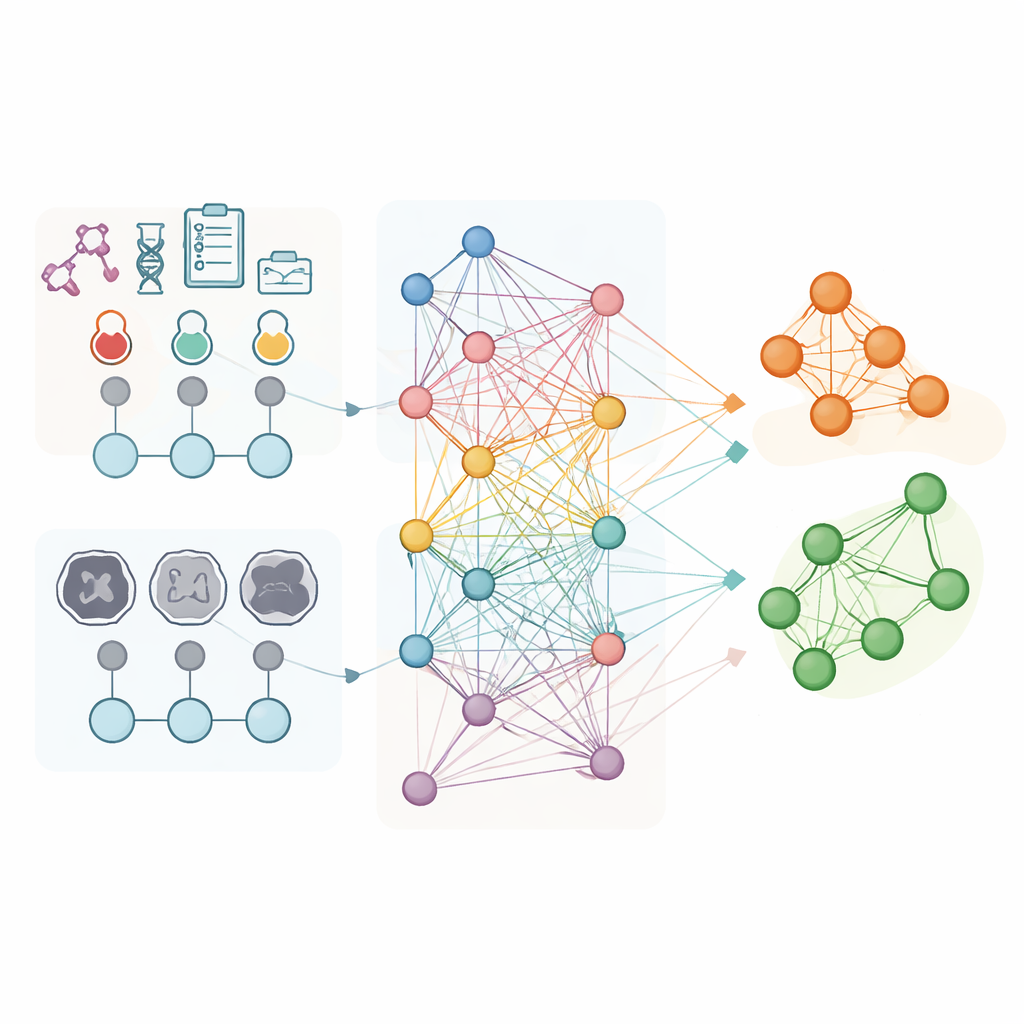
Forskarna analyserade data från 853 kvinnor med avancerad äggstockscancer som alla fick cytostatika före intervaloperation vid tre sjukhus. För varje patient använde de rutinmässiga laboratorieresultat och detaljerade egenskaper utvunna från förbehandlings‑CT‑bilder, såsom form och textur hos synliga tumörer. Istället för att betrakta varje person som ett isolerat fall byggde de en "populationsgraf" där varje patient är en nod och kopplingar länkar patienter med liknande laboratorieprofiler. En specialiserad form av artificiell intelligens, ett grafkonvolutionellt nätverk, lärde sig sedan mönster över detta nät—CT‑baserade egenskaper användes som huvudbeskrivningar för varje nod medan kopplingarna bar information om hur patienterna liknade varandra.
Bättre än befintliga prediktionsverktyg
Teamet bad sin modell utföra två uppgifter som är av stor betydelse för patienter och kirurger: att förutsäga total överlevnad över flera år och att uppskatta sannolikheten för att uppnå en operation utan synlig tumör kvar (kallad R0‑resektion). De jämförde dess prestanda med fyra etablerade tillvägagångssätt byggda på kliniska data, enbart röntgenelement, en kombination av båda, och KELIM‑poängen, samt med ett vanligt använt kirurgiskt poängsystem. Vid huvudsjukhuset och vid två oberoende testsjukhus gav grafmodellen konsekvent mer exakta överlevnadsprognoser. Den klarade sig också bättre än de andra metoderna när det gällde att urskilja vilka patienter som sannolikt skulle avsluta operationen tumörfria och vilka som inte skulle göra det, även när traditionella modeller visade liten separation.
Hitta hopp där äldre poäng ser risk
Ett av de mest slående fynden var att den nya modellen identifierade en betydande grupp kvinnor—ungefär 16 procent av totalen—som hade låga KELIM‑poäng (vilket vanligtvis signalerar dåligt svar) men som faktiskt levde lika länge som de med gynnsamma KELIM‑värden. Med andra ord skulle äldre verktyg ha klassat dem som högrisk, medan grafmetoden korrekt kände igen deras goda prognos. Modellen visade även ett jämnt, stegvis samband mellan sin poäng och utfall: när poängen ökade steg både överlevnadstid och sannolikheten för fullständig tumörborttagning stadigt, från nästan inga R0‑operationer vid de lägsta poängen till nästan alla patienter som uppnådde R0 vid de högsta. Detta jämna mönster syntes inte med enbart KELIM, vilket tyder på att den nya poängen fångar en tydligare biologisk signal.
Utformad för bruk i verklighetens sjukhus
Många avancerade AI‑verktyg kräver kraftfulla grafikkort som sällan finns i vanliga sjukhusdatorer. I kontrast är denna grafbaserade modell byggd för att köras helt på vanliga centralprocessorer, vilket gör den mer praktisk för dagligt kliniskt bruk. Den bygger på laboratorietester och CT‑bilder som redan ingår i rutinvården, och författarna visade att dess prediktiva värde förblev starkt även efter att man justerat för ålder, tumörstadium, typ och KELIM‑poäng. Även om studien var retrospektiv och ännu inte inkluderade genetiska markörer som BRCA‑status, tyder dess multicenter‑validering på att metoden är robust över olika sjukhus och patientgrupper.
Vad detta kan innebära för framtida vård
För patienter är huvudbudskapet enkelt: genom att lära av mönster över många liknande individer kan detta nya verktyg mer exakt identifiera vem som sannolikt får nytta av cytostatika före operation och vem som kan behöva en annan plan. En hög poäng signalerar stor chans till längre överlevnad och framgångsrik tumörborttagning, medan en låg poäng kan få läkare att ompröva operations‑timingen eller undersöka alternativa terapier i stället för att fortsätta med en strategi som sannolikt inte hjälper. Med fortsatt prospektiv testning och integration i journalsystem kan grafbaserade modeller som denna bidra till att flytta äggstockscancerbehandling från en universalstrategi till vård som är mer precist anpassad till varje kvinnas unika profil.
Citering: Zhang, S., Liu, Y., Liu, Z. et al. Multimodal data-based graph convolutional networks for predicting outcomes in ovarian cancer receiving neoadjuvant chemotherapy. npj Precis. Onc. 10, 157 (2026). https://doi.org/10.1038/s41698-026-01346-9
Nyckelord: äggstockscancer, neoadjuvant cytostatikabehandling, grafneurala nätverk, radiomik, behandlingsprediktion