Clear Sky Science · pl
Wielo-modalne sieci konwolucyjne oparte na grafach do przewidywania wyników u pacjentek z rakiem jajnika leczonych chemioterapią neoadjuwantową
Dlaczego te badania są ważne dla pacjentek
Dla kobiet z zaawansowanym rakiem jajnika wybór odpowiedniej ścieżki leczenia może zaważyć o losie życia. Wiele pacjentek otrzymuje chemioterapię przed zabiegiem, aby zmniejszyć guzy i zwiększyć bezpieczeństwo operacji, ale lekarze wciąż mają trudności z przewidzeniem, kto odniesie największą korzyść, a kto powinien otrzymać inną strategię. Niniejsze badanie przedstawia nową, dokładniejszą metodę prognozowania zarówno przeżycia, jak i powodzenia operacji, wykorzystując informacje już gromadzone w szpitalach, co może przybliżyć spersonalizowaną opiekę do codziennej praktyki klinicznej.
Widzieć całą pacjentkę, a nie tylko jedną wartość
Tradycyjnie lekarze opierali decyzje przedoperacyjne na kilku pojedynczych pomiarach. Przykładem jest popularny wskaźnik KELIM, określający, jak szybko spada marker nowotworowy CA‑125 we wczesnej fazie chemioterapii. Inne narzędzia analizują wyniki obrazowania lub proste stosunki z badań laboratoryjnych, takie jak liczba białych krwinek. Choć przydatne, każde z tych podejść pokazuje tylko jeden fragment historii pacjentki. Nowe podejście uznaje, że pacjentki są bardziej złożone: badania krwi, cechy ze skanów, wiek i właściwości guza wzajemnie się przeplatają w subtelny sposób i wspólnie determinują odpowiedź na leczenie.
Łączenie podobnych pacjentek w sieć uczącą się
Badacze przeanalizowali dane 853 kobiet z zaawansowanym rakiem jajnika, które wszystkie otrzymały chemioterapię przed zabiegiem przerywającym leczenie (interval surgery) w trzech szpitalach. Dla każdej pacjentki wykorzystano rutynowe wyniki badań laboratoryjnych oraz szczegółowe cechy wyekstrahowane z przedterapeutycznych tomografii komputerowych, takie jak kształt i tekstura widocznych guzów. Zamiast traktować każdą osobę jako odrębny przypadek, zbudowano „graf populacyjny”, w którym każdy pacjent jest węzłem, a krawędzie łączą pacjentki o podobnych profilach laboratoryjnych. Specjalistyczna forma sztucznej inteligencji, zwana grafową siecią konwolucyjną, nauczyła się wzorców na tej sieci, używając cech opartych na CT jako głównych opisów każdego węzła, podczas gdy połączenia przenosiły informacje o podobieństwach między pacjentkami.
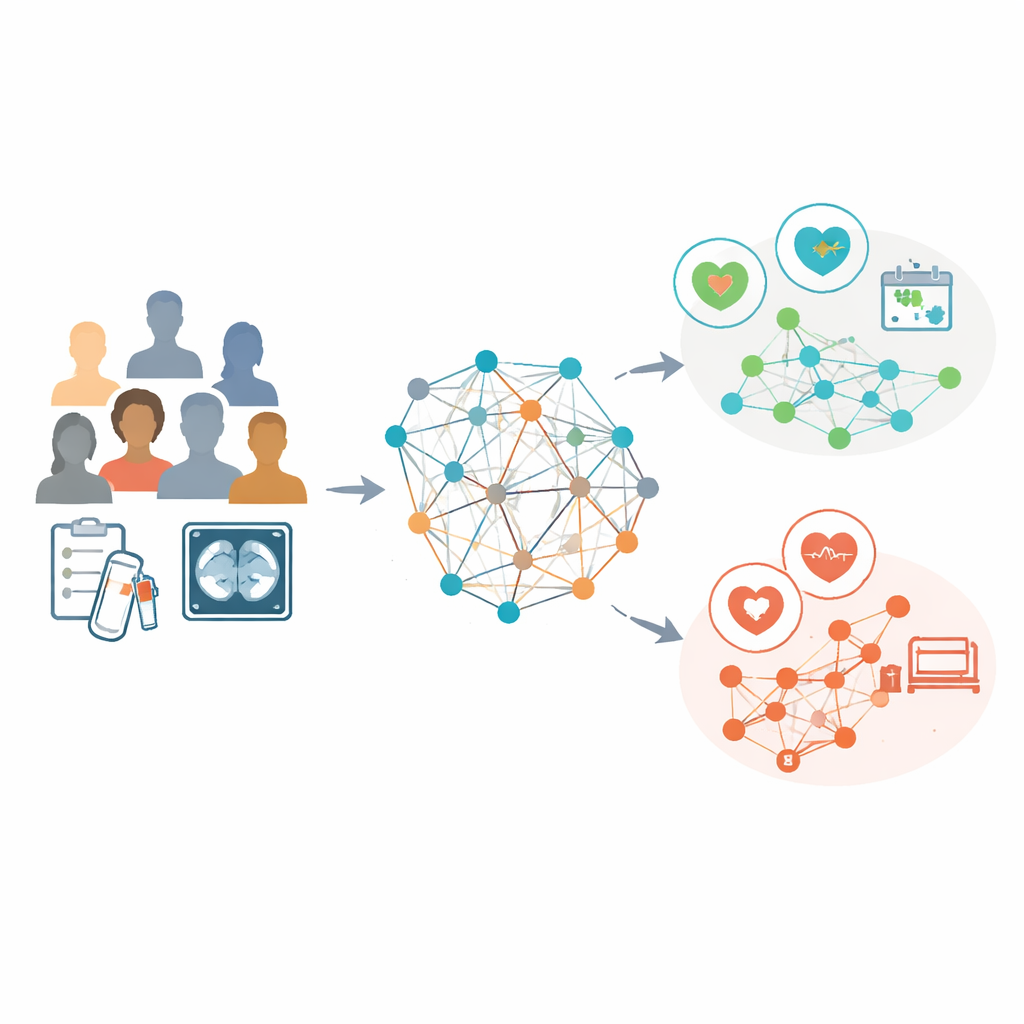
Przewyższając istniejące narzędzia predykcyjne
Zespół poprosił model o wykonanie dwóch zadań istotnych dla pacjentek i chirurgów: przewidzieć całkowite przeżycie w ciągu kilku lat oraz oszacować prawdopodobieństwo osiągnięcia operacji pozostawiającej brak widocznego guza (tzw. resekcja R0). Wyniki porównano z czterema ustalonymi podejściami opartymi na danych klinicznych, samych cechach ze skanów, ich kombinacji oraz wskaźniku KELIM, a także z powszechnie stosowanym systemem punktacji chirurgicznej. W szpitalu macierzystym i w dwóch niezależnych ośrodkach testowych model oparty na grafie konsekwentnie dawał dokładniejsze prognozy przeżycia. Lepsze było też jego rozróżnianie pacjentek, które prawdopodobnie zakończą operację bez widocznego guza, od tych, które tego celu nie osiągną — nawet gdy tradycyjne modele wykazywały niewielkie rozdzielenie.
Odnajdywanie nadziei tam, gdzie starsze wskaźniki widziały ryzyko
Jednym z najbardziej uderzających wyników było odkrycie przez model istotnej grupy kobiet — około 16 procent badanej populacji — które miały niskie wartości KELIM (zwykle sugerujące słabą odpowiedź), a mimo to przeżywały tak długo jak pacjentki z korzystnymi wartościami KELIM. Innymi słowy, starsze narzędzia sklasyfikowałyby je jako obarczone wysokim ryzykiem, podczas gdy metoda oparta na grafie poprawnie rozpoznała ich korzystne rokowanie. Model wykazał również gładką, stopniową zależność między swoją punktacją a wynikami: wraz ze wzrostem wyniku rosły zarówno czas przeżycia, jak i prawdopodobieństwo całkowitego usunięcia guza — od niemal braku resekcji R0 przy najniższych wynikach do niemal wszystkich pacjentek osiągających R0 przy najwyższych. Tego typu stabilny wzorzec nie był widoczny dla samego KELIM, co sugeruje, że nowy wynik lepiej oddaje biologiczny sygnał.
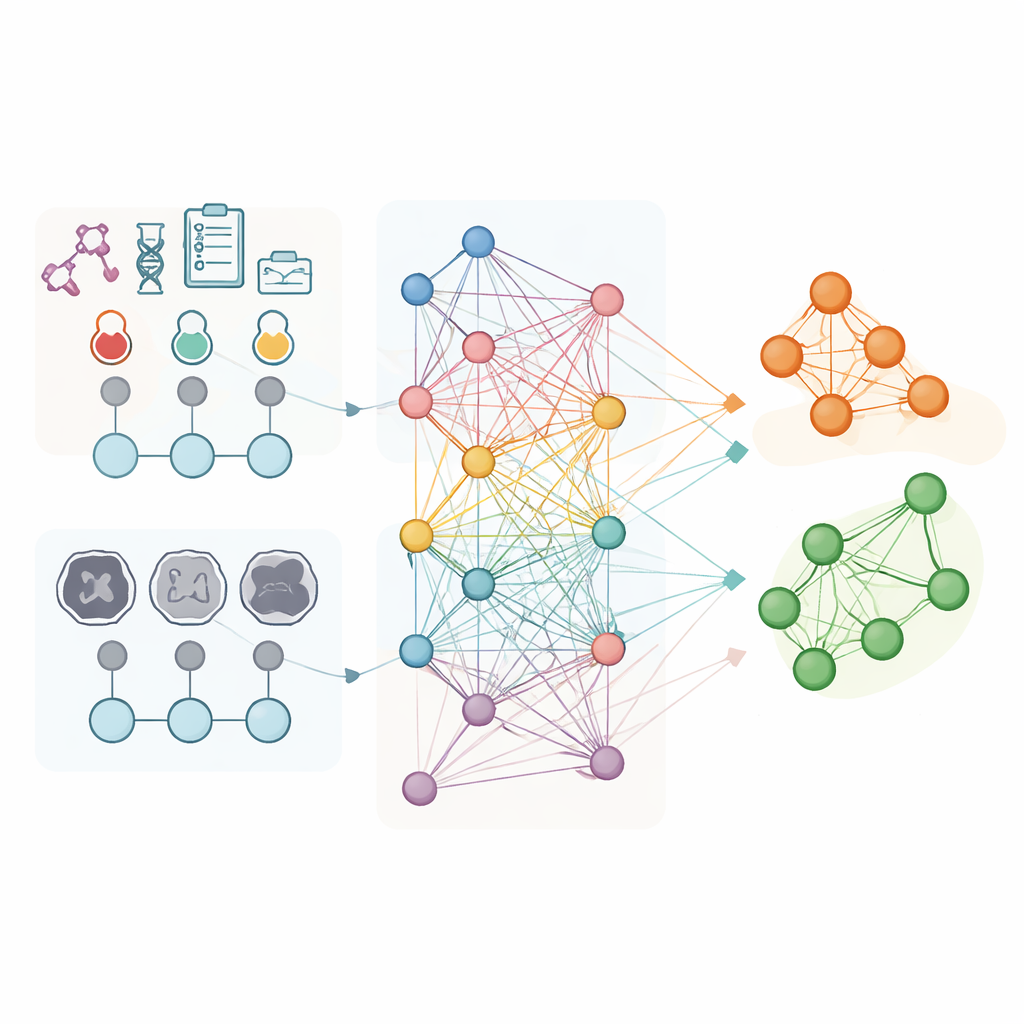
Zaprojektowane z myślą o praktyce szpitalnej
Wiele zaawansowanych narzędzi AI wymaga wydajnych procesorów graficznych, rzadko dostępnych w standardowych komputerach szpitalnych. W przeciwieństwie do tego model oparty na grafie zaprojektowano tak, by działał w całości na zwykłych procesorach centralnych, co czyni go bardziej praktycznym do codziennego użytku klinicznego. Opiera się na badaniach laboratoryjnych i tomografiach komputerowych, które już wchodzą w skład rutynowej opieki, a autorzy pokazali, że jego wartość predykcyjna pozostawała wysoka nawet po uwzględnieniu wieku, stadium choroby, typu guza i wyniku KELIM. Chociaż badanie miało retrospektywny charakter i nie obejmowało jeszcze markerów genetycznych, takich jak status BRCA, walidacja w kilku ośrodkach sugeruje, że metoda jest odporna na różnice między szpitalami i grupami pacjentek.
Co to może znaczyć dla przyszłej opieki
Dla pacjentek główne przesłanie jest proste: ucząc się na wzorcach występujących wśród wielu podobnych osób, to nowe narzędzie może dokładniej wskazać, kto prawdopodobnie skorzysta z chemioterapii przed zabiegiem, a kto powinien otrzymać inną strategię. Wysoki wynik wskazuje silniejsze szanse dłuższego przeżycia i skutecznego usunięcia guza, natomiast niski wynik może skłonić lekarzy do ponownego rozważenia terminu operacji lub rozważenia alternatywnych terapii zamiast kontynuacji strategii mało obiecującej. Po dalszych badaniach prospektywnych i integracji z oprogramowaniem szpitalnym modele oparte na grafach, takie jak ten, mogą przyczynić się do odejścia od uniwersalnych decyzji terapeutycznych i do wprowadzenia opieki lepiej dopasowanej do indywidualnego profilu każdej kobiety.
Cytowanie: Zhang, S., Liu, Y., Liu, Z. et al. Multimodal data-based graph convolutional networks for predicting outcomes in ovarian cancer receiving neoadjuvant chemotherapy. npj Precis. Onc. 10, 157 (2026). https://doi.org/10.1038/s41698-026-01346-9
Słowa kluczowe: rak jajnika, chemioterapia neoadjuwantowa, grafowe sieci neuronowe, radiomika, predykcja leczenia