Clear Sky Science · fr
Réseaux de neurones convolutionnels sur graphes basés sur des données multimodales pour prédire les résultats chez les patientes atteintes d’un cancer de l’ovaire recevant une chimiothérapie néoadjuvante
Pourquoi cette recherche compte pour les patientes
Pour les femmes confrontées à un cancer de l’ovaire avancé, choisir la bonne stratégie thérapeutique peut changer la vie. Beaucoup reçoivent une chimiothérapie avant la chirurgie pour réduire les tumeurs et rendre l’opération plus sûre, mais les cliniciens peinent encore à prédire qui en bénéficiera le plus et qui devrait suivre une autre approche. Cette étude présente une méthode nouvelle et plus précise pour prévoir à la fois la survie et la réussite chirurgicale en s’appuyant sur des informations déjà recueillies dans les hôpitaux, ce qui pourrait rendre des soins plus personnalisés accessibles dans les établissements courants.
Voir la patiente dans sa globalité, pas seulement un chiffre
Traditionnellement, les médecins se fient à quelques mesures isolées pour orienter le traitement avant la chirurgie. Un exemple courant est le score KELIM, qui suit la rapidité de la baisse d’un marqueur tumoral appelé CA‑125 au début de la chimiothérapie. D’autres outils s’appuient sur les images scannographiques ou sur des ratios simples de biologie comme les numérations en éléments blancs. Utile, chacun de ces éléments ne reflète cependant qu’un aspect de l’histoire d’une patiente. L’approche présentée reconnaît que les patientes sont plus complexes : analyses sanguines, caractéristiques des images, âge et traits tumoraux interagissent de façon subtile et influencent la réponse au traitement.
Relier des patientes similaires pour créer un réseau d’apprentissage
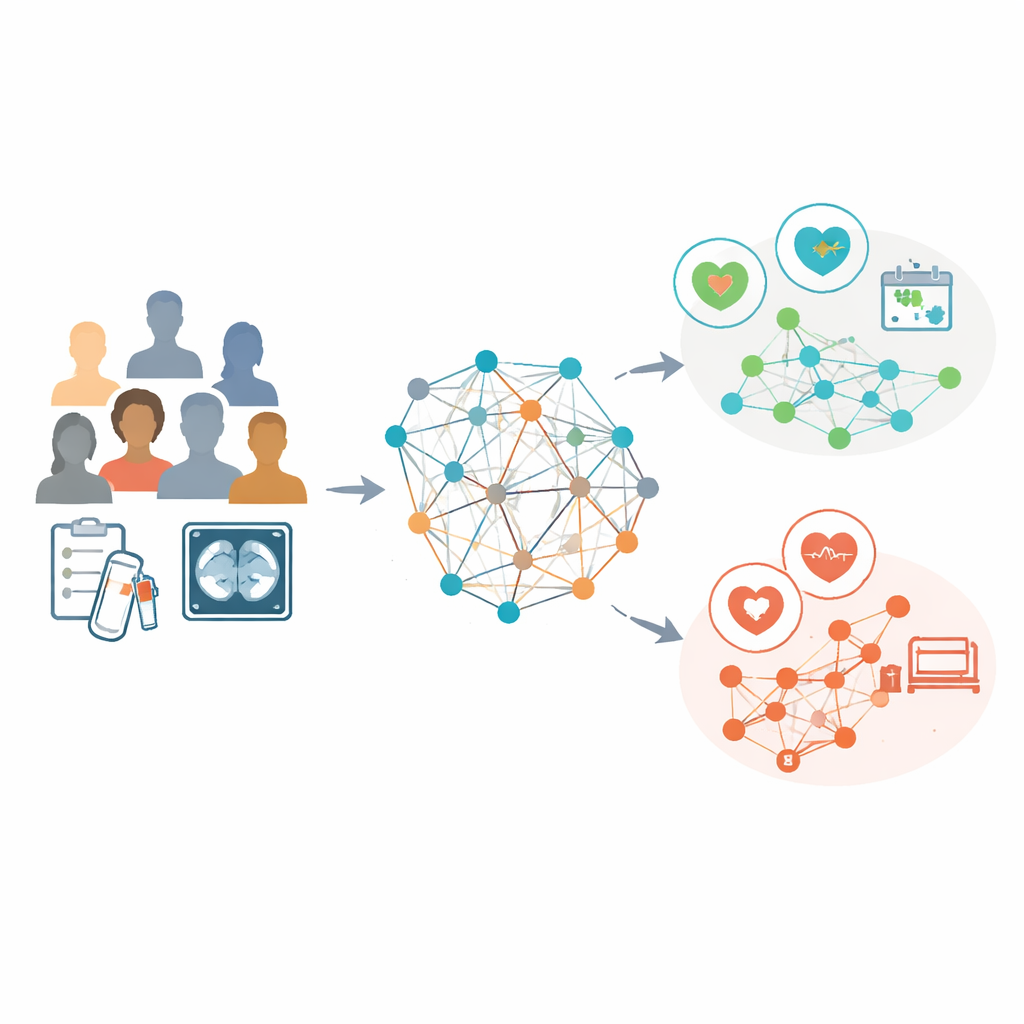
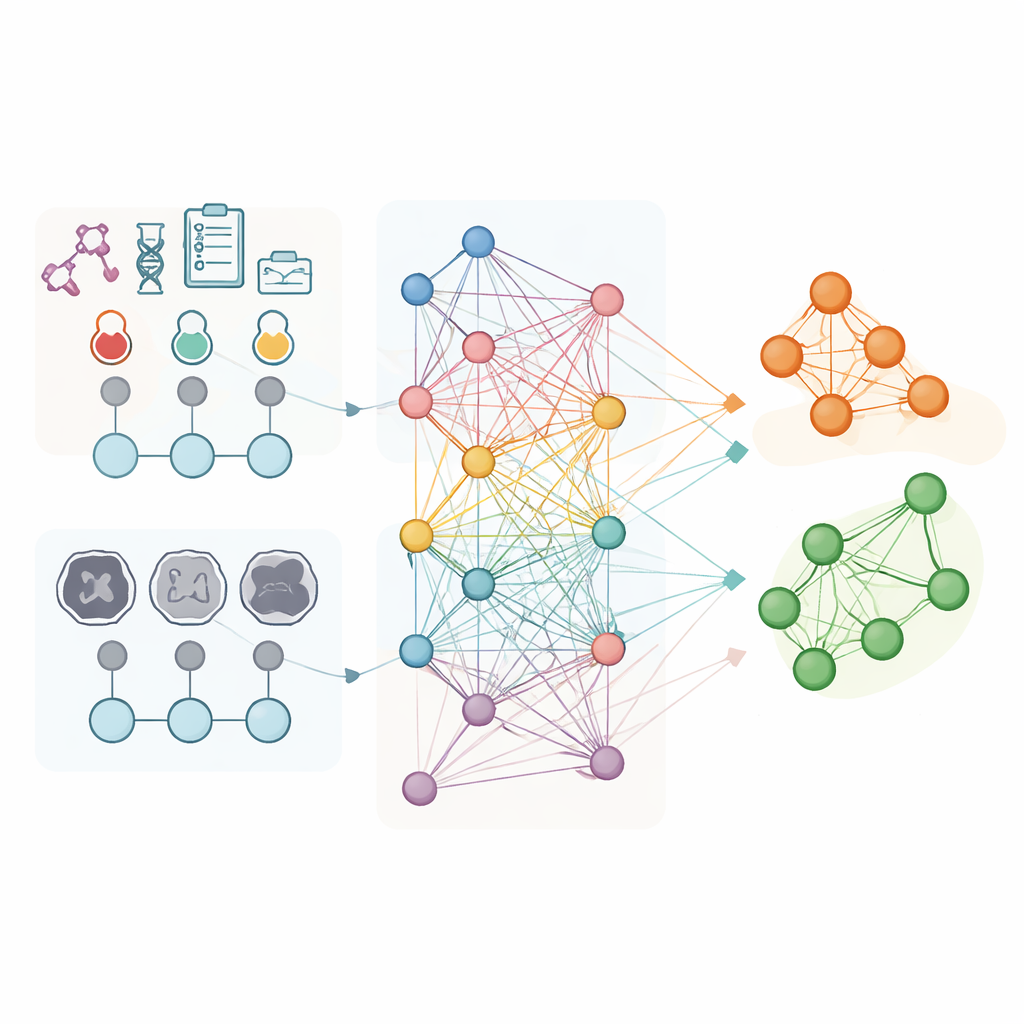
Les chercheurs ont analysé les données de 853 femmes atteintes d’un cancer de l’ovaire avancé ayant toutes reçu une chimiothérapie avant une chirurgie d’intervalle dans trois hôpitaux. Pour chaque patiente, ils ont utilisé des résultats biologiques de routine et des caractéristiques détaillées extraites des scanners pré‑traitement, comme la forme et la texture des tumeurs visibles. Plutôt que de considérer chaque cas isolément, ils ont construit un « graphe de population » où chaque patiente est un nœud et où des liens relient les personnes présentant des profils biologiques similaires. Une forme spécialisée d’intelligence artificielle, appelée réseau de neurones convolutionnel sur graphes, a alors appris des motifs au sein de ce réseau, utilisant les caractéristiques issues des scanners comme descripteurs principaux de chaque nœud tandis que les connexions transportaient l’information sur les ressemblances entre patientes.
De meilleures performances que les outils de prédiction actuels
L’équipe a demandé à leur modèle d’estimer deux éléments d’importance pour les patientes et les chirurgiens : la survie globale sur plusieurs années et la probabilité d’obtenir une opération sans tumeur visible résiduelle (appelée résection R0). Ils ont comparé ses performances à quatre approches établies construites à partir de données cliniques, de caractéristiques d’imagerie seules, de l’ensemble combiné, du score KELIM, ainsi qu’un système de cotation chirurgical couramment utilisé. Dans l’hôpital principal et dans deux hôpitaux tests indépendants, le modèle basé sur le graphe a systématiquement fourni des prévisions de survie plus précises. Il a également mieux distingué quelles patientes étaient susceptibles de terminer l’intervention sans tumeur visible et lesquelles ne le seraient pas, même lorsque les modèles traditionnels montraient peu de séparation.
Déceler de l’espoir là où les scores anciens voient du risque
Une des découvertes les plus marquantes est que le nouveau modèle a révélé un groupe important de femmes — environ 16 % de l’ensemble — qui avaient de faibles scores KELIM (signalant habituellement une mauvaise réponse) mais qui ont en réalité vécu aussi longtemps que celles présentant des KELIM favorables. Autrement dit, les outils plus anciens les auraient classées à haut risque, tandis que la méthode fondée sur le graphe a correctement reconnu leur bon pronostic. Le modèle a aussi montré une relation progressive et continue entre son score et les résultats : à mesure que le score augmentait, la durée de survie et la probabilité d’une résection complète augmentaient régulièrement, passant d’une quasi‑absence de R0 aux scores les plus bas à presque toutes les patientes atteignant R0 aux scores les plus élevés. Ce schéma progressif n’était pas observé avec le KELIM seul, ce qui suggère que le nouveau score capte un signal biologique plus net.
Conçu pour une utilisation hospitalière réelle
Beaucoup d’outils d’IA avancés exigent des processeurs graphiques puissants rarement présents sur les ordinateurs hospitaliers standards. En revanche, ce modèle basé sur les graphes a été conçu pour fonctionner entièrement sur des processeurs centraux ordinaires, ce qui le rend plus pratique pour un usage clinique quotidien. Il s’appuie sur des analyses de laboratoire et des scanners déjà intégrés aux soins de routine, et les auteurs ont montré que sa valeur prédictive restait élevée même après prise en compte de l’âge, du stade tumoral, du type et du score KELIM. Bien que l’étude soit rétrospective et n’ait pas encore inclus de marqueurs génétiques comme le statut BRCA, sa validation multicentrique suggère que la méthode est robuste entre différents hôpitaux et groupes de patientes.
Ce que cela pourrait signifier pour les soins futurs
Pour les patientes, le message principal est simple : en apprenant des motifs observés chez de nombreuses personnes similaires, cet outil peut mieux identifier qui est susceptible de bénéficier d’une chimiothérapie avant chirurgie et qui pourrait nécessiter une autre stratégie. Un score élevé indique une forte probabilité de survie prolongée et de résection tumorale complète, tandis qu’un score faible pourrait inciter les médecins à reconsidérer le calendrier de la chirurgie ou à explorer des thérapies alternatives plutôt que de poursuivre une stratégie peu prometteuse. Avec des tests prospectifs supplémentaires et une intégration dans les logiciels hospitaliers, des modèles basés sur des graphes comme celui‑ci pourraient aider à faire évoluer le traitement du cancer de l’ovaire vers des décisions moins standardisées et mieux adaptées au profil unique de chaque femme.
Citation: Zhang, S., Liu, Y., Liu, Z. et al. Multimodal data-based graph convolutional networks for predicting outcomes in ovarian cancer receiving neoadjuvant chemotherapy. npj Precis. Onc. 10, 157 (2026). https://doi.org/10.1038/s41698-026-01346-9
Mots-clés: cancer de l’ovaire, chimiothérapie néoadjuvante, réseaux de neurones sur graphes, radiomique, prévision du traitement