Clear Sky Science · nl
Multimodale, op gegevens gebaseerde graafconvolutionele netwerken voor het voorspellen van uitkomsten bij eierstokkanker bij patiënten die neoadjuvante chemotherapie krijgen
Waarom dit onderzoek belangrijk is voor patiënten
Voor vrouwen met gevorderde eierstokkanker kan het kiezen van de juiste behandelingsroute levensveranderend zijn. Velen krijgen eerst chemotherapie om tumoren te verkleinen en operaties veiliger te maken, maar artsen hebben nog moeilijkheden te voorspellen wie het meeste baat heeft en wie mogelijk een andere strategie nodig heeft. Deze studie presenteert een nieuwe, nauwkeurigere manier om zowel overleving als chirurgisch succes te voorspellen met behulp van informatie die ziekenhuizen al verzamelen, wat persoonlijkere zorg binnen bereik van gewone klinieken kan brengen.
De hele patiënt zien, niet slechts één getal
Traditioneel baseren artsen zich op enkele afzonderlijke metingen om de behandeling voor de operatie te sturen. Een bekend voorbeeld is de bloedtestpatroon genaamd KELIM-score, die volgt hoe snel een tumormarker, CA‑125, daalt tijdens vroege chemotherapie. Andere instrumenten kijken naar bevindingen op scans of eenvoudige laboratoriumverhoudingen zoals witte bloedcelwaarden. Hoewel nuttig, richten al deze methoden zich maar op één deel van het verhaal van een patiënt. De nieuwe benadering erkent dat echte patiënten complexer zijn: bloedwaarden, scangegevens, leeftijd en tumorkenmerken beïnvloeden elkaar op subtiele manieren die bepalen hoe iemand op de behandeling reageert.
Vergelijkbare patiënten verbinden in een leerend netwerk
De onderzoekers analyseerden gegevens van 853 vrouwen met gevorderde eierstokkanker die allemaal chemotherapie kregen vóór intervaloperatie in drie ziekenhuizen. Voor elke patiënt gebruikten ze routinematige laboratoriumuitslagen en gedetailleerde kenmerken die uit pretreatment CT‑scans werden gehaald, zoals de vorm en textuur van zichtbare tumoren. In plaats van elke persoon als een geïsoleerd geval te behandelen, bouwden ze een "populatiegraaf" waarin elke patiënt een knooppunt is en verbindingen patiënten met vergelijkbare labprofielen koppelen. Een gespecialiseerde vorm van kunstmatige intelligentie, een graafconvolutioneel netwerk, leerde vervolgens patronen over dit netwerk, waarbij de CT‑gebaseerde kenmerken dienden als de belangrijkste beschrijvingen voor elk knooppunt en de verbindingen informatie droegen over hoe patiënten op elkaar leken.
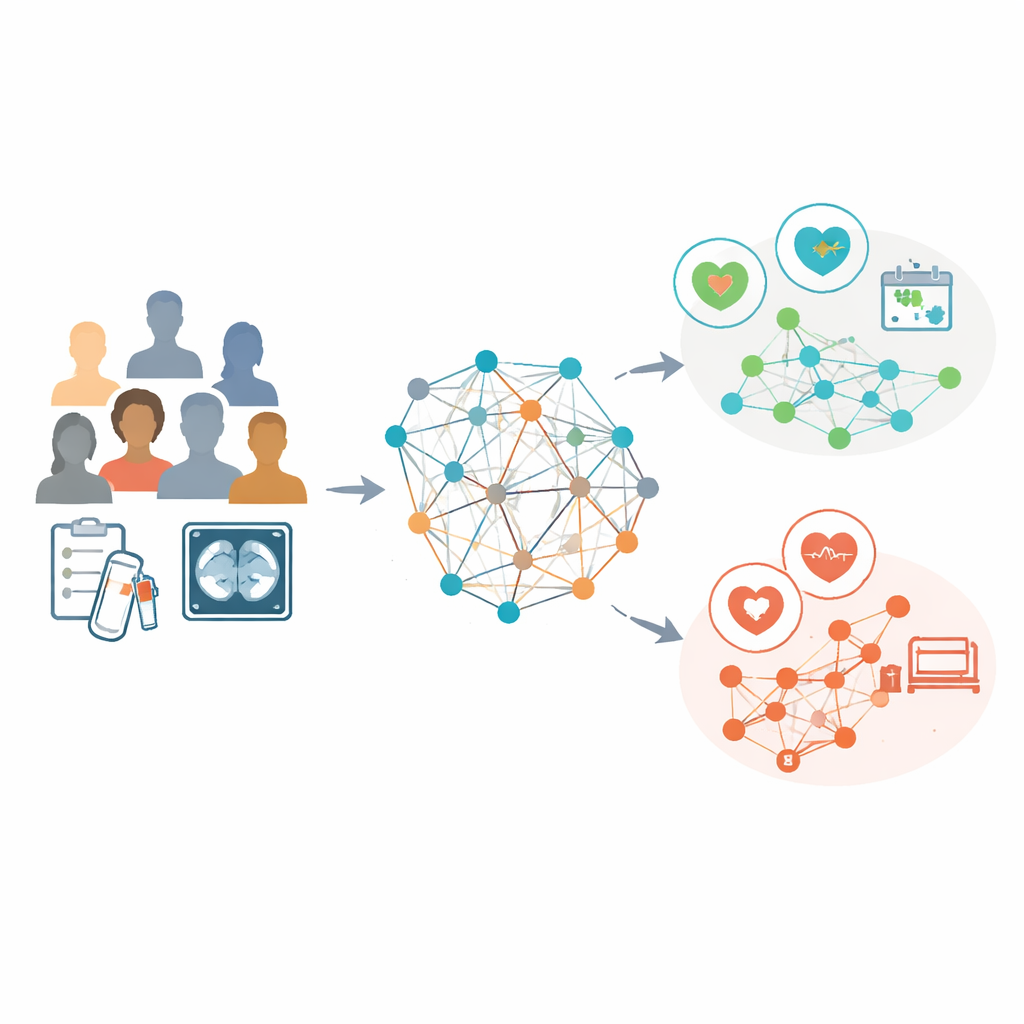
Betere prestaties dan bestaande voorspellende hulpmiddelen
Het team liet hun model twee zaken voorspellen die van groot belang zijn voor patiënten en chirurgen: de totale overleving over meerdere jaren en de kans op het behalen van een operatie zonder zichtbaar tumorweefsel achter te laten (R0‑resectie). Ze vergeleken de prestaties met vier gevestigde benaderingen opgebouwd uit klinische gegevens, alleen scankenmerken, een combinatie van beide, en de KELIM‑score, evenals een veelgebruikt chirurgisch scoremodel. In het hoofdziekenhuis en in twee onafhankelijke testziekenhuizen leverde het graafgebaseerde model consequent nauwkeurigere overlevingsvoorspellingen. Het deed ook beter dan de andere methoden in het onderscheiden welke patiënten waarschijnlijk met een tumorvrije operatie zouden eindigen en welke niet, zelfs wanneer traditionele modellen weinig scheiding lieten zien.
Hoop vinden waar oudere scores risico zien
Een van de meest opvallende bevindingen was dat het nieuwe model een aanzienlijke groep vrouwen — ongeveer 16 procent van het totaal — identificeerde die lage KELIM‑scores hadden (wat gewoonlijk op een slechte respons wijst) maar die in werkelijkheid even lang leefden als degenen met gunstige KELIM‑waarden. Met andere woorden, oudere instrumenten zouden hen als hoog risico hebben bestempeld, terwijl de graafgebaseerde methode hun goede vooruitzicht correct herkende. Het model toonde ook een vloeiende, stapsgewijze relatie tussen zijn score en uitkomsten: naarmate de score steeg, namen zowel de overlevingstijd als de kans op volledige tumorverwijdering gestaag toe — van bijna geen R0‑operaties bij de laagste scores tot vrijwel alle patiënten die R0 bereikten bij de hoogste scores. Dit consistente patroon werd niet gezien met alleen KELIM, wat suggereert dat de nieuwe score een helderder biologisch signaal opvangt.
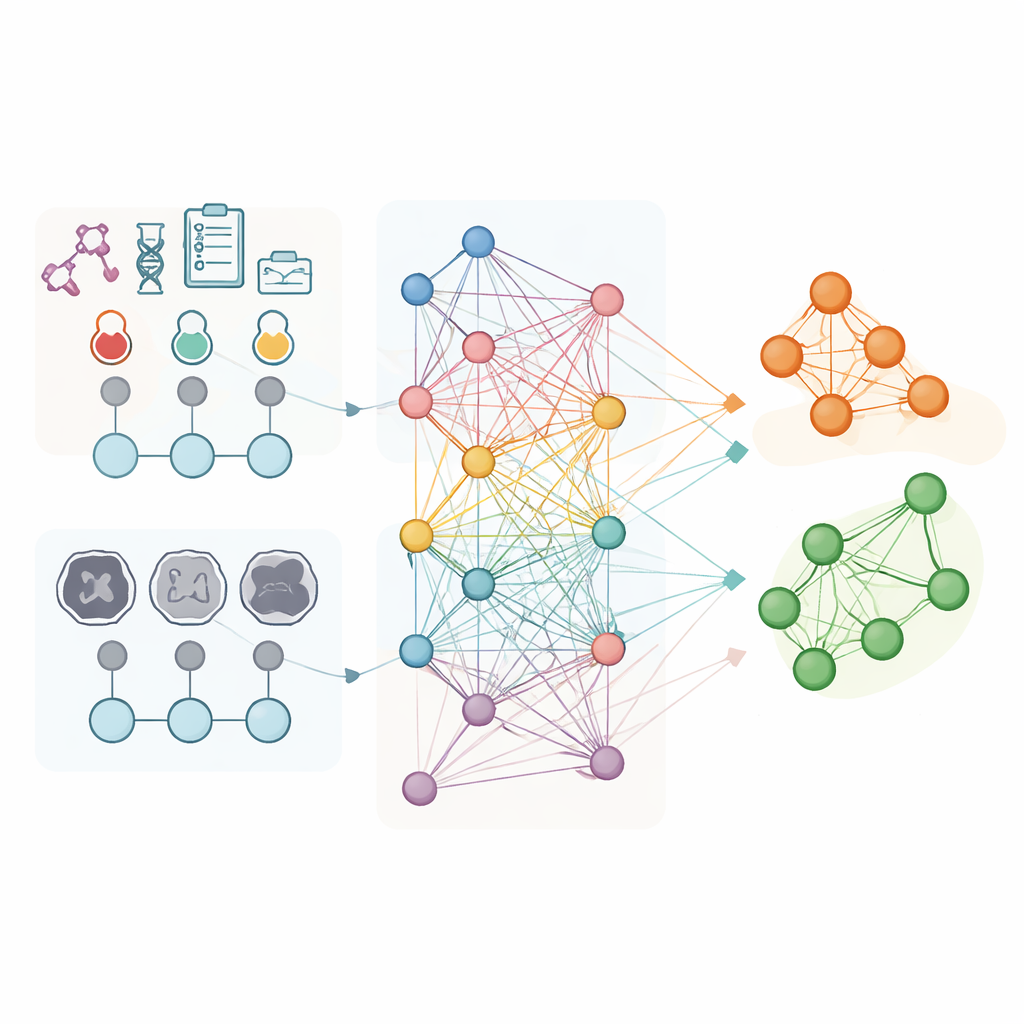
Ontworpen voor gebruik in de echte wereld van ziekenhuizen
Veel geavanceerde AI‑instrumenten vereisen krachtige grafische processors die zelden beschikbaar zijn in standaard ziekenhuiscomputers. In tegenstelling daarmee is dit graafgebaseerde model gebouwd om volledig op gewone centrale processors te draaien, waardoor het praktischer is voor dagelijks klinisch gebruik. Het vertrouwt op labtests en CT‑scans die al deel uitmaken van routinematige zorg, en de auteurs lieten zien dat de voorspellende waarde sterk bleef, zelfs na correctie voor leeftijd, tumoirstadium, type en de KELIM‑score. Hoewel de studie retrospectief was en nog geen genetische markers zoals BRCA‑status bevatte, suggereert de multicenter‑validatie dat de methode robuust is over verschillende ziekenhuizen en patiëntengroepen.
Wat dit zou kunnen betekenen voor toekomstige zorg
Voor patiënten is de kernboodschap helder: door te leren van patronen over veel vergelijkbare individuen kan dit nieuwe hulpmiddel nauwkeuriger vaststellen wie waarschijnlijk baat heeft bij chemotherapie vóór de operatie en wie een andere aanpak nodig heeft. Een hoge score wijst op een grote kans op langere overleving en succesvolle tumorverwijdering, terwijl een lage score artsen kan aansporen de timing van de operatie te heroverwegen of alternatieve therapieën te verkennen in plaats van vol te houden met een strategie die waarschijnlijk niet helpt. Met verdere prospectieve testing en integratie in ziekenhuissoftware zouden graafgebaseerde modellen zoals dit kunnen bijdragen aan een verschuiving van one‑size‑fits‑all beslissingen naar zorg die beter is afgestemd op het unieke profiel van elke vrouw.
Bronvermelding: Zhang, S., Liu, Y., Liu, Z. et al. Multimodal data-based graph convolutional networks for predicting outcomes in ovarian cancer receiving neoadjuvant chemotherapy. npj Precis. Onc. 10, 157 (2026). https://doi.org/10.1038/s41698-026-01346-9
Trefwoorden: eierstokkanker, neoadjuvante chemotherapie, grafische neurale netwerken, radiomics, behandelingsvoorspelling