Clear Sky Science · ru
Графовые сверточные сети на основе мультимодальных данных для прогнозирования исходов у пациенток с раком яичников, получающих неоадъювантную химиотерапию
Почему это исследование важно для пациенток
Для женщин с распространённым раком яичников выбор правильной стратегии лечения может изменить жизнь. Многие получают химиотерапию до операции, чтобы уменьшить опухоли и сделать вмешательство безопаснее, но врачам по‑прежнему трудно предсказать, кто извлечёт из этого наибольшую пользу, а кому потребуются иные подходы. В этом исследовании предложен новый, более точный способ прогнозирования как выживаемости, так и вероятности успешной хирургии, основанный на данных, которые уже собирают больницы, — это может приблизить индивидуализированную помощь к повседневной клинической практике.
Видеть пациентку целиком, а не опираться на одно число
Традиционно врачи опираются на несколько отдельных измерений при принятии решений до операции. Один из широко используемых примеров — показатель KELIM, основанный на скорости снижения маркера CA‑125 в ранний период химиотерапии. Другие инструменты рассматривают данные сканирования или простые лабораторные соотношения, например числа лейкоцитов. Эти подходы полезны, но каждый охватывает лишь одну сторону клинической картины. Новый метод признаёт, что пациентки сложнее: анализы крови, данные КТ, возраст и характеристики опухоли взаимодействуют тонкими способами, которые влияют на реакцию на лечение.
Связывая похожих пациенток в единую обучающую сеть
Исследователи проанализировали данные 853 женщин с распространённым раком яичников, получивших химиотерапию перед промежуточной операцией в трёх больницах. Для каждой пациентки использовали рутинные лабораторные результаты и подробные характеристики, извлечённые из предлечебных КТ‑сканов, такие как форма и текстура видимых опухолей. Вместо того чтобы рассматривать каждую пациентку как изолированный случай, они построили «популяционный граф», где каждая пациентка представлена узлом, а связи соединяют пациенток с похожими лабораторными профилями. Специальный вид искусственного интеллекта — графовая сверточная сеть — затем изучал закономерности в этой сети, используя признаки, основанные на КТ, в качестве основных описателей узлов, а связи передавали информацию о сходстве между пациентками.
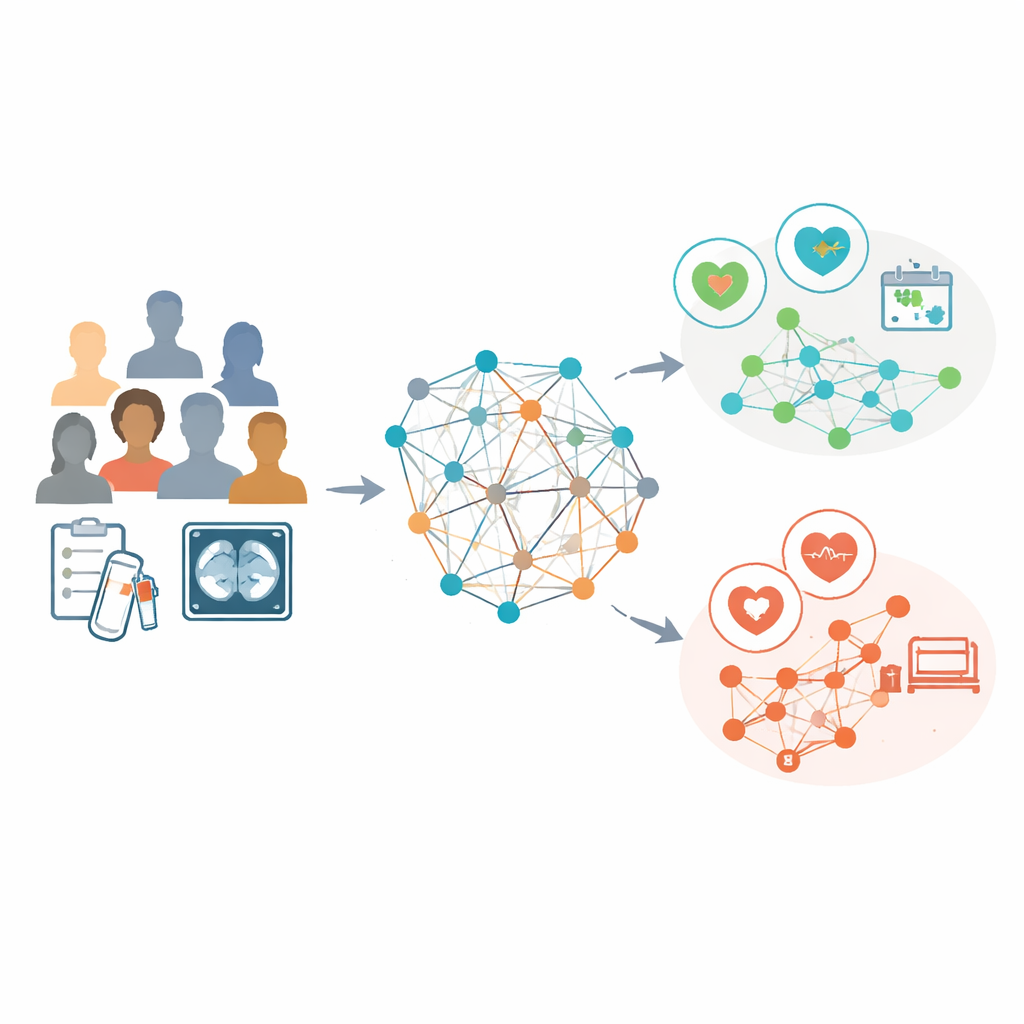
Превосходство над существующими инструментами прогнозирования
Команда попросила модель выполнить две задачи, важные для пациенток и хирургов: спрогнозировать общую выживаемость на протяжении нескольких лет и оценить вероятность проведения операции, оставляющей после себя отсутствие видимой опухоли (R0‑резекция). Они сравнили её работу с четырьмя устоявшимися подходами, построенными на клинических данных, только признаках сканирования, их сочетании и показателе KELIM, а также с общепринятой хирургической шкалой. В основной больнице и в двух независимых тестовых центрах модель на графах последовательно давала более точные прогнозы выживаемости. Она также лучше разделяла пациенток по вероятности достижения R0, даже когда традиционные модели давали слабое разделение.
Надеяться там, где старые показатели видят риск
Одним из наиболее заметных результатов стало то, что новая модель выделила значительную группу женщин — около 16 процентов от общего числа — у которых были низкие значения KELIM (обычно ассоциируемые с плохим ответом), но которые фактически жили так же долго, как пациентки с благоприятным KELIM. Иными словами, старые инструменты относили их к группе высокого риска, тогда как модель на основе графа верно распознавала благоприятный прогноз. Модель также показала плавную, ступенчатую зависимость между своим баллом и исходами: с ростом балла и время выживания, и вероятность полного удаления опухоли увеличивались устойчиво — от почти отсутствия R0 при самых низких значениях до почти всех пациентов с R0 при самых высоких. Такой ясной закономерности KELIM в одиночку не демонстрировал, что говорит о более чётком биологическом сигнале в новом показателе.
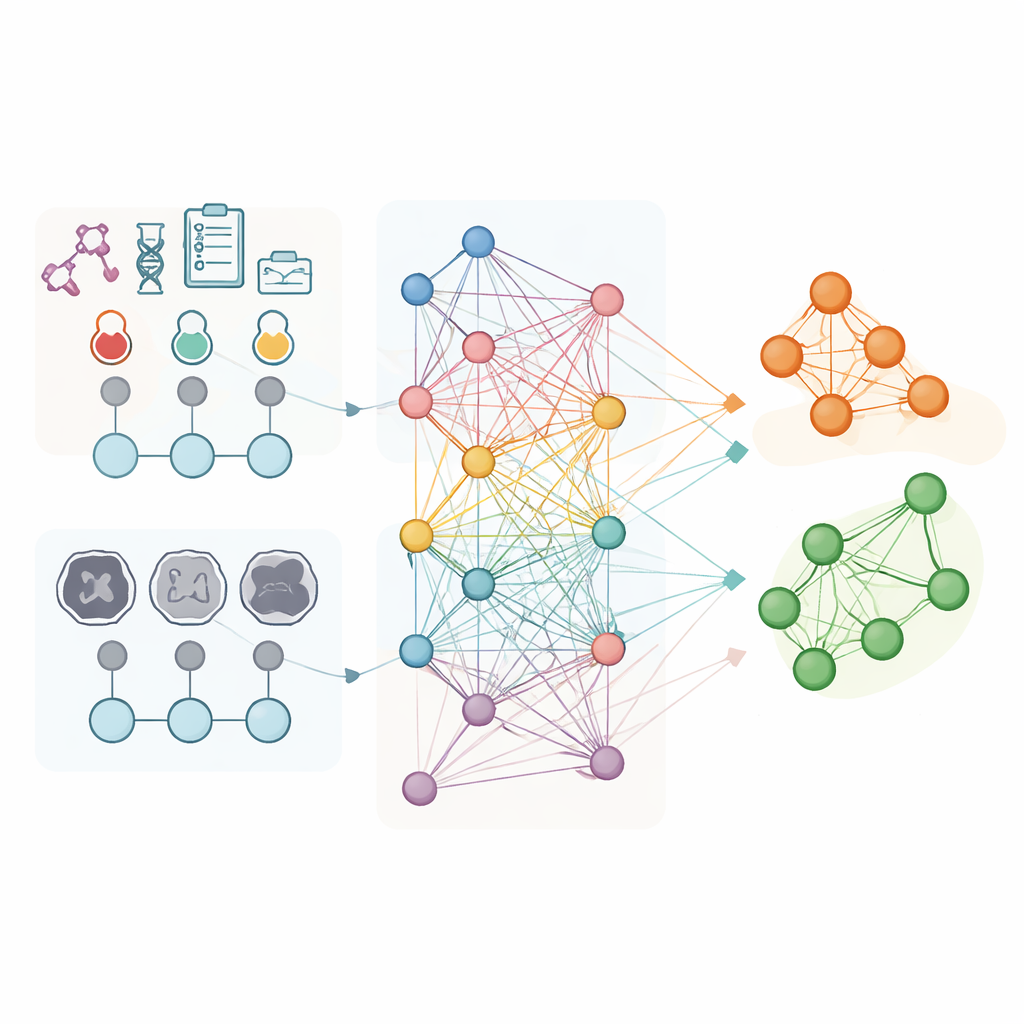
Разработано с прицелом на реальную работу в больницах
Многие продвинутые ИИ‑инструменты требуют мощных графических процессоров, которые редко есть в стандартных больничных компьютерах. Напротив, эта модель на графах была разработана для работы полностью на обычных центральных процессорах, что делает её более практичной для повседневного клинического применения. Она опирается на лабораторные тесты и КТ, которые уже входят в стандартный уход, и авторы показали, что её прогностическая сила сохраняется даже после учёта возраста, стадии и типа опухоли и показателя KELIM. Хотя исследование было ретроспективным и пока не включало генетические маркёры, такие как статус BRCA, многоцентровая валидация указывает на устойчивость метода в разных больницах и группах пациенток.
Что это может значить для будущего лечения
Для пациенток основной вывод прост: изучая закономерности среди многих похожих людей, этот новый инструмент может точнее определять, кто извлечёт выгоду из химиотерапии перед операцией, а кому стоит предложить иной план. Высокий балл означает высокую вероятность более длительной выживаемости и успешного удаления опухоли, а низкий балл может подтолкнуть врачей пересмотреть сроки операции или рассмотреть альтернативные терапии вместо продолжения стратегии, маловероятной для пользы. При дальнейшем проспективном тестировании и интеграции в больничное программное обеспечение модели на графах, подобные этой, могут помочь перейти от решений «один‑размер‑для‑всех» к уходу, более точно соответствующему индивидуальному профилю каждой женщины.
Цитирование: Zhang, S., Liu, Y., Liu, Z. et al. Multimodal data-based graph convolutional networks for predicting outcomes in ovarian cancer receiving neoadjuvant chemotherapy. npj Precis. Onc. 10, 157 (2026). https://doi.org/10.1038/s41698-026-01346-9
Ключевые слова: рак яичников, неоадъювантная химиотерапия, графовые нейронные сети, радиомика, прогнозирование лечения