Clear Sky Science · de
Multimodale, datenbasierte graphkonvolutionelle Netzwerke zur Vorhersage von Ergebnissen bei Ovarialkarzinom unter neoadjuvanter Chemotherapie
Warum diese Forschung für Patientinnen wichtig ist
Für Frauen mit fortgeschrittenem Ovarialkarzinom kann die Wahl des richtigen Behandlungswegs lebensverändernd sein. Viele erhalten vor einer Operation Chemotherapie, um Tumore zu verkleinern und Eingriffe sicherer zu machen, doch Ärztinnen und Ärzte haben weiterhin Schwierigkeiten vorherzusagen, wer am meisten profitieren wird und wer möglicherweise eine andere Strategie benötigt. Diese Studie präsentiert eine neue, genauere Methode zur Vorhersage sowohl des Überlebens als auch des operativen Erfolgs anhand der Informationen, die Krankenhäuser bereits routinemäßig erheben, und könnte so eine individuellere Versorgung in alltäglichen Kliniken näherbringen.
Den ganzen Patienten sehen, nicht nur eine Zahl
Traditionell stützen sich Ärzte auf wenige Einzelmessungen, um die Behandlung vor einer Operation zu lenken. Ein bekanntes Beispiel ist der KELIM‑Score, ein Bluttestmuster, das verfolgt, wie schnell der Tumormarker CA‑125 in den frühen Zyklen der Chemotherapie fällt. Andere Werkzeuge basieren auf Bildbefunden oder einfachen Laborverhältnissen wie Leukozytenzahlen. Diese Ansätze sind nützlich, betrachten jedoch jeweils nur einen Ausschnitt der Patientengeschichte. Der neue Ansatz berücksichtigt, dass reale Patientinnen komplexer sind: Laborwerte, Bilddetails, Alter und Tumoreigenschaften interagieren auf subtile Weise und beeinflussen, wie jemand auf Therapie reagiert.
Ähnliche Patientinnen zu einem lernenden Netzwerk verknüpfen
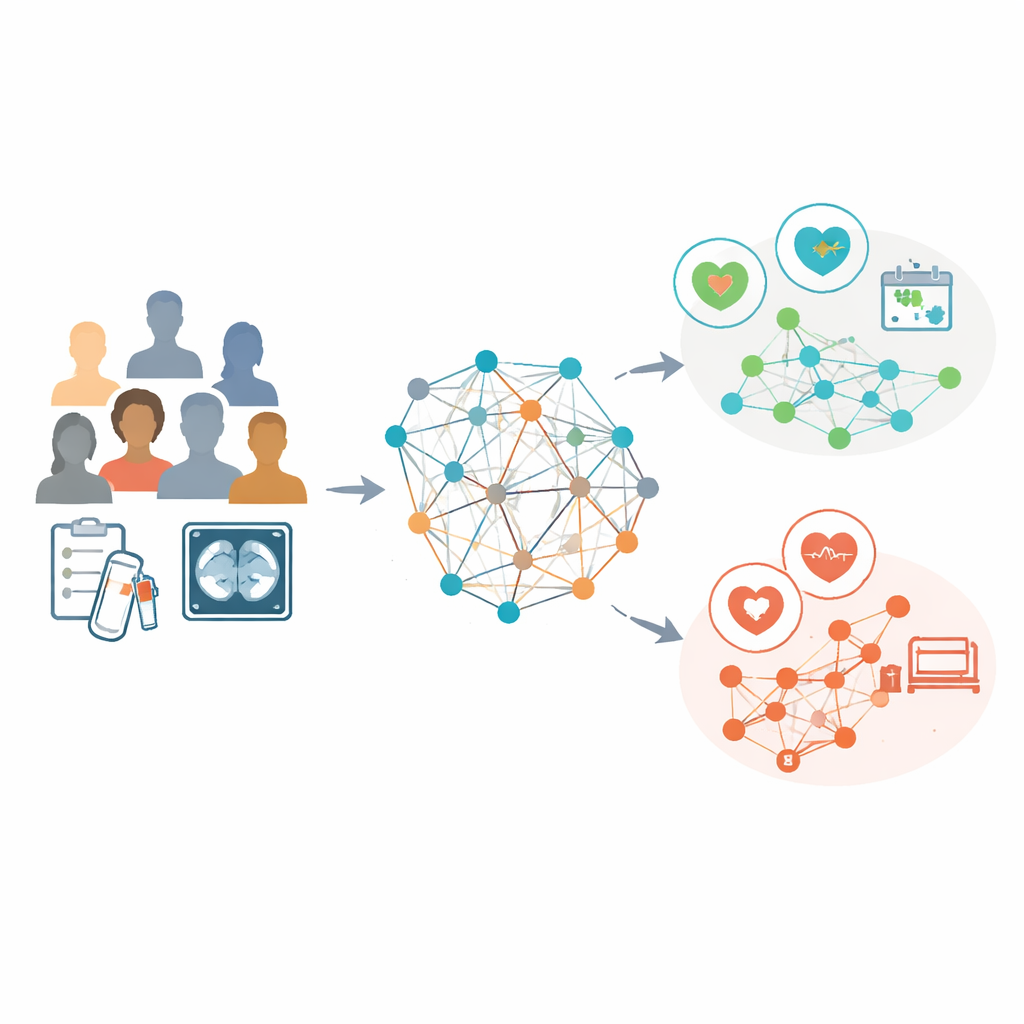
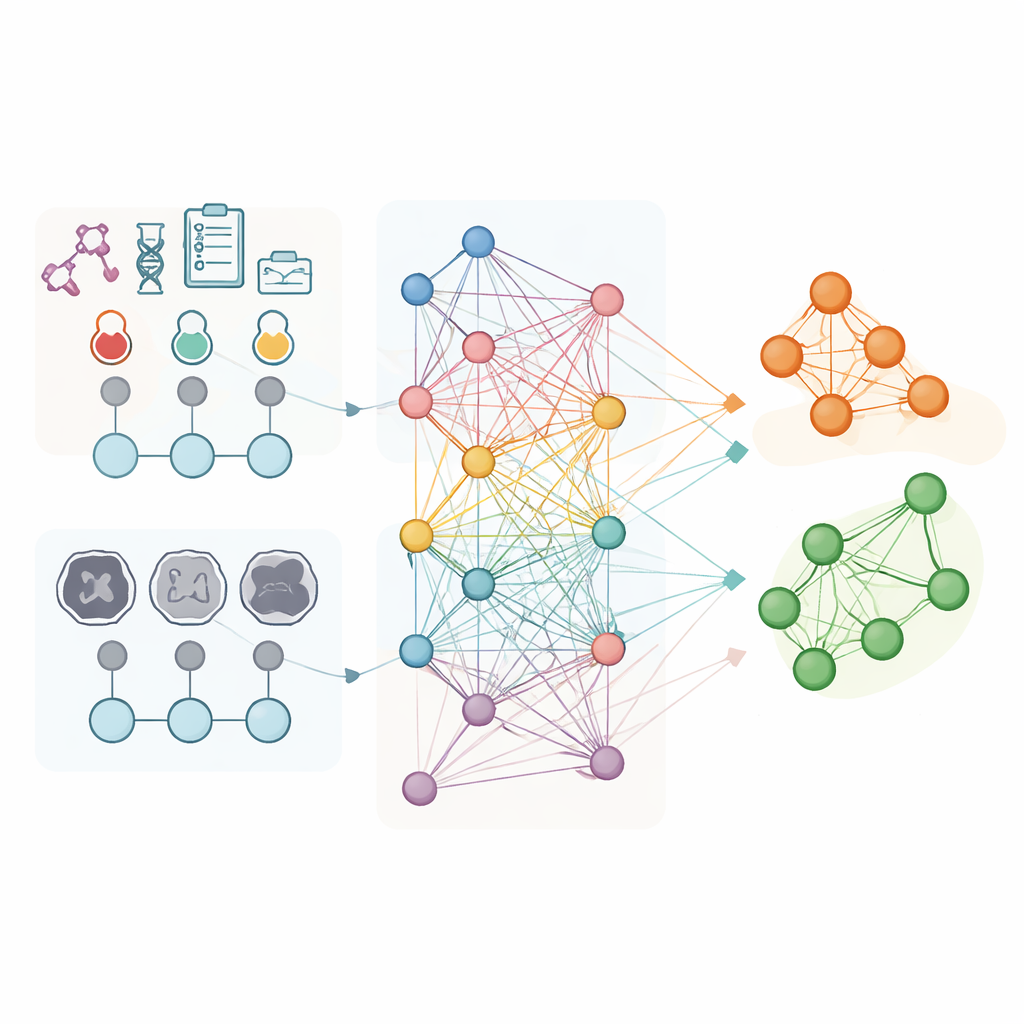
Die Forschenden analysierten Daten von 853 Frauen mit fortgeschrittenem Ovarialkarzinom, die alle vor einer Intervalloperation Chemotherapie an drei Krankenhäusern erhalten hatten. Für jede Patientin nutzten sie routinemäßige Laborwerte und detaillierte Merkmale, die aus den CT‑Aufnahmen vor der Behandlung extrahiert wurden, etwa Form und Textur sichtbarer Tumore. Anstatt jede Person als isolierten Fall zu behandeln, bauten sie einen „Populationsgraphen“ auf, in dem jede Patientin ein Knoten darstellt und Verbindungen Patientinnen mit ähnlichen Laborprofilen verknüpfen. Eine spezialisierte Form künstlicher Intelligenz, ein graphkonvolutionelles Netzwerk, lernte dann Muster über dieses Netz hinweg, wobei die CT‑basierten Merkmale die Hauptbeschreibungen für jeden Knoten lieferten und die Verbindungen Informationen darüber trugen, wie sich Patientinnen ähneln.
Die aktuellen Vorhersagewerkzeuge übertreffen
Das Team ließ ihr Modell zwei für Patientinnen und Operateurinnen wichtige Aufgaben übernehmen: das Gesamtüberleben über mehrere Jahre vorherzusagen und die Wahrscheinlichkeit abzuschätzen, eine Operation ohne sichtbare Tumorreste (sogenannte R0‑Resektion) zu erreichen. Sie verglichen die Leistung mit vier etablierten Ansätzen, die auf klinischen Daten, Bildmerkmalen allein, einer Kombination beider sowie dem KELIM‑Score basieren, außerdem mit einem gebräuchlichen chirurgischen Score. In der Ausgangsklinik und in zwei unabhängigen Testkliniken lieferte das graphbasierte Modell durchgehend genauere Überlebensprognosen. Es unterschied außerdem besser als die anderen Methoden, welche Patientinnen wahrscheinlich tumorfrei operiert werden konnten und welche nicht, selbst wenn traditionelle Modelle nur geringe Trennung zeigten.
Hoffnung finden, wo ältere Scores Risiko sehen
Eines der auffälligsten Ergebnisse war, dass das neue Modell eine beträchtliche Gruppe von Frauen — etwa 16 Prozent der Gesamtmenge — identifizierte, die niedrige KELIM‑Werte hatten (was üblicherweise auf schlechte Therapieansprechen hinweist), aber tatsächlich genauso lange lebten wie diejenigen mit günstigen KELIM‑Werten. Anders ausgedrückt: Ältere Werkzeuge hätten sie als Hochrisiko eingestuft, während die graphbasierte Methode ihre gute Prognose korrekt erkannte. Das Modell zeigte außerdem eine glatte, stufenartige Beziehung zwischen seinem Score und den Ergebnissen: Mit steigendem Score nahmen sowohl die Überlebenszeit als auch die Chance auf vollständige Tumorentfernung stetig zu — von nahezu keinen R0‑Operationen bei den niedrigsten Werten bis hin zu fast allen Patientinnen mit R0 bei den höchsten. Dieses stetige Muster zeigte sich nicht allein beim KELIM, was nahelegt, dass der neue Score ein klareres biologisches Signal erfasst.
Für den Einsatz im Klinikalltag entwickelt
Viele fortgeschrittene KI‑Werkzeuge benötigen leistungsstarke Grafikprozessoren, die in Standardkrankenhauscomputern selten vorhanden sind. Im Gegensatz dazu wurde dieses graphbasierte Modell so entwickelt, dass es vollständig auf gewöhnlichen Zentralprozessoren läuft, was es praktischer für den täglichen klinischen Einsatz macht. Es stützt sich auf Laboruntersuchungen und CT‑Aufnahmen, die bereits zur Routine gehören, und die Autorinnen und Autoren zeigten, dass sein Vorhersagewert stark blieb, selbst nachdem Alter, Tumorstadium, Tumortyp und der KELIM‑Score berücksichtigt wurden. Obwohl die Studie retrospektiv war und noch keine genetischen Marker wie BRCA‑Status einschloss, deutet die multizentrische Validierung darauf hin, dass die Methode über verschiedene Krankenhäuser und Patientengruppen hinweg robust ist.
Was das für die zukünftige Versorgung bedeuten könnte
Für Patientinnen ist die Kernbotschaft einfach: Indem das Modell Muster über viele ähnliche Personen lernt, kann es genauer identifizieren, wer wahrscheinlich von einer Chemotherapie vor der Operation profitiert und wer einen anderen Plan benötigen könnte. Ein hoher Score signalisiert eine hohe Wahrscheinlichkeit für längeres Überleben und erfolgreiche Tumorentfernung, während ein niedriger Score Ärztinnen und Ärzte veranlassen kann, den Operationszeitpunkt zu überdenken oder alternative Therapien zu prüfen, anstatt an einer Strategie festzuhalten, die vermutlich wenig nützt. Mit weiteren prospektiven Tests und der Integration in Krankenhaus‑Software könnten graphbasierte Modelle wie dieses dazu beitragen, die Behandlung des Ovarialkarzinoms von Einheitslösungen hin zu einer stärker auf das individuelle Profil jeder Frau zugeschnittenen Versorgung zu bewegen.
Zitation: Zhang, S., Liu, Y., Liu, Z. et al. Multimodal data-based graph convolutional networks for predicting outcomes in ovarian cancer receiving neoadjuvant chemotherapy. npj Precis. Onc. 10, 157 (2026). https://doi.org/10.1038/s41698-026-01346-9
Schlüsselwörter: Ovarialkarzinom, neoadjuvante Chemotherapie, Graph-Neuronale Netzwerke, Radiomics, Therapieprognose