Clear Sky Science · sv
Identifiering och klusteranalys av läkemedelsreaktiva tidsvarierande gener via högfrekvent longitudinell RNA-sekvensering
Varför det är viktigt att bevaka gener över tid
När vi tar ett läkemedel svarar kroppen inte i ett enda ögonblick. Celler anpassar sig, försvarar sig, reparerar skador och återhämtar sig över timmar och dagar. Ändå tittar de flesta laboratorietester bara före och efter behandling och missar det som händer däremellan. Denna studie visar att genom att ta frekventa små blodprover och avläsa genaktivitet dag för dag kan forskare upptäcka dolda vågor av svar på läkemedel som annars skulle vara osynliga. Arbetet fokuserar på läkemedel som belastar levern hos råttor, men tillvägagångssättet pekar mot mer precis, tidsmedveten medicin för människor.
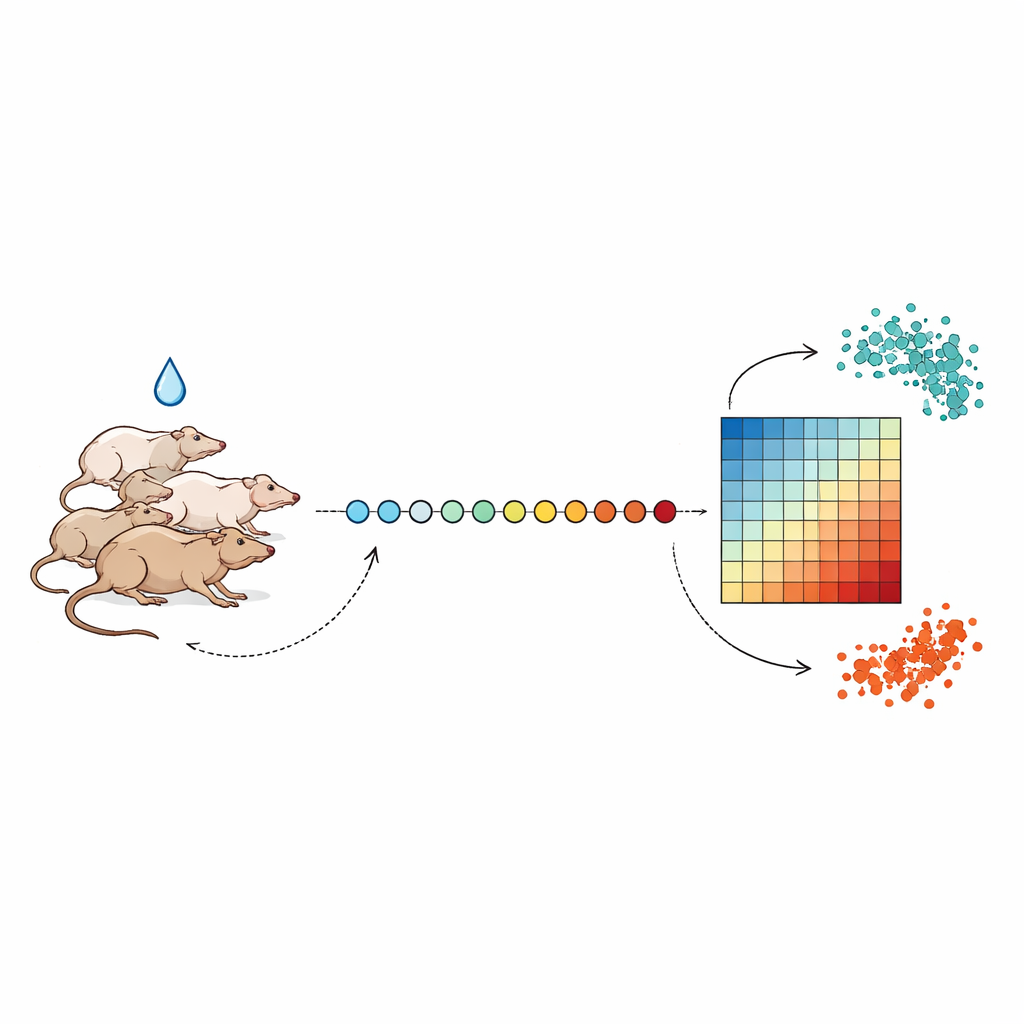
Dagliga ögonblicksbilder av kroppens reaktion
Forskarna följde grupper av råttor i upp till tre veckor och tog mycket små mängder blod nästan samma tid varje dag för att undvika normala dygnsvariationer i biologin. Efter några dagars baslinjemätningar gavs djuren en enkel dos av ett av flera levertoxiska ämnen, inklusive antibiotikan tetracyklin och tuberkulosläkemedlet isoniazid, i olika styrkor. Från varje blodprov extraherade teamet RNA — budbärarmolekyler som speglar vilka gener som är på- eller avstängda — och använde höggenomströmmande sekvensering för att mäta aktiviteten hos tusentals gener samtidigt. Genom att rada upp dessa mätningar över dagarna kunde de se hur genaktiviteten avvek från en frisk baslinje och sedan, i de flesta fall, gradvis återvände.
Att hitta gener som förändras över tid, inte bara i medelvärde
Standardanalyser av sådana data jämför vanligtvis en tidpunkt före behandling med en tidpunkt efteråt och flaggar gener med stora genomsnittliga förändringar som "olika." Men det ögonblicksbildsperspektivet kan missa gener som kortvarigt skjuter i höjden eller dalar, eller som svarar senare och sedan normaliseras. För att hantera detta använde författarna ett ramverk för att identifiera "tidsvarierande gener" — gener vars aktivitet fluktuerar på ett meningsfullt sätt under behandlingsförloppet, även om start- och slutnivåerna ser lika ut. Genom att poängsätta hur starkt varje gens nivåer steg och föll över dagarna och filtrera bort rutinmässigt brus, som milda effekter av upprepade blodtagningar, upptäckte de tusentals gener vars beteende innehöll rik tidsinformation om läkemedelsresponsen.
Mönster av tidig varning, långvarig stress och sen återhämtning
När teamet grupperade dessa tidsvarierande gener efter hur deras aktivitet förändrades efter en hög dos tetracyklin framträdde tydliga mönster. Vissa gener sköt snabbt upp och återgick inom några dagar och fungerade som tidiga varningsklockor. Andra steg upp och förblev höga genom läkemedlets topppåverkan och återspeglade långvarig stress på proteintillverkning och andra kärnprocesser i cellen. En tredje grupp slog på eller av senare, vilket markerade långsammare reparations- och städfaser. Liknande, om än inte identiska, tidmönster dök upp med andra levertoxiska läkemedel. Genom att koppla varje mönster till kända cellulära funktioner — såsom immunförsvar, avfallshantering eller DNA-reparation — kunde författarna skissera en stegvis berättelse om hur levern först känner av skada, sedan anpassar sig och slutligen försöker läka.
Delade varningssignaler och läkemedelsspecifika fingeravtryck
Över fyra olika giftiga föreningar katalogiserade forskarna mer än 4 000 unika tidsvarierande gener. Endast 186 av dem förändrades på ett samordnat sätt för varje läkemedel och bildade en delad "kärn"-signatur för leverstress som var särskilt rik på gener som hanterar järn och en form av celldöd kallad ferroptos. Resten var läkemedelsspecifika och betonade att olika kemikalier skadar celler via skilda vägar och utlöser olika återhämtningsprogram. Teamet undersökte också hur gensvaren berodde på dos. Vissa gener reagerade även vid de lägsta läkemedelsnivåerna, vilket gör dem till lovande tidiga varningsmarkörer, medan andra svarade endast vid de starkaste doserna och pekade på vägar som aktiveras när skadan blir allvarlig. Dessa doströsklar kan hjälpa förklara varför samma behandling kan ge lindrig obehagskänsla hos en individ och allvarlig skada hos en annan.
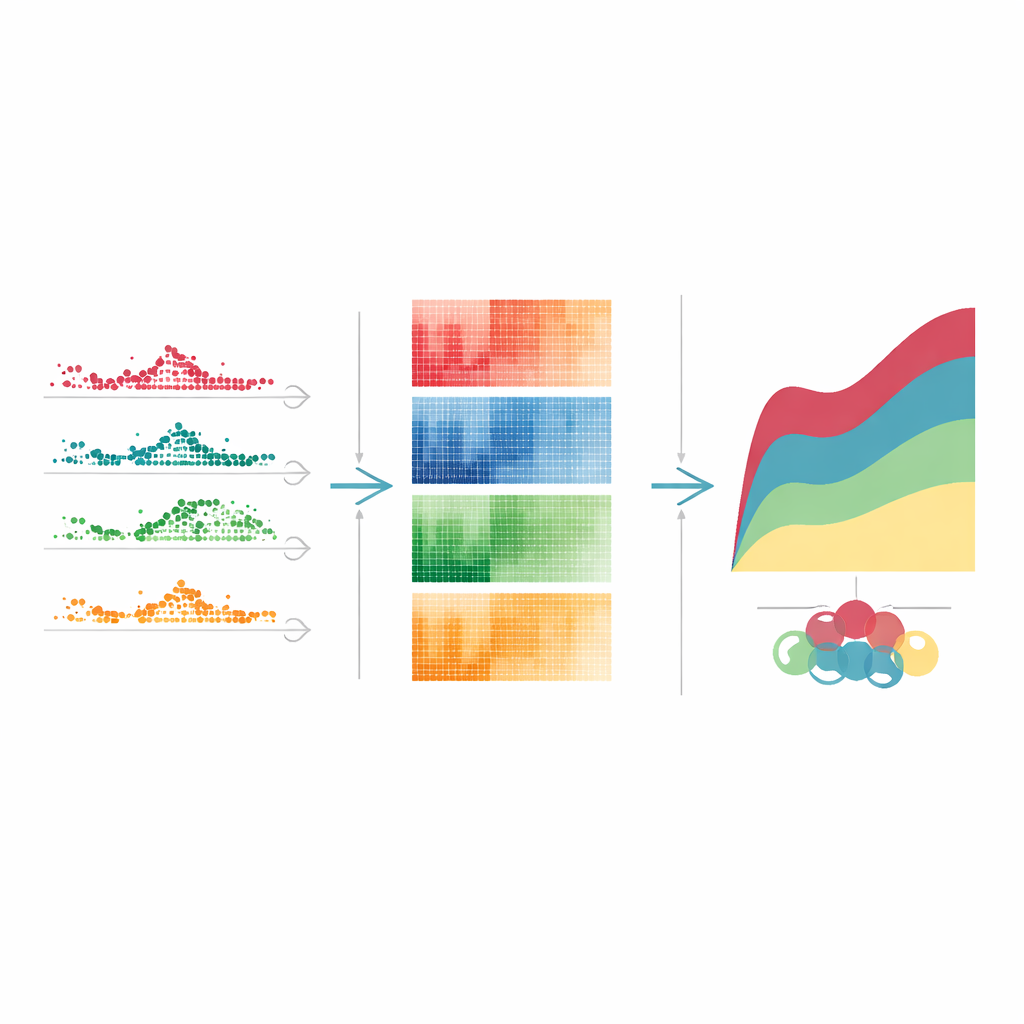
Vad detta innebär för framtida behandlingar
Sammantaget visar studien att bevakning av genaktivitet över tid kan avslöja subtila, snabba eller fördröjda svar som platta, enstaka tidpunkts-tester förbiser. Författarna menar att dessa tidsvarierande gener erbjuder ett känsligare sätt att skilja direkta läkemedelseffekter från kroppens egna försök att anpassa sig och reparera, samt att särskilja säkra exponeringsnivåer från farliga. Även om arbetet utfördes på råttor och fokuserade på levertoxiska föreningar, kan den underliggande idén — tät, upprepad provtagning kombinerad med smart analys — tillämpas brett. När sekvensering blir billigare och dataanalys kraftfullare kan sådan longitudinell molekylär övervakning hjälpa till att skräddarsy dosering, upptäcka biverkningar tidigare och bättre anpassa behandlingar till varje individs unika svarsmönster.
Citering: Jiang, Q., Weng, X., Chai, Y. et al. Identification and clustering analysis of drug-responsive temporally varying genes through high-frequency longitudinal RNA sequencing. Sci Rep 16, 14143 (2026). https://doi.org/10.1038/s41598-026-44560-y
Nyckelord: longitudinell RNA-sekvensering, läkemedelsinducerad leverskada, genuttrycksdynamik, toxicologiska biomarkörer, precisionfarmakologi