Clear Sky Science · ar
تحديد وتحليل تجميع الجينات المتغيرة زمنياً المستجيبة للأدوية عبر تسلسل الحمض النووي الريبي الطولي عالي التكرار
لماذا يهم مراقبة الجينات مع مرور الوقت
عندما نتناول دواءً، لا يستجيب جسدنا فوراً دفعة واحدة. تتكيف الخلايا، تكافح، تصلح الأضرار وتتعافى على مدار ساعات وأيام. ومع ذلك، تركز معظم الاختبارات المخبرية على قبل وبعد العلاج فقط، مما يفوّت ما يحدث بين هذين النقطتين. تُظهر هذه الدراسة أنه من خلال أخذ عينات دم صغيرة متكررة وقياس نشاط الجينات يومًا بيوم، يمكن للباحثين كشف موجات استجابة مخفية للأدوية قد تظل غير مرئية خلاف ذلك. ركزت الدراسة على أدوية تجهد الكبد في الفئران، لكن المنهجية تشير إلى طب أكثر دقة وواعٍ بالزمن لدى البشر.
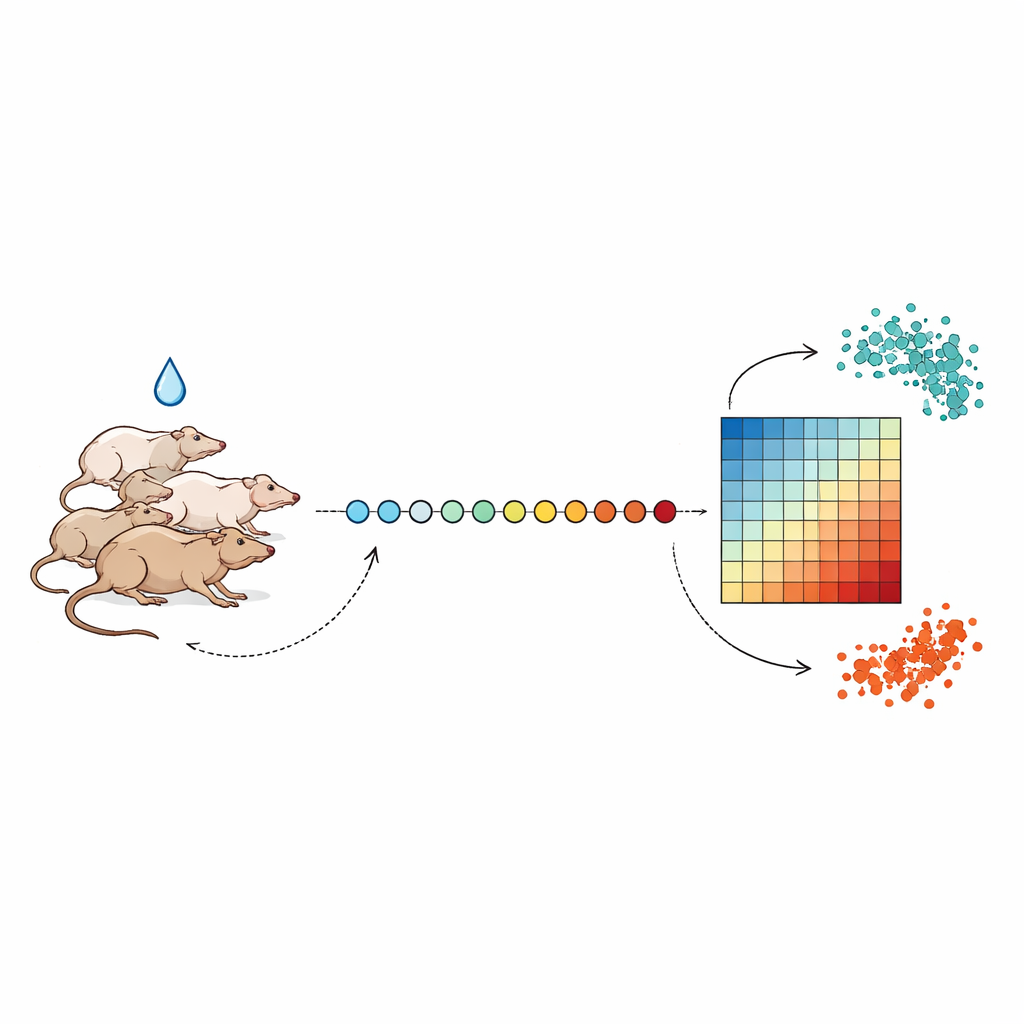
التقاط لقطات يومية لرد فعل الجسم
تتبّع الباحثون مجموعات من الفئران لمدة تصل إلى ثلاثة أسابيع، وأخذوا كمية صغيرة جدًا من الدم تقريبًا في نفس الوقت كل يوم لتفادي التقلبات الطبيعية المرتبطة بدورة الليل والنهار. بعد بضعة أيام من أخذ العينات الأساسية، تلقّت الحيوانات جرعة واحدة من أحد المركبات المسببة لتسمم الكبد، بما في ذلك المضاد الحيوي التتراسيكلين ودواء السل أيزونيازيد، بتركيزات مختلفة. من كل عينة دم، استخرج الفريق الحمض النووي الريبي—جزيئات الرسول التي تعكس أي الجينات قيد التشغيل أو الإيقاف—واستخدموا تسلسلًا عالي الإنتاجية لقياس نشاط آلاف الجينات مرة واحدة. بترتيب هذه القياسات على مدى الأيام، استطاعوا متابعة كيف ابتعدت نشاطات الجينات عن الخط الأساس الصحي ثم، في معظم الحالات، عادت تدريجيًا.
إيجاد الجينات التي تتغير مع الزمن، لا فقط في المتوسط
تحليلات البيانات التقليدية عادةً ما تقارن نقطة زمنية واحدة قبل العلاج بأخرى بعده، معلمة الجينات ذات التغيرات المتوسطة الكبيرة بأنها «مختلفة». لكن رؤية اللقطة الواحدة هذه قد تفوّت الجينات التي ترتفع أو تنخفض مؤقتًا، أو التي تستجيب في وقت لاحق ثم تعود إلى وضعها الطبيعي. لمواجهة ذلك، استخدم المؤلفون إطارًا لتحديد «الجينات المتغيرة زمنياً» — الجينات التي يتقلب نشاطها بطريقة ذات مغزى على مدار فترة العلاج، حتى لو بدا أن مستوياتها في البداية والنهاية متشابهة. من خلال تسجيل مدى ارتفاع وهبوط مستويات كل جين عبر الأيام، وتصفيتهم للضوضاء الروتينية مثل التأثيرات الخفيفة للنزف المتكرر، كشفوا عن آلاف الجينات التي حملت معلومات زمنية غنية حول استجابة الدواء.
أنماط الإنذار المبكر، والإجهاد المستمر، والتعافي المتأخر
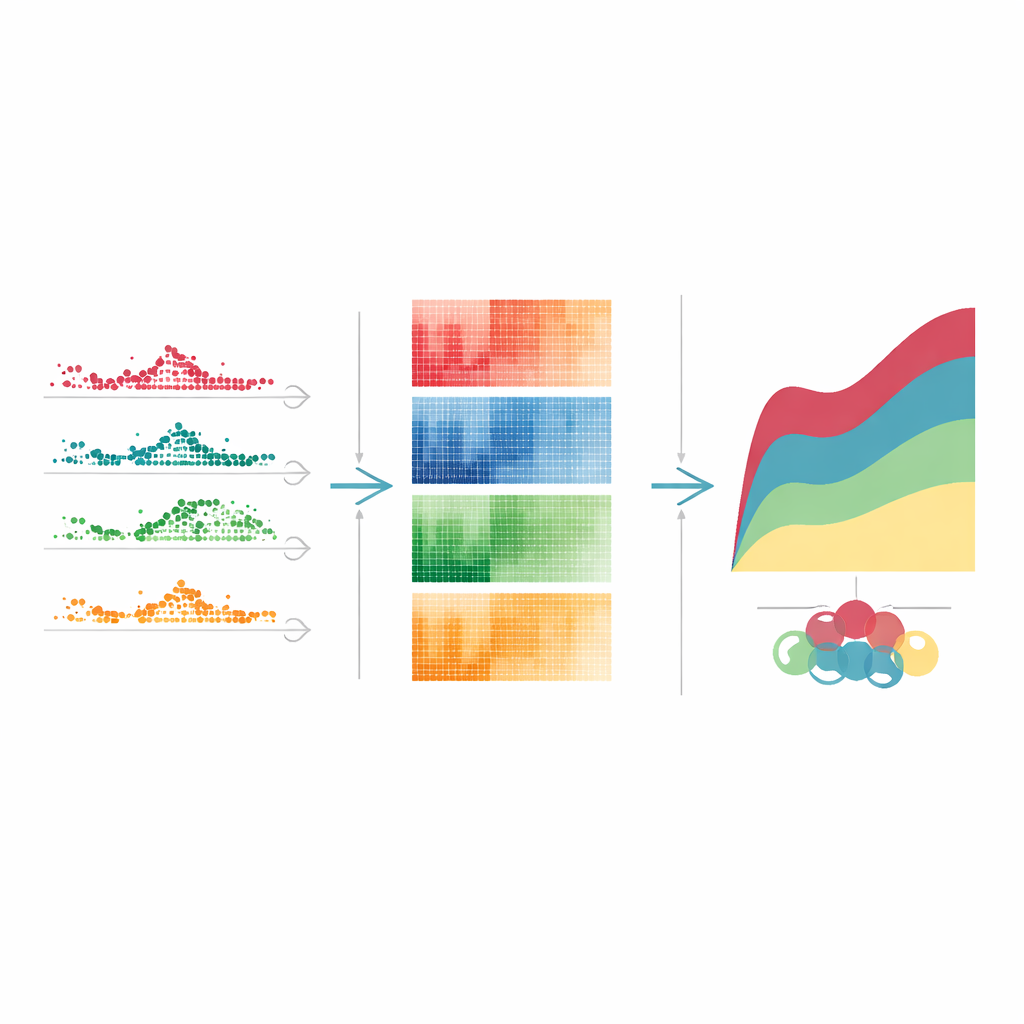
عندما جمع الفريق هذه الجينات المتغيرة زمنياً بحسب كيفية تغير نشاطها بعد جرعة عالية من التتراسيكلين، ظهرت أنماط واضحة. قفزت بعض الجينات بسرعة ثم استقرت خلال أيام قليلة، فعملت كأجراس إنذار مبكرة. ارتفع آخرون وظلوا على مستويات مرتفعة خلال ذروة تأثير الدواء، مما يعكس إجهادًا مستمرًا لعمليات تصنيع البروتين وغيرها من العمليات الخلوية الأساسية. مجموعة ثالثة اشتغلت أو انطفأت في وقت لاحق، مشيرة إلى مراحل إصلاح وتنظيف أبطأ. ظهرت أنماط زمنية مشابهة، وإن لم تكن متطابقة، مع أدوية أخرى سامة للكبد. من خلال ربط كل نمط بالمهام الخلوية المعروفة—مثل الدفاع المناعي، والتخلص من النفايات، أو إصلاح الحمض النووي—تمكن المؤلفون من رسم قصة مرحلية لكيفية شعور الكبد بالإصابة أولًا، ثم تكيفه، وفي النهاية محاولته للشفاء.
علامات تحذير مشتركة وبصمات خاصة بكل دواء
عند النظر عبر أربعة مركبات سامة مختلفة، قام الباحثون بتصنيف أكثر من 4000 جين فريد متغير زمنياً. تغير 186 منهم فقط بطريقة منسقة لكل دواء، مكوّنين توقيعًا «أساسيًا» مشتركًا لإجهاد الكبد كان غنيًا بشكل خاص بالجينات المتحكمة بالحديد وبنوع من موت الخلايا يُدعى الفيروبتوزيس. أما الباقي فكان خاصًا بكل دواء، مما يُبرز أن المواد الكيميائية المختلفة تُحدث إصابات بطرق مميزة وتستحث برامج تعافٍ مختلفة. كما فحص الفريق كيف اعتمدت استجابات الجينات على الجرعة. تفاعل بعض الجينات حتى عند أدنى مستويات الدواء، مما يجعلها مؤشرات واعدة للإنذار المبكر، بينما استجابت أخرى فقط للجرعات الأقوى، مشيرة إلى مسارات تُفعّل عند تفاقم الضرر. قد تساعد هذه العتبات الجرعية في تفسير لماذا يمكن أن يؤدي نفس العلاج إلى إزعاج طفيف لدى شخص وجَدْرَ ضرر خطير لدى آخر.
ماذا يعني هذا للعلاجات المستقبلية
تُظهر الدراسة مجتمعة أن متابعة نشاط الجينات عبر الزمن يمكن أن تكشف استجابات دقيقة، سريعة أو متأخرة قد تغفلها الاختبارات المسطحة التي تأخذ نقطة زمنية واحدة فقط. يجادل المؤلفون بأن هذه الجينات المتغيرة زمنياً تقدم وسيلة أكثر حساسية لتمييز التأثيرات المباشرة للأدوية عن محاولات الجسم للتكيف والإصلاح، وللفصل بين مستويات التعرض الآمنة وتلك الخطرة. وعلى الرغم من أن العمل أُجري في فئران وركز على مركبات سامة للكبد، فإن الفكرة الأساسية—أخذ عينات متكررة وكثيفة مع تحليل ذكي—قابلة للتطبيق على نطاق أوسع. ومع انخفاض تكلفة التسلسل وتقوى أدوات تحليل البيانات، قد تساعد مثل هذه المتابعات الجزيئية الطولية في تخصيص جرعات الأدوية، واكتشاف الآثار الجانبية مبكرًا، ومطابقة العلاجات بشكل أفضل مع نمط استجابة كل فرد.
الاستشهاد: Jiang, Q., Weng, X., Chai, Y. et al. Identification and clustering analysis of drug-responsive temporally varying genes through high-frequency longitudinal RNA sequencing. Sci Rep 16, 14143 (2026). https://doi.org/10.1038/s41598-026-44560-y
الكلمات المفتاحية: تسلسل الحمض النووي الريبي الطولي, تلف الكبد الناجم عن الأدوية, ديناميكيات التعبير الجيني, مؤشرات السمية الحيوية, الصيدلة الدقيقة