Clear Sky Science · nl
Identificatie en clusteranalyse van medicijnen-responsieve, temporeel variërende genen via hoogfrequente longitudinale RNA-sequencing
Waarom het volgen van genen in de tijd ertoe doet
Als we een geneesmiddel innemen, reageert ons lichaam niet in één keer. Cellen passen zich aan, verzetten zich, repareren schade en herstellen zich over uren en dagen. Toch kijken de meeste laboratoriumtests alleen voor en na de behandeling, waardoor het gebeuren daartussen ontbreekt. Deze studie toont aan dat onderzoekers door frequente, kleine bloedafnames en dagelijkse uitlezing van genactiviteit verborgen golven van reactie op medicijnen kunnen blootleggen die anders onzichtbaar blijven. Het werk richt zich op middelen die de lever belasten bij ratten, maar de aanpak wijst in de richting van preciezere, tijdsbewuste geneeskunde voor mensen.
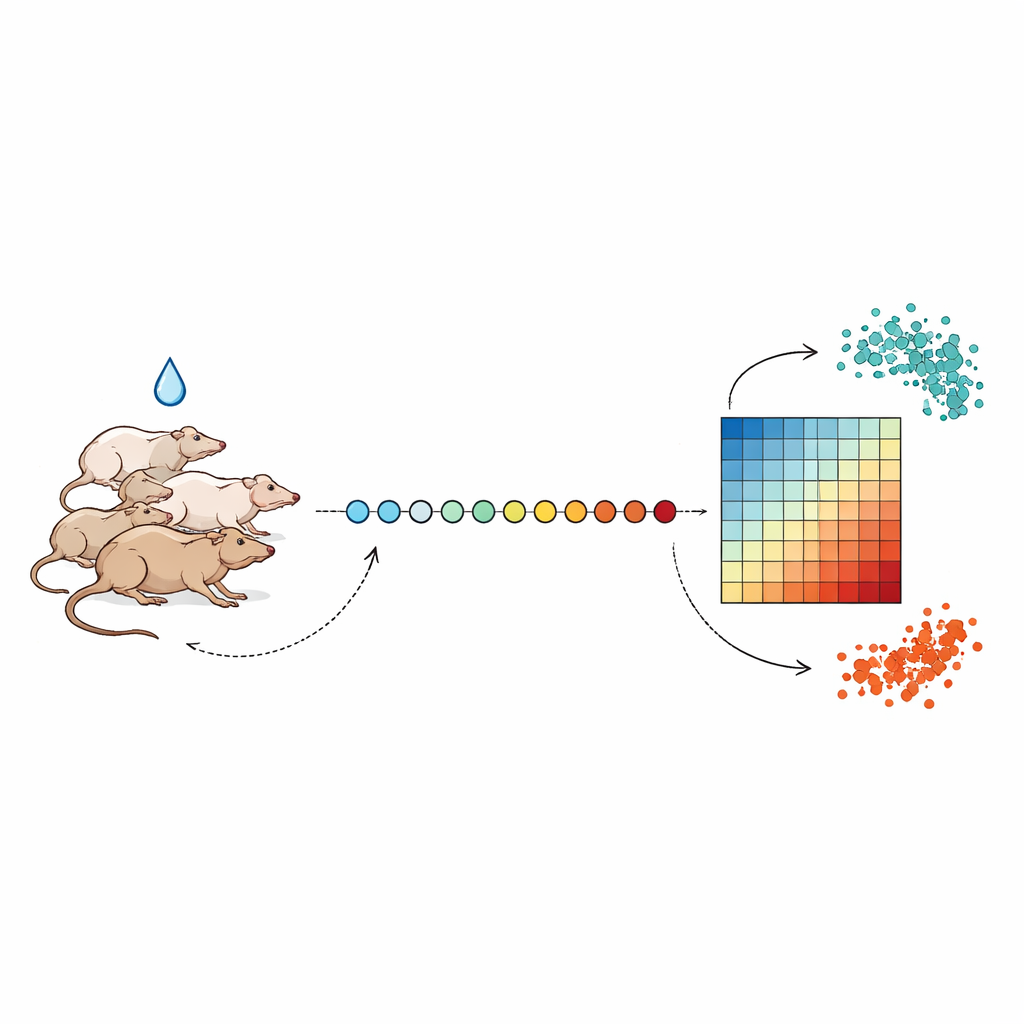
Dagelijkse snapshots van de reactie van het lichaam
De onderzoekers volgden groepen ratten tot drie weken en namen elke dag vrijwel op hetzelfde tijdstip een zeer kleine hoeveelheid bloed om normale dag–nachtwisselingen te vermijden. Na enkele dagen van basislijnmonsters kregen de dieren één dosis van een van meerdere levertoxische verbindingen, waaronder het antibioticum tetracycline en het tuberculosemiddel isoniazide, in verschillende sterktes. Uit elk bloedmonster haalde het team RNA—de boodschappermoleculen die weerspiegelen welke genen aan- of uitgezet zijn—en gebruikte hoogdoorloopssequencing om de activiteit van duizenden genen tegelijk te meten. Door deze metingen over de dagen uit te lijnen, konden ze zien hoe genactiviteit afweek van een gezonde basislijn en vervolgens in de meeste gevallen geleidelijk terugkeerde.
Genen vinden die met de tijd veranderen, niet alleen gemiddeld
Standaardanalyses van zulke gegevens vergelijken meestal één tijdpunt vóór behandeling met één tijdpunt erna en markeren genen met grote gemiddelde veranderingen als “verschillend”. Maar dat momentopnameperspectief kan genen missen die kortstondig pieken of dalen, of die later reageren en dan normaliseren. Om dit aan te pakken gebruikten de auteurs een kader om “temporeel variërende genen” te identificeren—genen waarvan de activiteit op betekenisvolle wijze fluctueert gedurende de behandeling, ook als begin- en eindniveaus vergelijkbaar lijken. Door te scoren hoe sterk de niveaus van elk gen over de dagen stegen en daalden, en routine-ruis zoals milde effecten van herhaaldelijk bloeden eruit te filteren, ontdekten ze duizenden genen met rijke timinginformatie over de medicijnrespons.
Patronen van vroege alarmen, aanhoudende stress en late herstel
Toen het team deze tijdsvariërende genen groepeerde op basis van hoe hun activiteit veranderde na een hoge dosis tetracycline, kwamen duidelijke patronen naar voren. Sommige genen schoten snel omhoog en zakten binnen een paar dagen weer terug, als vroege alarmbellen. Andere namen toe en bleven hoog tijdens de piek van de medicijnimpact, wat wijst op aanhoudende stress van eiwitsynthese en andere kernprocessen in de cel. Een derde groep schakelde later aan of uit en markeerde langzamere herstel- en schoonmaakfasen. Vergelijkbare, zij het niet identieke, timingpatronen verschenen bij andere levertoxische middelen. Door elk patroon te koppelen aan bekende cellulaire taken—zoals immuunverdediging, afvalverwerking of DNA-reparatie—kon het team een stapsgewijs verhaal schetsen van hoe de lever eerst schade waarneemt, zich daarna aanpast en uiteindelijk probeert te genezen.
Gedeelde waarschuwingssignalen en medicijn-specifieke vingerafdrukken
Over vier verschillende toxische verbindingen heen kaarteerden de onderzoekers meer dan 4.000 unieke temporeel variërende genen. Slechts 186 daarvan veranderden op gecoördineerde wijze bij elk medicijn en vormden een gedeelde “kern”handtekening van leverstress die vooral rijk was aan genen die ijzer verwerken en aan een vorm van celdood genaamd ferroptose. De rest was medicijn-specifiek, wat benadrukt dat verschillende chemicaliën cellen via uiteenlopende routes beschadigen en verschillende herstelprogramma’s activeren. Het team onderzocht ook hoe genreacties afhankelijk waren van de dosis. Sommige genen reageerden al bij de laagste medicijnniveaus en zijn veelbelovend als vroege waarschuwingsmarkers, terwijl andere alleen op de sterkste dosissen antwoordden en wijzen op paden die in werking treden bij ernstige schade. Deze drempels voor dosisrespons kunnen helpen verklaren waarom dezelfde behandeling bij de ene persoon milde klachten veroorzaakt en bij een andere ernstig letsel.
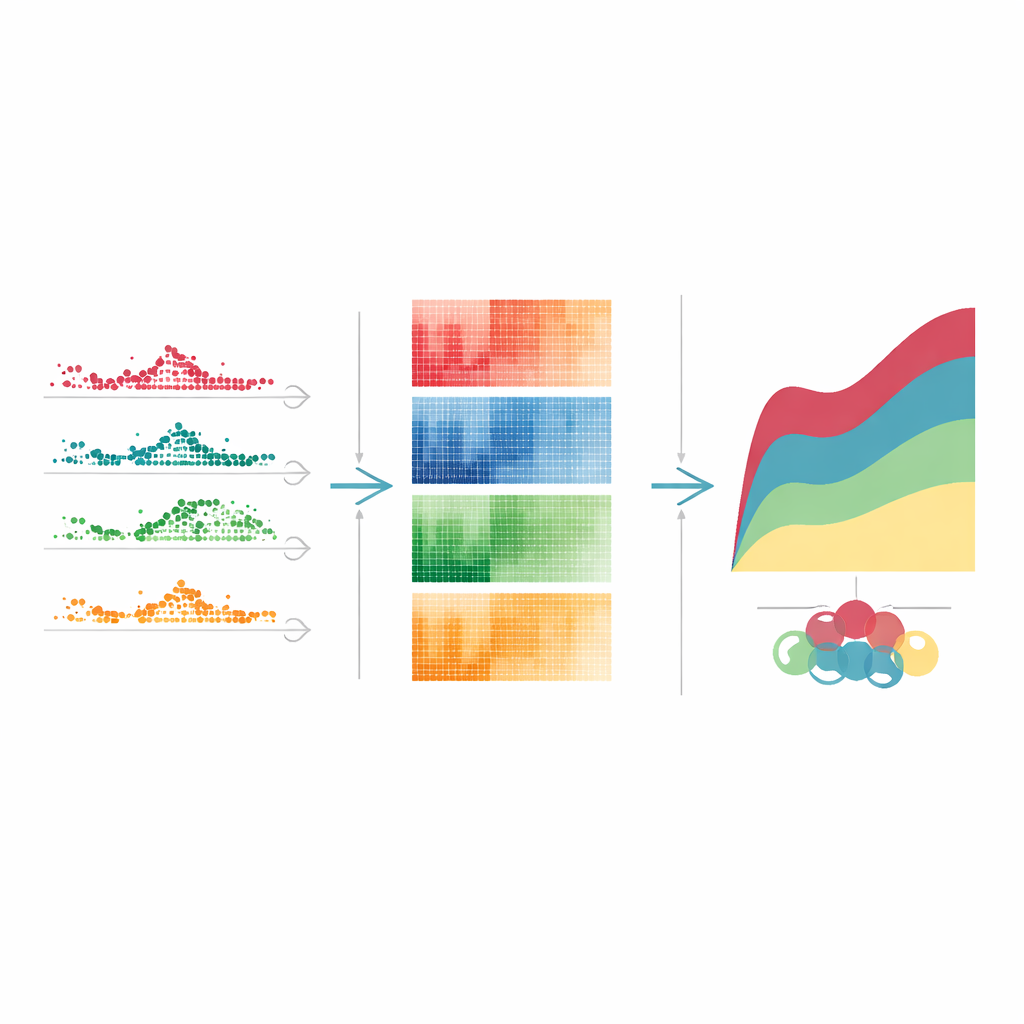
Wat dit betekent voor toekomstige behandelingen
Samengevat laat de studie zien dat het volgen van genactiviteit in de tijd subtiele, snelle of vertraagde reacties kan onthullen die platte, enkelvoudige tijdpunttests over het hoofd zien. De auteurs betogen dat deze temporeel variërende genen een gevoeliger manier bieden om directe medicijneffecten te onderscheiden van de eigen aanpassings- en herstelpogingen van het lichaam, en om veilige blootstellingsniveaus van gevaarlijke te scheiden. Hoewel het werk bij ratten werd uitgevoerd en zich richtte op levertoxische verbindingen, is het onderliggende idee—dichte, herhaalde bemonstering gecombineerd met slimme analyse—breed toepasbaar. Naarmate sequencing goedkoper wordt en data-analyse krachtiger, kan dergelijke longitudinale moleculaire monitoring helpen bij het afstemmen van doseringen, het eerder opsporen van bijwerkingen en het beter matchen van behandelingen op ieders unieke responsprofiel.
Bronvermelding: Jiang, Q., Weng, X., Chai, Y. et al. Identification and clustering analysis of drug-responsive temporally varying genes through high-frequency longitudinal RNA sequencing. Sci Rep 16, 14143 (2026). https://doi.org/10.1038/s41598-026-44560-y
Trefwoorden: longitudinale RNA-sequencing, door medicijnen veroorzaakte leverschade, dynamiek van genexpressie, biomerkers in toxicologie, precisie farmacologie