Clear Sky Science · sv
Antisense-oligonukleotidmedierad nedregleringsbehandling hos två spädbarn med svår KCNT1-epileptisk encefalopati
Varför denna studie är viktig för familjer
Några av de mest förödande epilepsierna börjar under de första levnadsdagarna och svarar inte på vanliga läkemedel, vilket lämnar spädbarn med ständiga anfall och djup utvecklingsstörning. Denna studie undersöker en starkt individualiserad form av genmedicin — ett antisense-oligonukleotidläkemedel — utformat för att dämpa aktiviteten hos en enda överaktiv hjärnkanal hos två små flickor. Den ger en inblick i hur precisionsbehandlingar kan tygla annars obehandlingsbara anfall, samtidigt som den blottlägger allvarliga risker som måste förstås innan sådana metoder blir allmänt använda.
Problemet med obevekliga tidiga anfall
Epilepsi i spädbarnsåldern med migrerande fokala anfall är ett sällsynt men extremt allvarligt tillstånd. Bebisar får anfall inom timmar eller dagar efter födseln och upplever ofta dussintals varje dag trots försök med många antiepileptika. Hos ungefär hälften av dessa barn är orsaken en ny mutation i en gen kallad KCNT1, som kodar för en kanal som släpper igenom kaliumjoner genom nervcellernas membran. Den specifika mutationen som studerats här, kallad p.R474H, gör kanalerna mycket mer aktiva än normalt och pressar nätverk av neuroner in i ett ständigt överexciterat tillstånd. Dessa barn visar vanligtvis nästan ingen utvecklingsframgång, har hög risk för tidig död och saknar för närvarande pålitligt effektiva behandlingar.
En genriktad medicin framtagen i laboratoriet
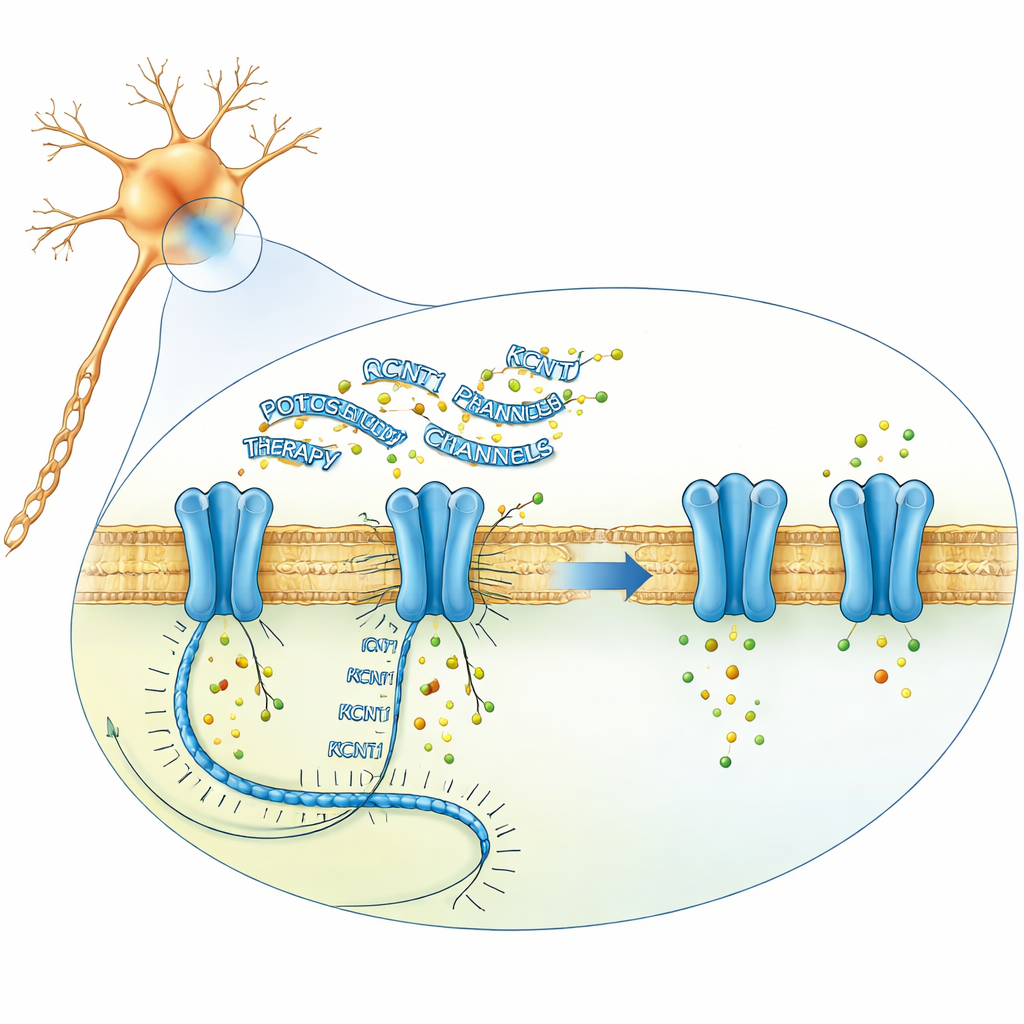
Forskargruppen gav sig i kast med att minska mängden felaktigt KCNT1-meddelande i neuroner med hjälp av antisense-oligonukleotider: korta, kemiskt modifierade kedjor av genetiskt material som kan binda till en utvald RNA och utlösa dess nedbrytning. Med start från mer än 250 kandidatsekvenser snävade de successivt ner designen i odlade mänskliga nervliknande celler, i neuroner framodlade från patienters stamceller och i musceller. Deras ledande förening, senare kallad valeriasen, sänkte kraftigt KCNT1-RNA och protein-nivåer i patientderiverade neuroner och i en musmodell som bar motsvarande sjukdomsmutation, utan att brett störa andra gener. Elektrofysiologiska experiment visade att läkemedlet normaliserade de abnormt stora kaliumströmmarna och förde de mutanta neuronernas fyrmönster mycket närmare friska cellers, vilket antyder att en dämpning av kanalen kan korrigera den underliggande elektriska obalansen.
Testning i djurmodeller före mänsklig användning
Innan man övervägde användning hos barn utvärderade forskarna läkemedlet i flera gnagarmodeller. I möss som konstruerats för att uttrycka mänskligt KCNT1 minskade injektioner i hjärnvätskan både mus- och mänskligt KCNT1-RNA i dosberoende grad. I en separat musstam som naturligt utvecklar svåra anfall, neurokognitiva problem och tidig död på grund av en annan KCNT1-mutation förlängde behandling med ledande läkemedel medianlivslängden från ungefär sex veckor till flera månader och förbättrade enkla beteendemått som bo-byggande. Studier i råttor med upprepade spinalinjektioner hjälpte till att fastställa doser som föreföll allmänt tolererbara baserat på beteende, neurologiska undersökningar och vävnadsanalys, samtidigt som man ändå uppnådde betydande KCNT1-nedreglering i hjärnregioner. Dessa fynd stödde en försiktig fortsättning till nära övervakad användning hos patienter inom ramen för ett särskilt utredningsprotokoll.
Tidig erfarenhet hos två barn
Två treåriga flickor med KCNT1 p.R474H-mutation, båda med anfall från nyföddhetsperioden och minimal utvecklingsframgång, fick stigande doser av valeriasen levererade via lumbalpunktion in i vätskan runt ryggmärgen. Hos båda minskade antalet anfall som familjerna registrerade och som bekräftades av upprepade EEG-undersökningar avsevärt efter flera doser, och ett barn visade förbättringar i huvudkontroll, sväljning och förmåga att själv trösta sig. Läkemedelsnivåerna i ryggmärgsvätska och blod uppträdde som förväntat utifrån djurstudierna. Efter flera månaders behandling med relativt höga kumulativa doser utvecklade båda barnen emellertid en allvarlig komplikation: progressiv förstoring av hjärnans vätskefyllda rum med förhöjt tryck, en form av hydrocefalus. En familj valde palliativ vård, och barnet avled senare; det andra behövde en kirurgiskt implanterad shunt för att dränera överflödig vätska.
Balansera löfte och risk
Inför denna oväntade biverkning pausade teamet doseringen och gick noggrant igenom djur- och laboratoriedata. Hydrocefalus hade inte observerats i musmodeller utan KCNT1 eller hos möss med sjukdomsmutationer, och genetiska undersökningar tyder på att människor kan tolerera att förlora en kopia av KCNT1, vilket talar emot enkel målinriktad toxicitet. Några andra antisense-läkemedel som används vid neurologiska sjukdomar har kopplats till sällsynta fall av förhöjt hjärntryck eller ventrikelutvidgning, särskilt vid högre doser, vilket antyder att problemet kan bero på hur vissa föreningar interagerar med hjärnans vätskeproducerande och vätskeavledande strukturer. Efter ett tvåårigt uppehåll återupptog den andra patienten behandlingen enligt ett reviderat, lägre doschema med extra MR-undersökningar och tryckkontroller; under detta försiktiga protokoll upplevde hon återigen ungefär två tredjedels minskning av anfallen utan ny vätskeansamling hittills.
Vad detta innebär framöver
För familjer och kliniker som står inför katastrofala genetiska epilepsier visar detta arbete att direkt dämpning av en överaktiv jonkanal med ett skräddarsytt genläkemedel verkligen kan minska anfall, även hos barn som misslyckats med varje konventionellt läkemedel. Samtidigt understryker framkomsten av hydrocefalus hos båda behandlade patienterna att så kraftfulla behandlingar kan medföra allvarliga, fortfarande dåligt förstådda risker. Författarna drar slutsatsen att hämning av KCNT1-kanalen är en giltig och lovande strategi, men att dosering måste ske gradvis, med noggrann hjärnavbildning och klinisk övervakning inbyggd i framtida prövningar. Mer allmänt framhäver studien både den transformerande potentialen och det etiska ansvar som följer med att utforma individualiserade genläkemedel för några av de svårast sjuka patienterna.
Citering: Nakayama, T., El Achkar, C.M., Burbano, L.E. et al. Antisense oligonucleotide-mediated knockdown therapy in two infants with severe KCNT1 epileptic encephalopathy. Nat Med 32, 1411–1420 (2026). https://doi.org/10.1038/s41591-026-04314-9
Nyckelord: KCNT1-epilepsi, antisense-oligonukleotid, precisionmedicin, spädbarnsseizurer, hydrocefalus