Clear Sky Science · pt
Terapia de redução mediada por oligonucleotídeo antisenso em duas lactentes com encefalopatia epiléptica grave por KCNT1
Por que este estudo importa para famílias
Algumas das epilepsias mais devastadoras começam nos primeiros dias de vida e não respondem aos medicamentos padrão, deixando lactentes com convulsões constantes e deficiência de desenvolvimento profunda. Este estudo explora um tipo altamente personalizado de medicina genética — um fármaco baseado em oligonucleotídeo antisenso — projetado para reduzir a atividade de um único canal cerebral hiperativo em duas meninas pequenas. Ele oferece um vislumbre de como terapias de precisão podem conter convulsões até então intratáveis, ao mesmo tempo em que revela riscos graves que precisam ser compreendidos antes que essas abordagens sejam amplamente usadas.
O problema das convulsões implacáveis no início da vida
A epilepsia da infância com convulsões focais migratórias é uma condição rara, mas extremamente grave. Bebês desenvolvem convulsões nas primeiras horas ou dias após o nascimento, frequentemente vivenciando dezenas por dia apesar do uso de muitos anticonvulsivantes. Em cerca de metade dessas crianças, a causa é uma mutação nova no gene chamado KCNT1, que codifica um canal que permite a passagem de íons potássio através das membranas das células cerebrais. A mutação específica estudada aqui, chamada p.R474H, torna os canais muito mais ativos que o normal, empurrando redes de neurônios a um estado de hiperexcitação contínua. Essas crianças normalmente apresentam quase nenhum progresso no desenvolvimento, têm alto risco de morte precoce e atualmente não dispõem de tratamentos comprovadamente eficazes.
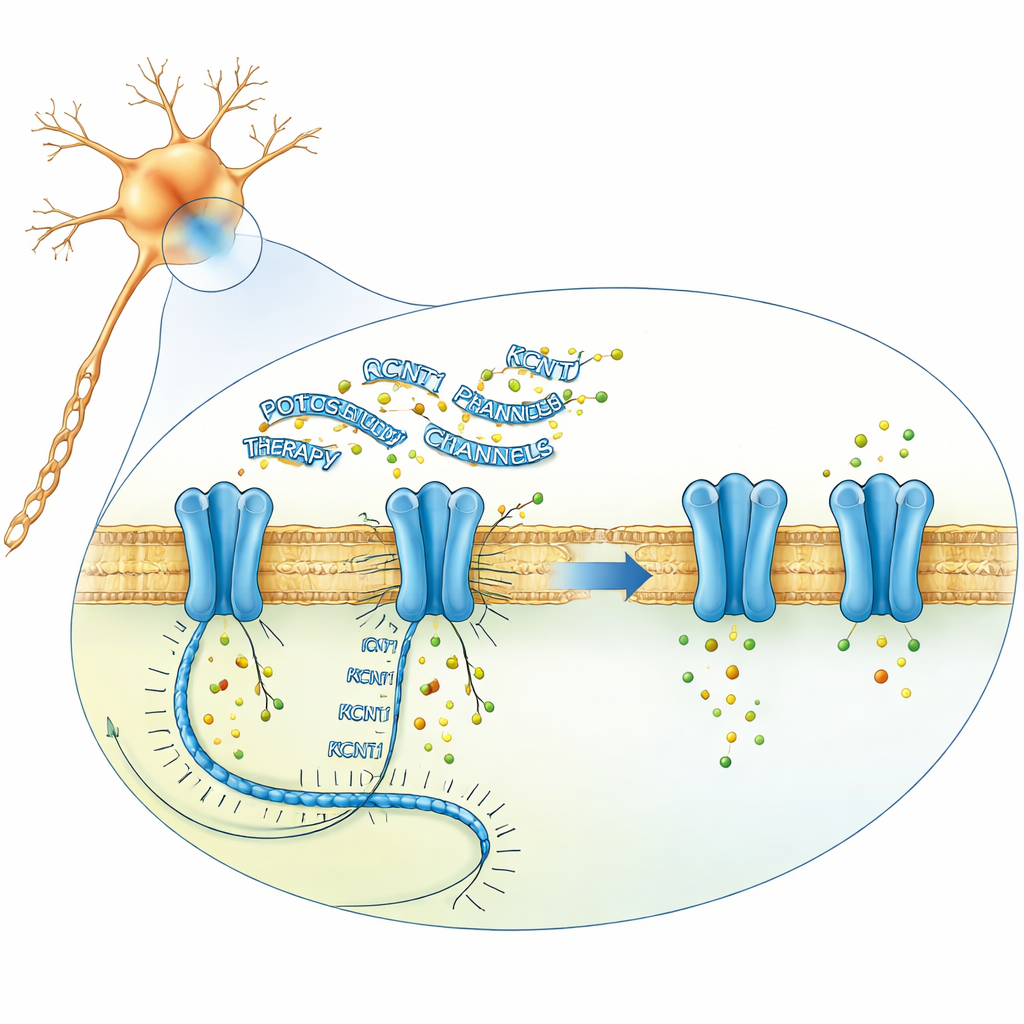
Um fármaco direcionado ao gene feito em laboratório
A equipe de pesquisa procurou reduzir a quantidade de mensageiro KCNT1 defeituoso dentro dos neurônios usando oligonucleotídeos antisenso: cadeias curtas de material genético quimicamente modificado que podem se ligar a um RNA escolhido e disparar sua destruição. Partindo de mais de 250 sequências candidatas, eles restringiram progressivamente os desenhos em células humanas do tipo nervoso em cultura, em neurônios derivados de células-tronco de pacientes e em células de camundongos. O composto líder, posteriormente chamado valeriasen, reduziu acentuadamente os níveis de RNA e proteína de KCNT1 em neurônios derivados de pacientes e em uma linhagem de camundongo que carregava a mutação correspondente da doença, sem perturbar amplamente outros genes. Experimentos eletrofisiológicos mostraram que o fármaco normalizou as correntes de potássio anormalmente grandes e aproximou os padrões de disparo dos neurônios mutantes aos dos neurônios saudáveis, sugerindo que reduzir a atividade do canal poderia corrigir o desequilíbrio elétrico subjacente.
Testes em modelos animais antes de humanos
Antes de considerar o uso em crianças, os pesquisadores avaliaram o fármaco em vários modelos de roedores. Em camundongos projetados para expressar o KCNT1 humano, injeções no líquido cerebral reduziram tanto o RNA de KCNT1 humano quanto o de camundongo de maneira dependente da dose. Em uma linhagem separada de camundongos que desenvolve naturalmente convulsões graves, problemas neurocognitivos e morte precoce devido a outra mutação em KCNT1, o tratamento com o composto líder aumentou a sobrevida mediana de cerca de seis semanas para vários meses e melhorou medidas comportamentais simples, como a construção de ninhos. Estudos em ratos com injeções espinhais repetidas ajudaram a estabelecer doses que pareciam geralmente toleradas com base no comportamento, exames neurológicos e análise de tecidos, ao mesmo tempo em que alcançavam redução substancial de KCNT1 em regiões cerebrais. Esses achados apoiaram o avanço para uso cauteloso e monitorado em pacientes sob um protocolo investigacional especial.
Experiência inicial em duas crianças
Duas meninas de três anos com a mutação KCNT1 p.R474H, ambas com convulsões desde o período neonatal e progresso de desenvolvimento mínimo, receberam doses crescentes de valeriasen administradas por punção lombar no líquido que envolve a medula espinhal. Em ambas, as contagens de convulsões registradas pelas famílias e confirmadas por eletroencefalogramas repetidos caíram consideravelmente após várias doses, e uma criança apresentou melhorias no controle da cabeça, deglutição e na capacidade de se acalmar sozinha. Os níveis do fármaco no líquido espinhal e no sangue comportaram-se conforme esperado a partir dos estudos animais. No entanto, após meses de tratamento com doses cumulativas relativamente altas, ambas as crianças desenvolveram uma complicação séria: aumento progressivo dos espaços fluidos do cérebro com aumento da pressão, uma forma de hidrocefalia. A família de uma das crianças optou por cuidados paliativos, e ela veio a falecer; a outra precisou de um shunt implantado cirurgicamente para drenar o excesso de líquido.
Equilibrando promessa e risco
Diante desse efeito colateral inesperado, a equipe pausou as doses e revisou cuidadosamente os dados de animais e de laboratório. Hidrocefalia não havia sido observada em modelos de camundongo sem KCNT1 ou portadores de mutações da doença, e levantamentos genéticos sugerem que pessoas toleram a perda de uma cópia de KCNT1, o que argumenta contra uma toxicidade simples no alvo. Alguns outros oligonucleotídeos antisenso usados em doenças neurológicas foram associados a casos raros de aumento da pressão intracraniana ou ampliação ventricular, especialmente em doses mais altas, sugerindo que o problema pode derivar da interação de certos compostos com as estruturas cerebrais que produzem e drenam o líquido. Após uma pausa de dois anos, a segunda paciente retomou o tratamento com um regime revisado de dose mais baixa e com ressonâncias magnéticas e checagens de pressão adicionais; sob esse protocolo cauteloso, ela novamente apresentou cerca de dois terços de redução nas convulsões sem novo acúmulo de líquido até o momento.
O que isso significa para o futuro
Para famílias e clínicos que enfrentam epilepsias genéticas catastróficas, este trabalho mostra que silenciar diretamente um canal iônico hiperativo com um fármaco genético sob medida pode realmente reduzir convulsões, mesmo em crianças que não responderam a todos os medicamentos convencionais. Ao mesmo tempo, o aparecimento de hidrocefalia em ambas as pacientes tratadas destaca que terapias tão potentes podem acarretar riscos sérios e ainda pouco compreendidos. Os autores concluem que inibir o canal KCNT1 é uma estratégia válida e promissora, mas que a dosagem deve ser abordada de forma gradual, com monitoramento clínico e imagens cerebrais cuidadosos incorporados a futuros ensaios. Mais amplamente, o estudo ressalta tanto o potencial transformador quanto a responsabilidade ética envolvida no desenvolvimento de medicamentos genéticos individualizados para alguns dos pacientes mais graves.
Citação: Nakayama, T., El Achkar, C.M., Burbano, L.E. et al. Antisense oligonucleotide-mediated knockdown therapy in two infants with severe KCNT1 epileptic encephalopathy. Nat Med 32, 1411–1420 (2026). https://doi.org/10.1038/s41591-026-04314-9
Palavras-chave: epilepsia KCNT1, oligonucleotídeo antisenso, medicina de precisão, convulsões infantis, hidrocefalia