Clear Sky Science · ar
علاج بالخفض باستخدام أوليغونوكليوتيدات مضادة للحس في رضيعَين مصابين باعتلال دماغي صرعي شديد مرتبط بـ KCNT1
لماذا تهم هذه الدراسة العائلات
بعض أشد أنواع الصرع تدميراً تبدأ في الأيام الأولى من الحياة ولا تستجيب للأدوية القياسية، فتترك الرضَّع يعانون نوبات متكررة وإعاقات نموية عميقة. تستكشف هذه الدراسة نوعاً شديد التخصيص من الأدوية الجينية — دواء على شكل أوليغونوكليوتيد مضاد للحس — مصمم لتقليل نشاط قناة دماغية واحدة مفرطة النشاط لدى فتاتين صغيرتين. تُظهر الدراسة كيف قد تُخضع العلاجات الموجهة نوبات لا تستجيب للعلاج، لكنها تكشف أيضاً عن مخاطر خطيرة يجب فهمها قبل أن تنتشر هذه الأساليب.
مشكلة النوبات المستمرة في بداية الحياة
الصرع الطفولي مع نوبات بؤرية هاجرة هو حالة نادرة لكنها بالغة الشدة. تصاب الأَطفال بنوبات خلال ساعات أو أيام من الولادة، وغالباً ما يعانون عشرات النوبات يومياً رغم تجريب عدة أدوية مضادة للنوبات. في نحو نصف هؤلاء الأطفال يكون السبب طفرة جديدة في جين يدعى KCNT1، والذي يشفر قناة تسمح لأيونات البوتاسيوم بالمرور عبر أغشية خلايا الدماغ. الطفرة المحددة المدروسة هنا، المسماة p.R474H، تجعل القنوات أكثر نشاطاً بكثير من الطبيعي، مما يدفع شبكات الخلايا العصبية إلى حالة فرط إثارة مستمرة. عادةً ما يظهر على هؤلاء الأطفال تقدم نمائي ضئيل جداً، مع خطر عالٍ للوفاة المبكرة ولا توجد حالياً علاجات فعالة مضمونة.
دواء يستهدف الجين صنع في المختبر
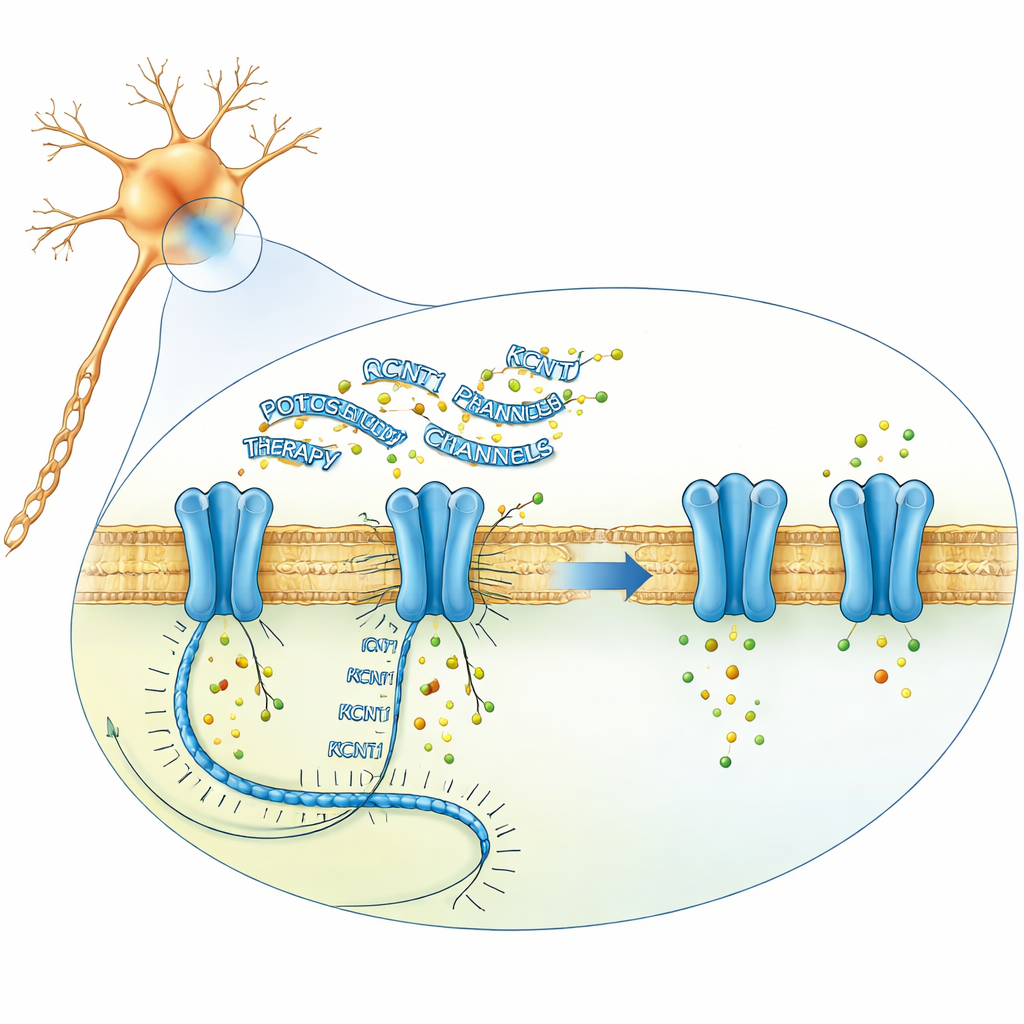
سعى فريق البحث إلى خفض كمية رسالة KCNT1 المعيبة داخل الخلايا العصبية باستخدام أوليغونوكليوتيدات مضادة للحس: سلاسل قصيرة معدلة كيميائياً من المادة الوراثية يمكنها الالتحام بشكل انتقائي بمرسال رنا معين وإحداث تكسّره. انطلقوا من أكثر من 250 تسلسلاً مرشحاً، ثم ضيقوا التصاميم تدريجياً في خلايا شبيهة بالعصب البشري المزروعة، وفي خلايا عصبية نُمت من خلايا جذعية لمرضى، وفي خلايا فأر. المركب الرائد لديهم، الذي سُمّي لاحقاً فاليرياسين، خفّض بشدة مستويات رنا وبروتين KCNT1 في الخلايا العصبية المأخوذة من المرضى وفي سلالة فأر تحمل الطفرة المماثلة، دون الإخلال العام بجينات أخرى. أظهرت تجارب الكهرباء الخلوية أن الدواء أعاد تيارات البوتاسيوم الشاذة إلى طبيعتها وقرب أنماط إطلاق النَبَضات في الخلايا المُطالَبة لتكون أقرب إلى الخلايا السليمة، ما يوحي بأن تقليل نشاط القناة قد يصحح الخلل الكهربائي الكامن.
الاختبارات في نماذج حيوانية قبل البشر
قبل التفكير في الاستخدام لدى الأطفال، قيَّم الباحثون الدواء في عدة نماذج قوارض. في فئران هندست لتعبير KCNT1 البشري، أدت الحقن في سائل الدماغ إلى خفض رنا KCNT1 البشري والماوسي بطريقة تعتمد على الجرعة. في سلالة فأر منفصلة تتطور طبيعياً لتظهر نوبات شديدة ومشكلات معرفية وموتاً مبكراً بسبب طفرة KCNT1 مختلفة، مدد العلاج بالمركب الرائد متوسط العمر المتبقي من نحو ستة أسابيع إلى عدة أشهر وحسّن مقاييس سلوكية بسيطة مثل بناء العش. ساعدت دراسات في جرذان باستخدام حقن شوكية متكررة على تحديد جرعات اعتُبرت مقبولة عموماً استناداً إلى السلوك والفحوص العصبية وتحليل الأنسجة، وفي الوقت نفسه حققت خفضاً كبيراً في KCNT1 في مناطق الدماغ. دعمت هذه النتائج التقدم بحذر نحو استخدام مراقب عن كثب للمرضى في بروتوكول تحقيقي خاص.
التجربة المبكرة في طفلَين
تلقّت فتاتان تبلغان ثلاث سنوات وتحملان طفرة KCNT1 p.R474H، وكلتاهما تعرَّضت للنوبات منذ فترة الوليدية وحققت تقدماً نمائياً ضئيلاً، جرعات متصاعدة من فاليرياسين أُعطيت عبر بزل قطني إلى السائل المحيط بالحبل الشوكي. في كلتا الحالتين، انخفضت أعداد النوبات التي سجلتها العائلات وتأكدت عبر تخطيطات دماغ متكررة بعد عدة جرعات، وأظهرت إحداهن تحسناً في سيطرة الرأس والبلع والقدرة على تهدئة النفس. تصرّف مستوى الدواء في سائل النخاع والدم كما كان متوقعاً من الأعمال الحيوانية. ومع ذلك، بعد أشهر من العلاج بجرعات تراكمية مرتفعة نسبياً، طوّر كلتا الطفلتين مضاعفة خطيرة: تزايد تدريجي في اتساع تجاويف سائل الدماغ مع زيادة الضغط، وهو شكل من أشكال الاستسقاء. اختارت عائلة إحدى الطفلتين رعاية تلطيفية، وتوفيت لاحقاً؛ أما الأخرى فاحتاجت إلى صمام مزروع جراحياً لتصريف السائل الزائد.
موازنة الوعد والمخاطر
في مواجهة هذا التأثير الجانبي غير المتوقع، أوقف الفريق الجرعات وراجع بعناية بيانات الحيوانات والمختبر. لم يظهر الاستسقاء في نماذج الفأر التي تفتقر إلى KCNT1 أو التي تحمل طفرات مرضية، وتوحي دراسات جينية بأن البشر قد يتحملون فقدان نسخة واحدة من KCNT1، مما يقلل من احتمال سمية مباشرة مستهدفة. ارتبطت بعض الأدوية المضادة للحس المستخدمة في أمراض عصبية بحالات نادرة من ارتفاع ضغط الدماغ أو اتساع البطينات، لاسيما عند جرعات أعلى، مما يوحي بأن المشكلة قد تنجم عن تفاعلات بعض المركبات مع هياكل إنتاج أو تصريف السائل الدماغي. بعد توقف دام عامين، استأنفت المريضة الثانية العلاج بجرعات مخفَّضة مجدداً مع فحوص رنين مقطعي متتالية وفحوص ضغط؛ وفي هذا النظام الحذر اختبرت مرة أخرى انخفاضاً بحوالي ثلثَي عدد النوبات دون ظهور تراكم سائل جديد حتى الآن.
ما يعنيه هذا للمستقبل
بالنسبة للعائلات والأطباء الذين يواجهون الصرعات الجينية الكارثية، تُظهر هذه الدراسة أن إسكات قناة أيونية مفرطة النشاط مباشرةً بواسطة دواء جيني مخصص يمكن أن يقلل النوبات بفاعلية، حتى لدى أطفال لم تنجح معهم كل الأدوية التقليدية. وفي الوقت نفسه، يؤكّد بروز الاستسقاء في كلتا الحالتين المعالَجتين أن مثل هذه العلاجات القوية قد تحمل مخاطر خطيرة لا تزال مفهومة جزئياً. يستنتج المؤلفون أن تثبيط قناة KCNT1 استراتيجية صحيحة وواعدة، لكن يجب الاقتراب من الجرعات تدريجياً مع تضمين تصوير دماغي دقيق ورقابة سريرية في التجارب المستقبلية. وعلى نطاق أوسع، تسلط الدراسة الضوء على الإمكانات التحولية والمسؤولية الأخلاقية المرتبطة بتصميم أدوية جينية مخصصة لبعض أشد المرضى احتياجاً.
الاستشهاد: Nakayama, T., El Achkar, C.M., Burbano, L.E. et al. Antisense oligonucleotide-mediated knockdown therapy in two infants with severe KCNT1 epileptic encephalopathy. Nat Med 32, 1411–1420 (2026). https://doi.org/10.1038/s41591-026-04314-9
الكلمات المفتاحية: صرع KCNT1, أوليغونوكليوتيد مضاد للحس, الطب الدقيق, نوبات رضَعَة, استسقاء الرأس