Clear Sky Science · nl
Antisense-oligonucleotide-gemedieerde knockdown-therapie bij twee zuigelingen met ernstige KCNT1 epileptische encefalopathie
Waarom deze studie belangrijk is voor gezinnen
Sommige van de verwoestendste vormen van epilepsie beginnen in de eerste levensdagen en reageren niet op standaardmedicatie, waardoor zuigelingen constante aanvallen en ernstige ontwikkelingsachterstand hebben. Deze studie onderzoekt een sterk gepersonaliseerde vorm van genetische geneeskunde — een antisense-oligonucleotidemiddel — dat is ontworpen om de activiteit van één overactief hersenkanaal terug te schroeven bij twee jonge meisjes. Het biedt een blik op hoe precisietherapieën anders onbehandelbare aanvallen kunnen temperen, terwijl het ook ernstige risico’s blootlegt die moeten worden begrepen voordat dergelijke benaderingen breed kunnen worden ingezet.
Het probleem van onophoudelijke aanvallen in de vroege levensfase
Epilepsie van de zuigeling met verschuivende focale aanvallen is een zeldzame maar extreem ernstige aandoening. Baby’s krijgen binnen uren of dagen na de geboorte aanvallen en ervaren vaak tientallen per dag ondanks het proberen van vele anti-epileptica. Bij ongeveer de helft van deze kinderen is de oorzaak een nieuwe mutatie in een gen genaamd KCNT1, dat codeert voor een kanaal waardoor kaliumionen door de membranen van hersencellen stromen. De specifieke mutatie die hier bestudeerd wordt, p.R474H, maakt de kanalen veel actiever dan normaal, waardoor netwerken van neuronen voortdurend overgeprikkeld raken. Deze kinderen laten doorgaans vrijwel geen ontwikkelingsteken zien, hebben een hoog risico op vroege sterfte en hebben momenteel geen betrouwbaar effectieve behandelingen.
Een in het laboratorium ontwikkeld gengericht middel
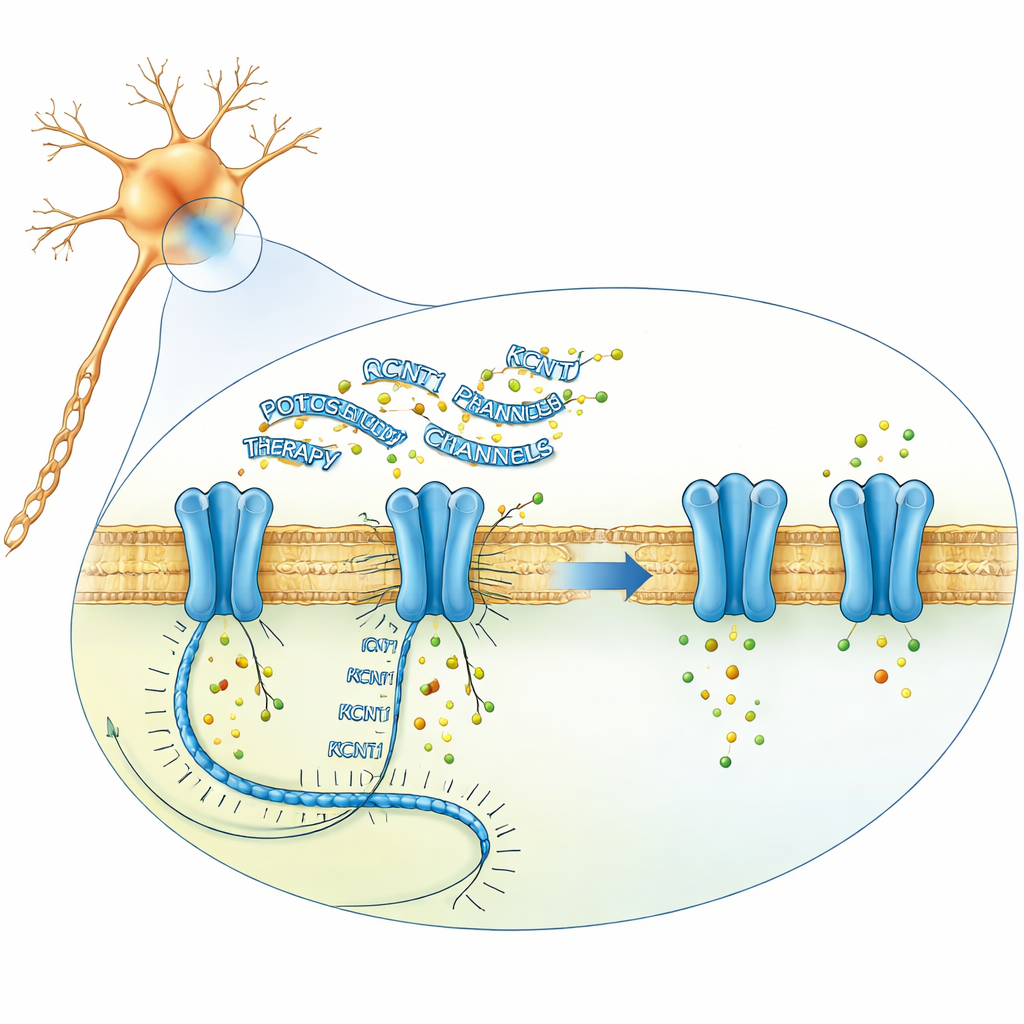
Het onderzoeksteam wilde de hoeveelheid foutief KCNT1-bericht in neuronen verminderen met antisense-oligonucleotiden: korte, chemisch gemodificeerde strengen genetisch materiaal die zich aan een gekozen RNA kunnen binden en de vernietiging daarvan kunnen activeren. Beginnend met meer dan 250 kandidaat-sequenties verfijnden ze de ontwerpen stapsgewijs in gekweekte mensachtige zenuwcellen, in neuronen die uit patiëntstamcellen waren gekweekt en in muiscellen. Hun leidende verbinding, later valeriasen genoemd, verlaagde scherp de KCNT1-RNA- en eiwitniveaus in patiënt-afgeleide neuronen en in een muislijn met de overeenkomstige ziekte-mutatie, zonder andere genen breed te verstoren. Elektrofysiologische experimenten toonden aan dat het middel de abnormaal grote kaliumstromen normaliseerde en de vuurmotoriek van mutant-neuronen veel dichter bij die van gezonde cellen bracht, wat suggereert dat het afzwakken van het kanaal de onderliggende elektrische disbalans kan herstellen.
Testen in diermodellen vóór gebruik bij mensen
Voordat men het middel bij kinderen overwoog, evalueerden de onderzoekers het in meerdere knaagdiermodellen. Bij muizen die geprogrammeerd waren om menselijk KCNT1 te tot expressie te brengen, verminderden injecties in het hersenvocht zowel muis- als menselijk KCNT1-RNA op een dosisafhankelijke manier. In een aparte muizenstam die van nature ernstige aanvallen, neurocognitieve problemen en vroege sterfte ontwikkelt door een andere KCNT1-mutatie, verlengde behandeling met het leidende middel de mediane levensduur van ongeveer zes weken naar vele maanden en verbeterde eenvoudige gedragsmaatregelen zoals nestbouw. Studies bij ratten met herhaalde spinale injecties hielpen doses vaststellen die op basis van gedrag, neurologisch onderzoek en weefselanalyse over het algemeen verdragen leken te worden, terwijl toch aanzienlijke KCNT1-knockdown in hersengebieden werd bereikt. Deze bevindingen ondersteunden het voorzichtig doorgaan naar zorgvuldig gecontroleerd gebruik bij patiënten onder een speciaal onderzoeksprotocol.
Vroege ervaring bij twee kinderen
Twee driejarige meisjes met de KCNT1 p.R474H-mutatie, beide met aanvallen vanaf de pasgeboren periode en minimale ontwikkelingsprogressie, ontvingen oplopende doses valeriasen toegediend via lumbaalpunctie in het vocht rond het ruggenmerg. Bij beide nam het aantal aanvallen, zoals door gezinnen geregistreerd en bevestigd met herhaalde elektro-encefalogrammen, aanzienlijk af na meerdere doses, en één kind liet verbeteringen zien in hoofdcontrole, slikken en vermogen om zichzelf te troosten. De medicijnspiegels in ruggenmergvocht en bloed gedroegen zich zoals verwacht op basis van het dieronderzoek. Echter, na maanden van behandeling met relatief hoge cumulatieve doses, ontwikkelden beide kinderen een ernstige complicatie: progressieve vergroting van de met vocht gevulde ruimtes in de hersenen met verhoogde druk, een vorm van hydrocefalus. De familie van één kind koos voor palliatieve zorg en zij overleed later; het andere kind had een chirurgisch geïmplanteerde shunt nodig om overtollig vocht af te voeren.
Afweging van belofte en risico
Gevraagd geconfronteerd met dit onverwachte bijeffect, stopte het team met doseren en beoordeelde zorgvuldig dier- en laboratoriumgegevens. Hydrocefalus was niet waargenomen in muismodellen zonder KCNT1 of met ziektemutaties, en genetische onderzoeken suggereren dat mensen het verlies van één kopie van KCNT1 kunnen verdragen, wat pleit tegen eenvoudige on-target toxiciteit. Sommige andere antisense-middelen die in neurologische aandoeningen worden gebruikt, zijn in zeldzame gevallen in verband gebracht met verhoogde hersendruk of ventriculaire vergroting, vooral bij hogere doses, wat erop wijst dat het probleem mogelijk samenhangt met hoe bepaalde verbindingen interactie hebben met de structuren die hersenvocht produceren en afvoeren. Na een onderbreking van twee jaar hervatte de tweede patiënt de behandeling onder een herzien, lager dosisregime met extra MRI-scans en drukcontroles; onder dit behoedzame schema ervoer zij opnieuw ongeveer een twee derde reductie van aanvallen zonder tot nu toe nieuwe vochtophoping.
Wat dit betekent voor de toekomst
Voor gezinnen en clinici die geconfronteerd worden met catastrofale genetische epilepsieën toont dit werk aan dat het direct tot rust brengen van een overactief ionenkanaal met een op maat gemaakt genetisch middel aanvallen daadwerkelijk kan verminderen, zelfs bij kinderen die op geen enkele conventionele medicatie reageerden. Tegelijkertijd onderstreept het optreden van hydrocefalus bij beide behandelde patiënten dat zulke krachtige therapieën ernstige, nog slecht begrepen risico’s kunnen meebrengen. De auteurs concluderen dat remming van het KCNT1-kanaal een valide en veelbelovende strategie is, maar dat dosering geleidelijk moet gebeuren, met zorgvuldige beeldvorming van de hersenen en klinische monitoring ingebouwd in toekomstige trials. Breder gezien benadrukt de studie zowel het transformerende potentieel als de ethische verantwoordelijkheid die gepaard gaan met het ontwerpen van geïndividualiseerde genetische geneesmiddelen voor enkele van de ernstigst zieke patiënten.
Bronvermelding: Nakayama, T., El Achkar, C.M., Burbano, L.E. et al. Antisense oligonucleotide-mediated knockdown therapy in two infants with severe KCNT1 epileptic encephalopathy. Nat Med 32, 1411–1420 (2026). https://doi.org/10.1038/s41591-026-04314-9
Trefwoorden: KCNT1 epilepsie, antisense-oligonucleotide, precisiegeneeskunde, zuigelingkrampen, hydrocefalus