Clear Sky Science · sv
2′-O-metyl-guanosin RNA-fragment motverkar TLR7 och TLR8 för att begränsa autoimmunsjukdom
Varför vårt immunsystem måste skilja vän från fiende
Varje dag rensar våra kroppar tyst bort miljarder döende celler utan att väcka skadlig inflammation. Samtidigt måste immunsystemet vara redo att slå till mot virus och bakterier, många av vilka bär genetiskt material som liknar vårt eget. Denna studie avslöjar en inbyggd säkerhetsmekanism som hjälper immunsensorer att undvika överreaktioner mot kroppens eget RNA, och ger nya ledtrådar till varför vissa personer utvecklar autoimmuna sjukdomar som lupus samt hur vi bättre kan utforma vacciner och antiinflammatoriska läkemedel.
Vakter som lyssnar efter farosignaler
Långt inne i immunceller sitter två molekylära "lyssnarpunkter" kallade TLR7 och TLR8. De patrullerar små membranblåsor som slukar delar av RNA från virus, bakterier eller döende celler. När dessa receptorer upptäcker rätt typ av korta RNA-fragment antar de en aktiv form och utlöser produktion av antiviral och inflammatorisk signalering. Om de svarar för svagt kan infektioner som svår COVID‑19 bli livshotande; om de aktiveras för lätt kan immunsystemet börja angripa frisk vävnad. Fram till nu förstod forskare inte fullt ut hur dessa sensorer ignorerar floden av ofarliga RNA-fragment som bildas när kroppen tyst återvinner sina egna celler.
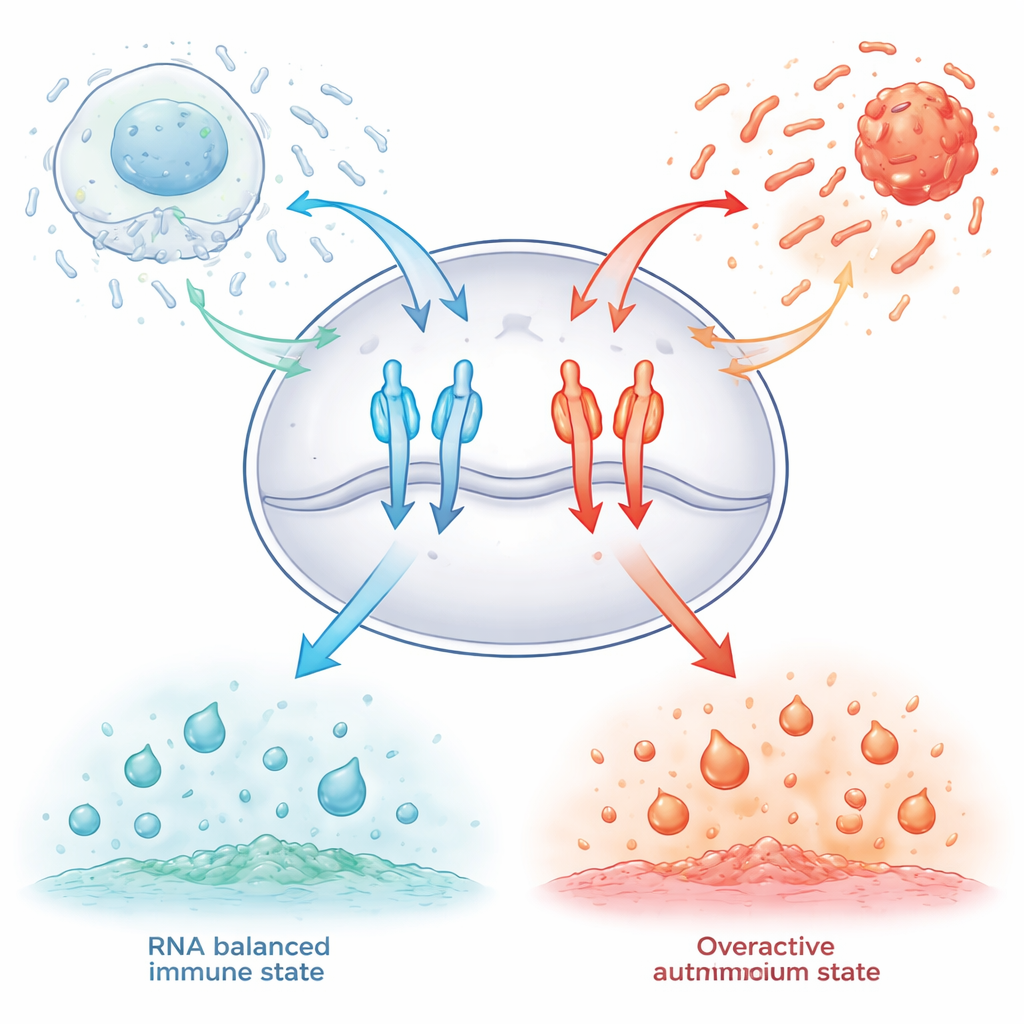
Särskilda RNA-fragment som fungerar som molekylära bromsar
Författarna fokuserade på mycket korta, tre-bokstavslånga RNA-bitar som bär en subtil kemisk ändring: en metylgrupp på sockret i en guanosinbas, känd som 2′‑O‑metyl‑guanosin. Genom att systematiskt testa alla 64 möjliga tre-bokstavskombinationer i humana celler som ingenjörsmodellerats för att uttrycka TLR7 eller TLR8 fann de att fragment som börjar med denna modifierade guanosin kraftigt kan dämpa receptoraktiviteten. Vissa kombinationer tystade TLR7, andra TLR8, och några ökade till och med TLR8‑svar, vilket visar att den exakta sekvensen finjusterar hur dessa immunknappfunktioner beter sig. Viktigt är att dessa korta bitar fungerade inte bara mot konstgjorda läkemedelsliknande stimulanser utan också mot genuina RNA-agonister från virus och bakterier, och de kunde dämpa immunsignalering i mänskligt blod.
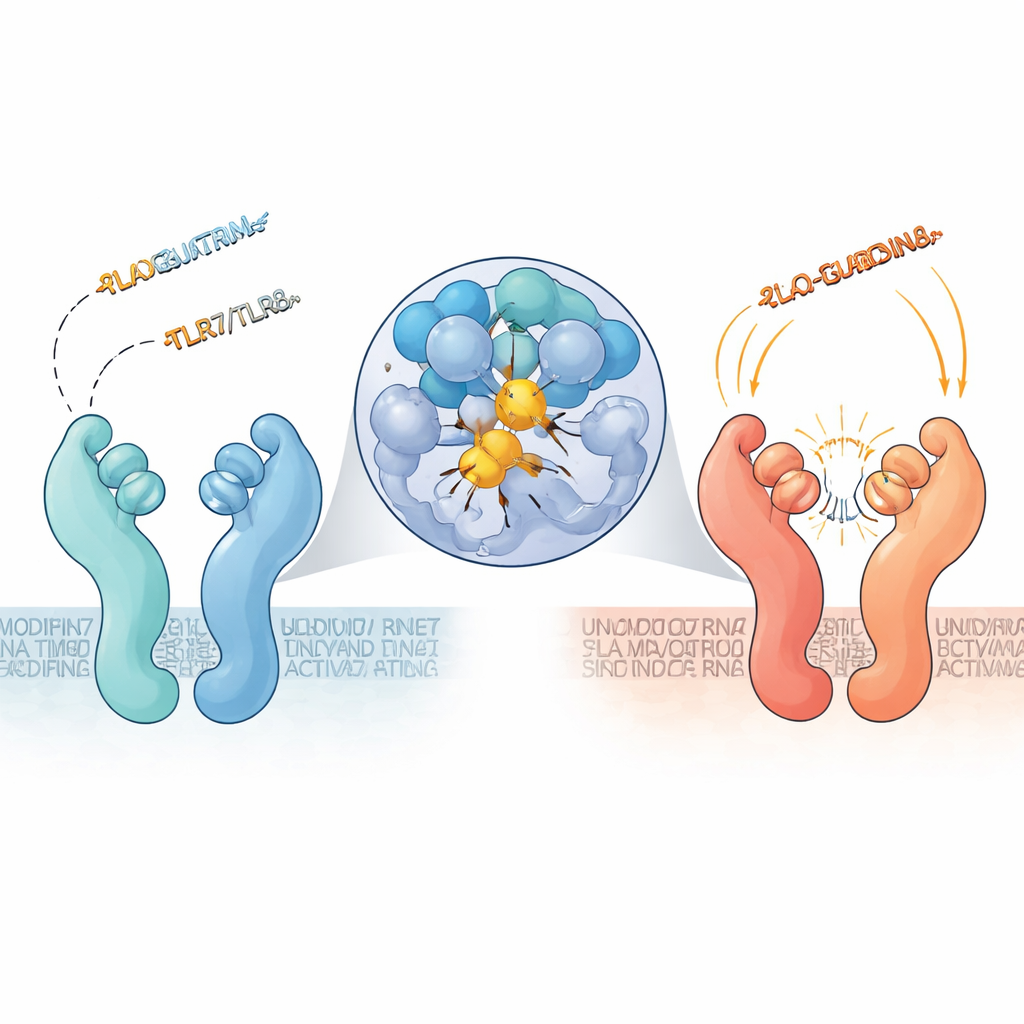
En dold avstängningsficka avslöjad
För att förstå hur dessa fragment verkar kombinerade teamet avancerad mikroskopi med datorimuleringar. Högupplöst kryo-elektronmikroskopi visade att särskilda tre-bokstavsfragment som innehåller 2′‑O‑metyl‑guanosin hakar fast i en tidigare underskattad fåra som bildas mellan de två halvorna av TLR7-proteinet. När denna ficka fylls förblir receptorn i en "öppen" vilande form som inte kan signalera, även om aktiverande RNA finns någon annanstans. Den modifierade guanosinen i fragmentets början ligger djupt inbäddad i en klunga aromatiska aminosyror och bildar täta staplings- och vätebindningsinteraktioner. Vanligt, omodifierat RNA kan inte greppa denna plats lika bra, vilket gör dessa metylerade fragment till kraftfulla naturliga antagonister.
Naturliga bromsar från ribosomalt RNA och mutationskopplingar till sjukdom
Berättelsen blir ännu mer intressant när man funderar på var sådana fragment kommer ifrån. Författarna påpekar att våra ribosomer — de cellulära maskiner som bygger proteiner — är packade med över hundra 2′‑O‑metylmärken, många av dem på guanosin i tre-bokstavsmönster som matchar de mest effektiva hämmande motiven. När ribosomalt RNA sönderdelas under normal cellomsättning uppstår dessa fragment inne i immunceller. Experiment visade att renat ribosomalt RNA kan undertrycka TLR7- och TLR8‑aktivitet, och att minskad nivå av metylsättande enzymet fibrillarin försvagar denna effekt. Dessutom ändrar sällsynta mänskliga mutationer som hittats hos patienter med lupus eller besläktade tillstånd viktiga aminosyror i antagonistfickan hos TLR7 eller TLR8. Dessa förändringar minskar bindningen av de modifierade fragmenten, luckrar upp den naturliga bromsen och främjar autoimmun inflammation.
Konsekvenser för vacciner och autoimmun terapi
I möss dämpade syntetiska tre-bokstavsfragment designade för att efterlikna dessa naturliga motiv framgångsrikt TLR7‑driven inflammation i modeller för hudsjukdom och minskade de inflammatoriska biverkningar som orsakades av ett omodifierat mRNA levererat i lipidnanopartiklar, liknande dem som används i vacciner. För en icke-specialist är huvudbudskapet att våra celler ständigt genererar små, kemiskt märkta RNA-bitar som stoppar en speciell avstängningsknapp på viktiga immunsensorer och förhindrar att de misstolkar vardagligt cellulärt skräp som ett hot. När den avstängningsknappen försvagas — genom genetisk mutation eller kanske genom obalanserad RNA‑bearbetning — är immunsystemet mer benäget att avfyra mot kroppen själv. Att förstå och utnyttja dessa naturliga RNA‑"bromsar" kan hjälpa till att utforma säkrare vacciner och nya behandlingar för autoimmuna sjukdomar.
Citering: Alharbi, A.S., Sapkota, S., Zhang, Z. et al. 2′-O-Methyl-guanosine RNA fragments antagonize TLR7 and TLR8 to limit autoimmunity. Nat Immunol 27, 762–775 (2026). https://doi.org/10.1038/s41590-026-02429-2
Nyckelord: medfödd immunitet, Toll-liknande receptorer, RNA-modifikationer, autoimmunitet, ribosomalt RNA