Clear Sky Science · it
Frammenti di RNA con 2′-O‑metil‑guanosina antagonizzano TLR7 e TLR8 per limitare l’autoimmunità
Perché il nostro sistema immunitario deve distinguere amici e nemici
Ogni giorno i nostri corpi eliminano silenziosamente miliardi di cellule in morte senza scatenare infiammazioni dannose. Allo stesso tempo, il sistema immunitario deve rimanere pronto ad attaccare virus e batteri, molti dei quali portano materiale genetico simile al nostro. Questo lavoro individua un meccanismo di sicurezza intrinseco che aiuta i sensori immunitari a evitare reazioni eccessive all’RNA endogeno, offrendo nuovi indizi sul perché alcune persone sviluppano malattie autoimmuni come il lupus e su come potremmo progettare meglio vaccini e farmaci antiinfiammatori.
Guardiani che ascoltano segnali di pericolo
All’interno delle cellule immunitarie si trovano due «postazioni d’ascolto» molecolari chiamate TLR7 e TLR8. Sorvegliano piccole vescicole di membrana che inglobano frammenti di RNA provenienti da virus, batteri o cellule in morte. Quando questi recettori rilevano il giusto tipo di brevi frammenti di RNA, assumono una conformazione attiva e innescano la produzione di molecole antivirali e infiammatorie. Se rispondono troppo poco, infezioni come forme gravi di COVID‑19 possono diventare pericolose; se si attivano troppo facilmente, il sistema immunitario può attaccare tessuti sani. Fino a oggi i ricercatori non avevano compreso del tutto come questi sensori ignorino il flusso di frammenti di RNA innocui prodotti quando il corpo ricicla silenziosamente le proprie cellule.
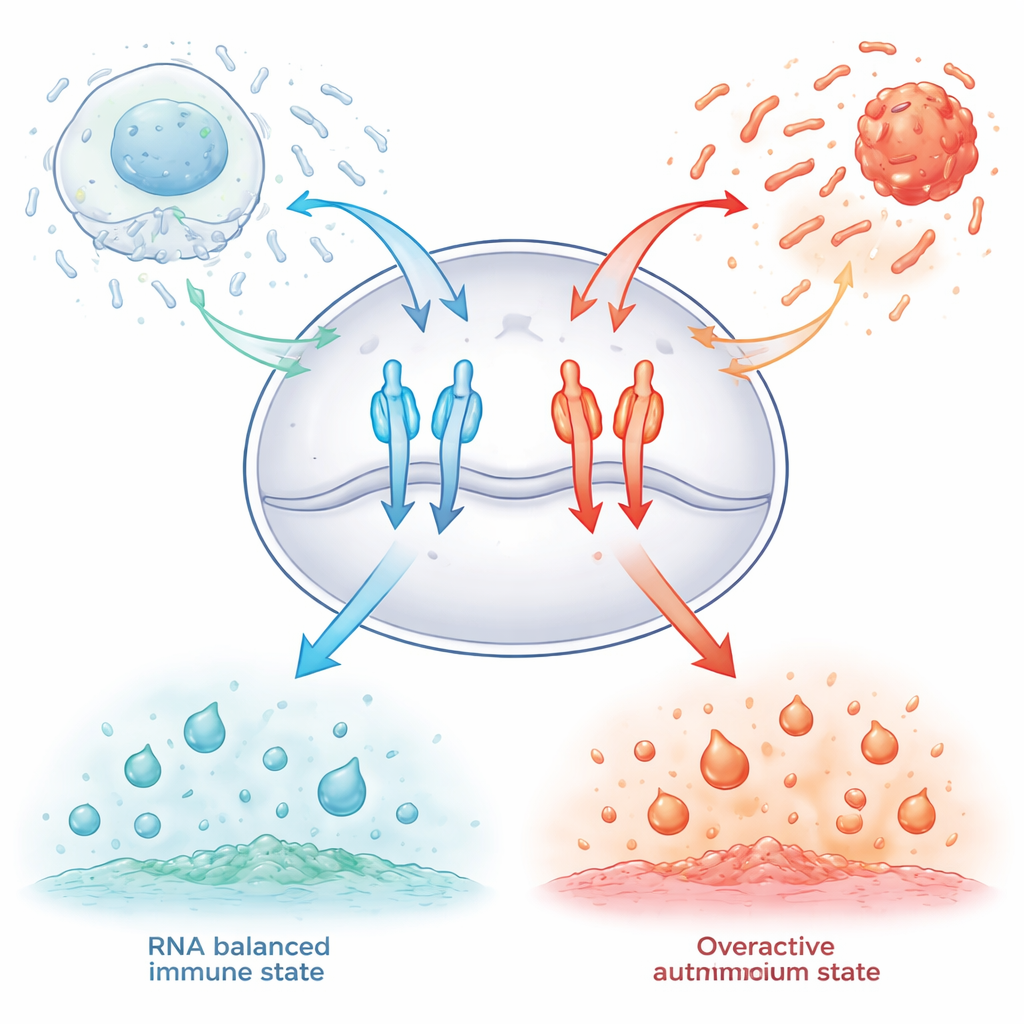
Frammenti di RNA speciali che fungono da freni molecolari
Gli autori si sono concentrati su pezzi di RNA molto corti, lunghi tre basi, che portano una sottile modifica chimica: un gruppo metile sullo zucchero della base guanosina, noto come 2′‑O‑metil‑guanosina. Testando sistematicamente tutte le 64 possibili combinazioni di tre basi in cellule umane ingegnerizzate per esprimere TLR7 o TLR8, hanno scoperto che i frammenti che iniziano con questa guanosina modificata possono attenuare fortemente l’attività dei recettori. Alcune combinazioni silenziavano TLR7, altre TLR8, e alcune aumentavano persino le risposte di TLR8, dimostrando che la sequenza precisa modula finemente il comportamento di questi interruttori immunitari. Importante, questi brevi pezzi funzionavano non solo contro stimolanti artificiali simili a farmaci, ma anche contro agonisti RNA genuini provenienti da virus e batteri, e riuscivano a ridurre la segnalazione immunitaria in cellule del sangue umano.
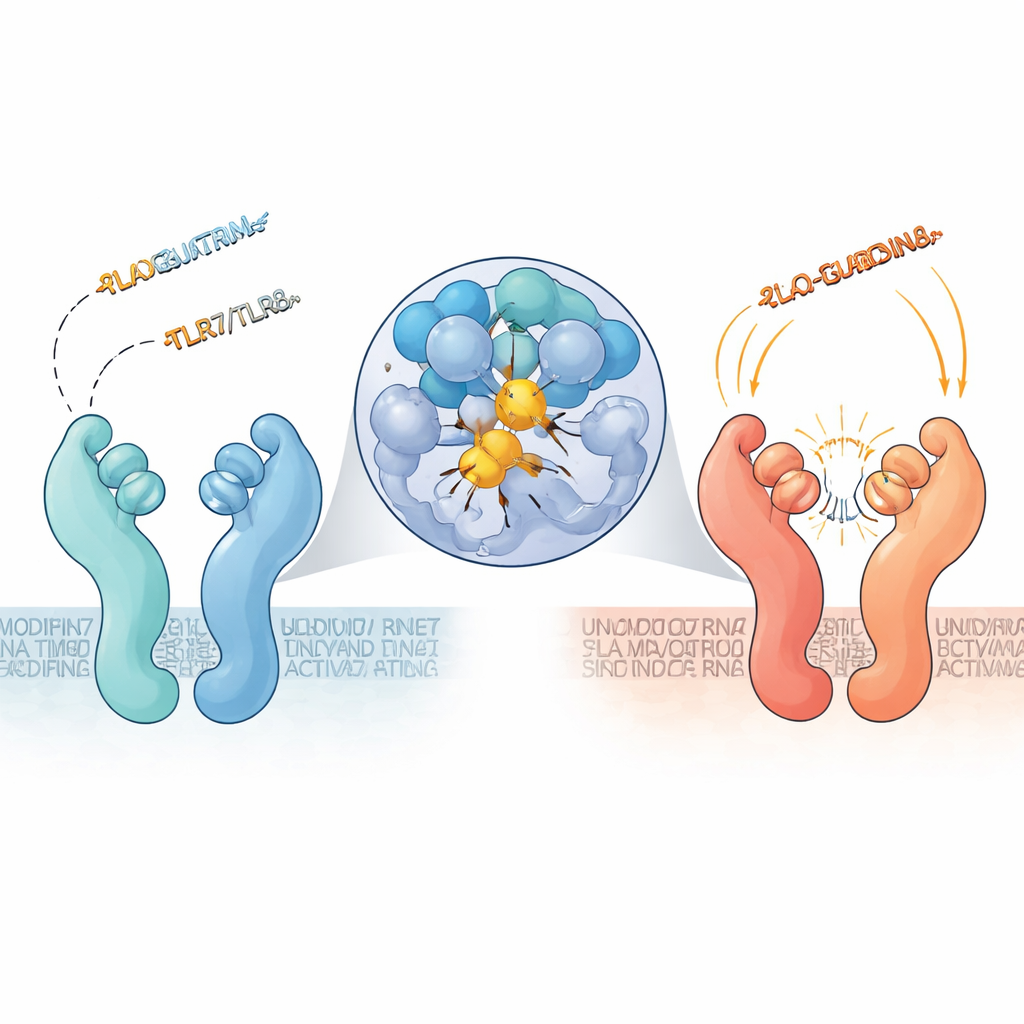
Rivelata una tasca nascosta per lo spegnimento
Per capire come agiscono questi frammenti, il gruppo ha combinato microscopia avanzata con simulazioni al computer. La microscopia crioelettronica ad alta risoluzione ha mostrato che particolari frammenti di tre basi contenenti 2′‑O‑metil‑guanosina si agganciano a una scanalatura finora poco apprezzata formata tra le due metà della proteina TLR7. Quando questa tasca è occupata, il recettore rimane in una conformazione «aperta» di riposo che non può segnalare, anche se RNA attivante è presente altrove. La guanosina modificata nella posizione iniziale del frammento si inserisce profondamente in un ammasso di amminoacidi aromatici, stabilendo interazioni di impilamento e legami a idrogeno robusti. L’RNA ordinario, non modificato, non riesce ad ancorarsi a questo sito altrettanto bene, rendendo questi frammenti metilati potenti antagonisti naturali.
Freni naturali dall’RNA ribosomiale e mutazioni associate alla malattia
La storia diventa ancora più interessante pensando alla provenienza di tali frammenti. Gli autori sottolineano che i nostri ribosomi—le macchine cellulari che costruiscono le proteine—sono ricchi di oltre cento marche 2′‑O‑metil, molte delle quali sulla guanosina in schemi di tre basi che corrispondono ai migliori motivi inibitori. Quando l’RNA ribosomiale viene frammentato durante il turnover cellulare normale, questi frammenti compaiono all’interno delle cellule immunitarie. Gli esperimenti hanno mostrato che l’RNA ribosomiale purificato può sopprimere l’attività di TLR7 e TLR8, e che ridurre l’enzima che aggiunge il metile, fibrillarin, indebolisce questo effetto. Inoltre, rare mutazioni umane riscontrate in pazienti con lupus o condizioni correlate alterano amminoacidi chiave nella tasca antagonista di TLR7 o TLR8. Questi cambiamenti riducono il legame dei frammenti modificati, allentando il freno naturale e favorendo l’infiammazione autoimmunitaria.
Implicazioni per vaccini e terapie autoimmuni
Nei topi, frammenti sintetici di tre basi progettati per imitare questi motivi naturali hanno attenuato con successo l’infiammazione guidata da TLR7 in modelli di malattia cutanea e hanno ridotto gli effetti infiammatori collaterali di un mRNA non modificato somministrato in nanoparticelle lipidiche, simili a quelle usate nei vaccini. Per un pubblico non specialista, il messaggio principale è che le nostre cellule producono costantemente piccoli pezzi di RNA chimicamente marcati che occupano un particolare interruttore di spegnimento su recettori immunitari chiave, impedendo loro di interpretare erroneamente i detriti cellulari quotidiani come una minaccia. Quando quell’interruttore è indebolito—per mutazione genetica o forse per un’elaborazione dell’RNA squilibrata—il sistema immunitario è più propenso a sbagliare bersaglio contro il corpo stesso. Comprendere e sfruttare questi «freni» naturali dell’RNA potrebbe aiutare a progettare vaccini più sicuri e nuovi trattamenti per le malattie autoimmuni.
Citazione: Alharbi, A.S., Sapkota, S., Zhang, Z. et al. 2′-O-Methyl-guanosine RNA fragments antagonize TLR7 and TLR8 to limit autoimmunity. Nat Immunol 27, 762–775 (2026). https://doi.org/10.1038/s41590-026-02429-2
Parole chiave: immunità innata, recettori Toll-like, modifiche dell’RNA, autoimmunità, RNA ribosomiale