Clear Sky Science · pl
Fragmenty RNA z 2′-O-metylowo zmodyfikowanym guanozyną antagonizują TLR7 i TLR8, ograniczając autoimmunizację
Dlaczego nasz układ odpornościowy musi rozróżniać swoich od obcych
Codziennie nasze ciało bezgłośnie usuwa miliardy obumarłych komórek, nie wywołując szkodliwych stanów zapalnych. Jednocześnie układ odpornościowy musi być gotów do ataku na wirusy i bakterie, z których wiele zawiera materiał genetyczny podobny do naszego. Niniejsza praca ujawnia wbudowany mechanizm bezpieczeństwa, który pomaga czujnikom odpornościowym unikać nadreaktywności wobec własnego RNA, dając nowe wskazówki, dlaczego niektórzy ludzie rozwijają choroby autoimmunologiczne, takie jak toczeń, oraz jak lepiej projektować szczepionki i leki przeciwzapalne.
Strażnicy nasłuchujący sygnałów zagrożenia
Głęboko wewnątrz komórek odpornościowych znajdują się dwa molekularne „punkty nasłuchu” zwane TLR7 i TLR8. Patrolują małe pęcherzyki błonowe, które pochłaniają fragmenty RNA wirusów, bakterii lub umierających komórek. Gdy te receptory wykryją odpowiedni rodzaj krótkich fragmentów RNA, zmieniają kształt na aktywny i uruchamiają produkcję cząsteczek przeciwwirusowych i prozapalnych. Jeśli reagują zbyt słabo, zakażenia, takie jak ciężkie COVID‑19, mogą stać się zagrażające życiu; jeśli natomiast uruchamiają się zbyt łatwo, układ odpornościowy może atakować zdrowe tkanki. Do tej pory badacze nie rozumieli do końca, jak te czujniki ignorują zalew nieszkodliwych fragmentów RNA powstających podczas cichego recyklingu komórek.
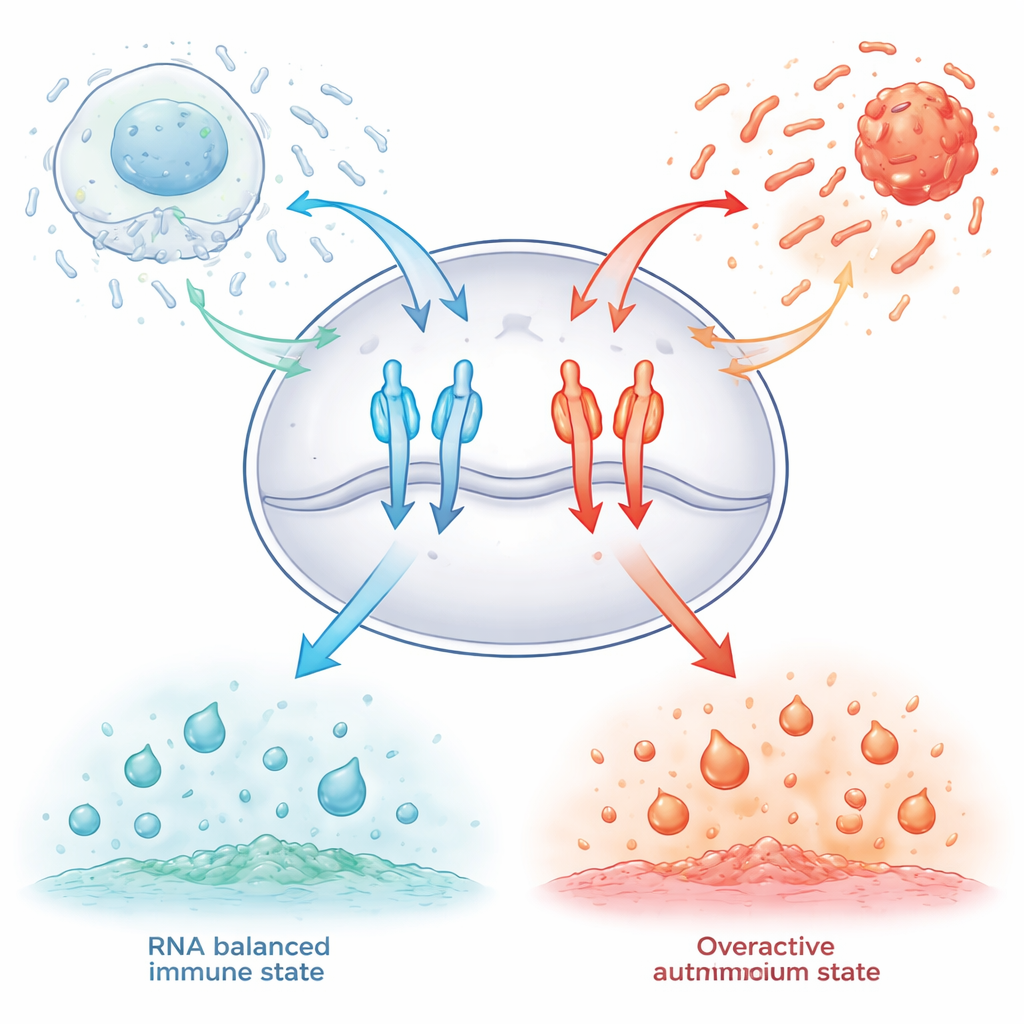
Specjalne fragmenty RNA działające jak molekularne hamulce
Autorzy skupili się na bardzo krótkich, trzy‑literowych odcinkach RNA z subtelną modyfikacją chemiczną: grupą metylową przy cukrze w zasadzie guanozynowej, znaną jako 2′‑O‑metyl‑guanozyna. Testując systematycznie wszystkie 64 możliwe trzy‑literowe kombinacje w komórkach ludzkich inżynieryjnie eksprymujących TLR7 lub TLR8, odkryli, że fragmenty zaczynające się od tej zmodyfikowanej guanozyny silnie tłumią aktywność receptorów. Niektóre sekwencje uciszały TLR7, inne TLR8, a kilka nawet wzmacniało odpowiedzi TLR8, pokazując, że dokładna sekwencja precyzyjnie reguluje działanie tych przełączników odpornościowych. Co ważne, te krótkie fragmenty działały nie tylko przeciw sztucznym stymulantom przypominającym leki, lecz także przeciw prawdziwym agonistom RNA pochodzącym od wirusów i bakterii, i potrafiły osłabić sygnalizację odpornościową w ludzkich komórkach krwi.
Ukryta kieszeń wyłącznika ujawniona
Aby zrozumieć mechanizm działania tych fragmentów, zespół połączył zaawansowaną mikroskopię z symulacjami komputerowymi. Obrazowanie krioelektronowe o wysokiej rozdzielczości wykazało, że pewne trzy‑literowe fragmenty zawierające 2′‑O‑metyl‑guanozynę zakotwiczają się w uprzednio niedocenianej szczelinie powstającej między dwiema połówkami białka TLR7. Gdy ta kieszeń jest wypełniona, receptor pozostaje w „otwartym” spoczynkowym kształcie, który nie może sygnalizować, nawet jeśli gdzie indziej obecne jest aktywujące RNA. Zmodyfikowana guanozyna na przodzie fragmentu wciska się głęboko w skupisko aromatycznych aminokwasów, tworząc ciasne stosowania i wiązania wodorowe. Zwykłe, niemodyfikowane RNA nie potrafi tak silnie uchwycić tego miejsca, co czyni te metylowane fragmenty potężnymi naturalnymi antagonistami.
Naturale hamulce z RNA rybosomalnego i mutacje związane z chorobami
Opowieść staje się jeszcze ciekawsza, gdy rozważymy, skąd pochodzą takie fragmenty. Autorzy zauważają, że nasze rybosomy — maszyneria komórkowa budująca białka — są naszpikowane ponad setką znaków 2′‑O‑metylacji, wiele z nich na guanozynie w trzy‑literowych wzorcach odpowiadających najsilniejszym motywom hamującym. Gdy RNA rybosomalne jest rozdrabniane podczas normalnej odnowy komórek, takie fragmenty trafiają do wnętrza komórek odpornościowych. Eksperymenty wykazały, że oczyszczone RNA rybosomalne może tłumić aktywność TLR7 i TLR8, a zmniejszenie aktywności enzymu dodającego metyl — fibrylaryny — osłabia ten efekt. Co więcej, rzadkie ludzkie mutacje znalezione u pacjentów z toczniem lub powiązanymi schorzeniami zmieniają kluczowe aminokwasy w kieszeni antagonistycznej TLR7 lub TLR8. Zmiany te zmniejszają wiązanie zmodyfikowanych fragmentów, poluzowując naturalny hamulec i sprzyjając zapaleniu autoimmunologicznemu.
Implikacje dla szczepionek i terapii autoimmunologicznych
U myszy syntetyczne trzy‑literowe fragmenty zaprojektowane na wzór tych naturalnych motywów skutecznie osłabiały zapalenie zależne od TLR7 w modelach chorób skórnych i zmniejszały zapalne skutki uboczne niemodyfikowanego mRNA dostarczanego w lipidowych nanocząstkach, podobnych do używanych w szczepionkach. Dla osoby niezaznajomionej ze szczegółami kluczowy wniosek jest taki, że nasze komórki stale wytwarzają małe, chemicznie oznakowane fragmenty RNA, które blokują specjalny wyłącznik na istotnych czujnikach odpornościowych, zapobiegając błędnej interpretacji codziennych szczątków komórkowych jako zagrożenia. Gdy ten wyłącznik zostaje osłabiony — przez mutację genetyczną lub być może przez zaburzone przetwarzanie RNA — układ odpornościowy częściej błądzi, atakując własne ciało. Zrozumienie i wykorzystanie tych naturalnych „hamulców” RNA może pomóc w projektowaniu bezpieczniejszych szczepionek i nowych terapii chorób autoimmunologicznych.
Cytowanie: Alharbi, A.S., Sapkota, S., Zhang, Z. et al. 2′-O-Methyl-guanosine RNA fragments antagonize TLR7 and TLR8 to limit autoimmunity. Nat Immunol 27, 762–775 (2026). https://doi.org/10.1038/s41590-026-02429-2
Słowa kluczowe: odporność wrodzona, receptory Toll‑podobne, modyfikacje RNA, autoimmunizacja, RNA rybosomalne