Clear Sky Science · pt
Fragmentos de RNA com 2′-O-metil‑guanosina antagonizam TLR7 e TLR8 para limitar a autoimunidade
Por que nosso sistema imune precisa distinguir amigo de inimigo
Todos os dias, nossos corpos removem silenciosamente bilhões de células moribundas sem provocar inflamação prejudicial. Ao mesmo tempo, o sistema imunológico precisa estar pronto para atacar vírus e bactérias, muitos dos quais carregam material genético parecido com o nosso. Este trabalho revela um mecanismo de segurança embutido que ajuda os sensores imunológicos a evitar reações exageradas ao RNA próprio do corpo, oferecendo novas pistas sobre por que algumas pessoas desenvolvem doenças autoimunes como lúpus e como poderíamos projetar melhores vacinas e medicamentos anti‑inflamatórios.
Guardas que escutam sinais de perigo
Lá dentro das células imunológicas existem dois “postos de escuta” moleculares chamados TLR7 e TLR8. Eles patrulham pequenas vesículas de membrana que englobam pedaços de RNA de vírus, bactérias ou células moribundas. Quando esses receptores detectam o tipo certo de fragmentos curtos de RNA, mudam para uma conformação ativa e desencadeiam a produção de moléculas antivirais e inflamatórias. Se responderem de forma muito fraca, infecções como COVID‑19 grave podem tornar‑se potencialmente fatais; se dispararem com facilidade excessiva, o sistema imune pode atacar tecidos saudáveis. Até agora, os pesquisadores não entendiam totalmente como esses sensores ignoram o fluxo de fragmentos de RNA inofensivos produzidos quando o corpo recicla discretamente suas próprias células.
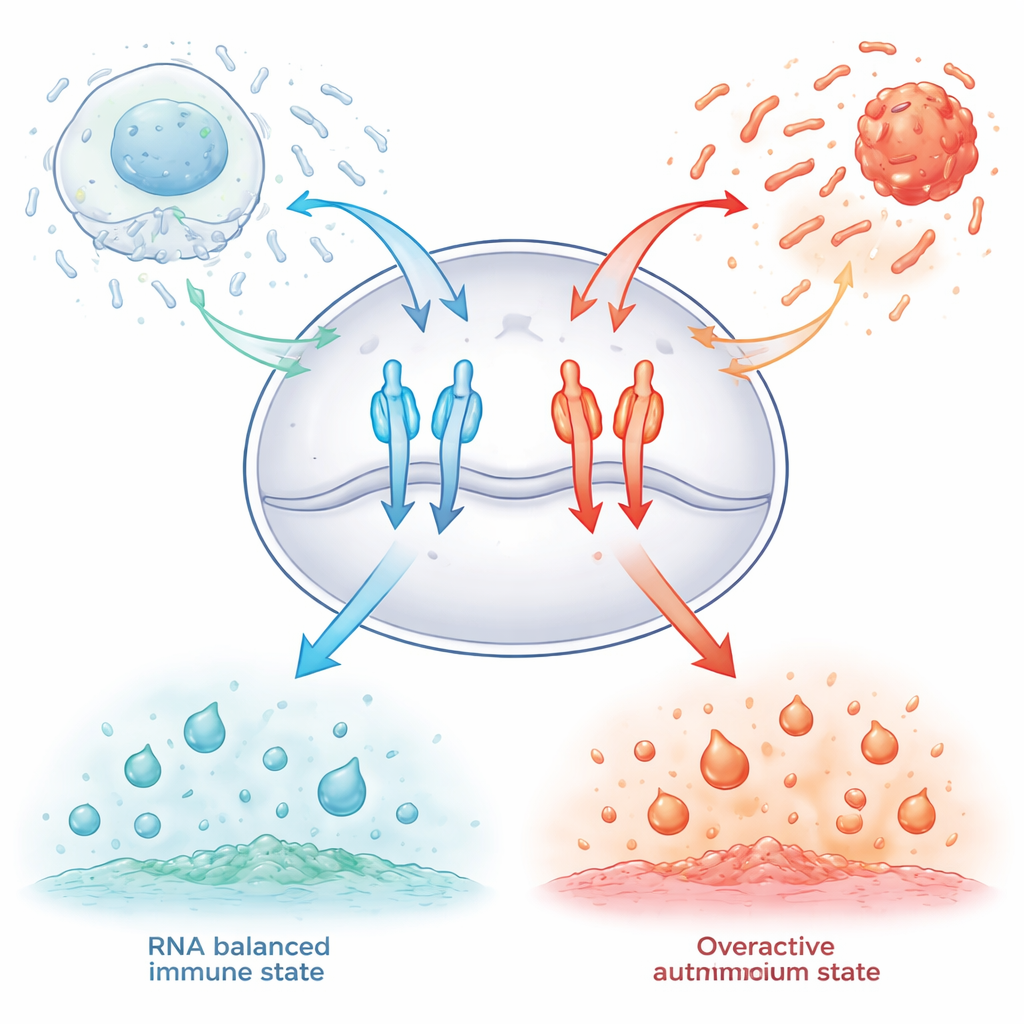
Fragmentos especiais de RNA que atuam como freios moleculares
Os autores focaram em pedaços muito curtos de RNA, de três nucleotídeos, que carregam uma modificação química sutil: um grupo metil no açúcar da base guanosina, conhecido como 2′‑O‑metil‑guanosina. Ao testar sistematicamente todas as 64 combinações possíveis de três letras em células humanas geneticamente modificadas para expressar TLR7 ou TLR8, descobriram que fragmentos que começam com essa guanosina modificada podem suprimir fortemente a atividade dos receptores. Algumas combinações silenciaram o TLR7, outras o TLR8, e algumas até aumentaram as respostas do TLR8, mostrando que a sequência exata ajusta como esses interruptores imunológicos se comportam. Importante, esses pequenos fragmentos funcionaram não apenas contra estimulantes artificiais semelhantes a drogas, mas também contra agonistas de RNA genuínos de vírus e bactérias, e foram capazes de reduzir a sinalização imune em células sanguíneas humanas.
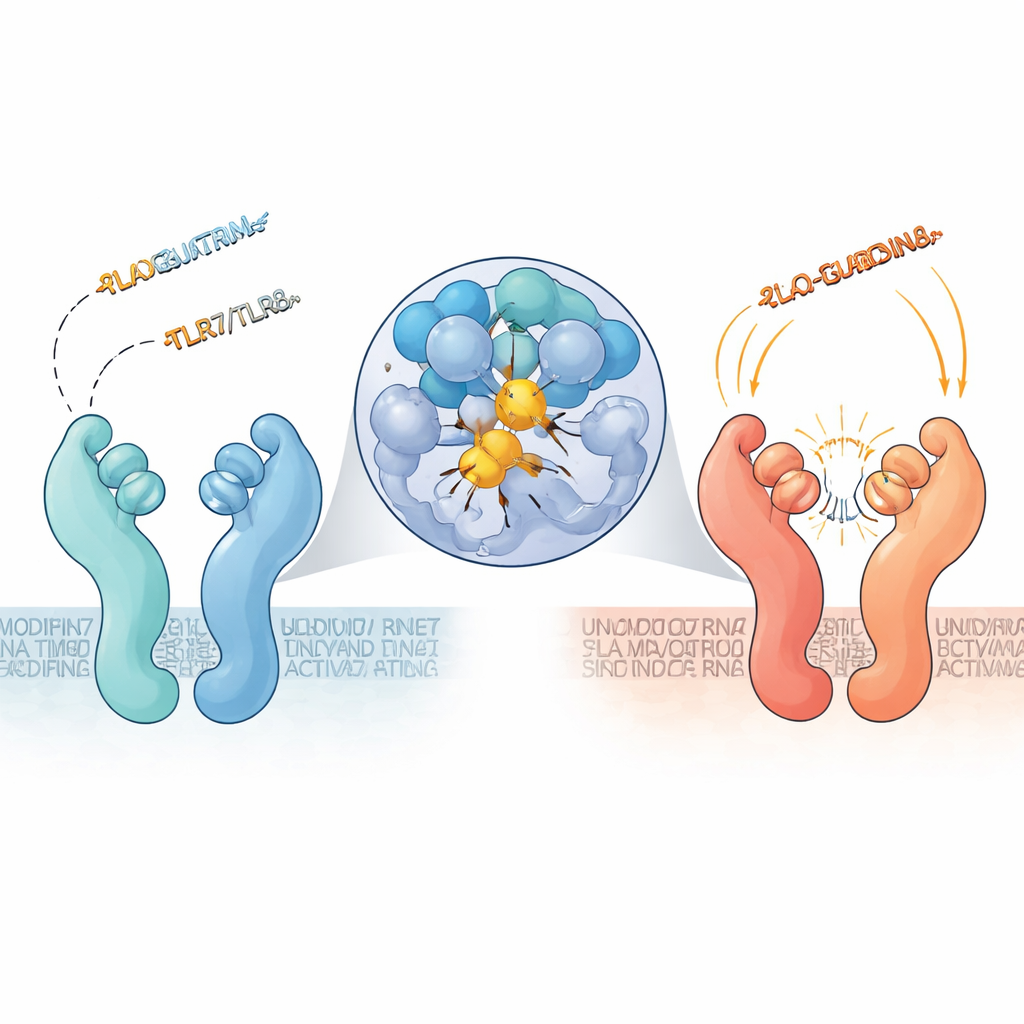
Um bolso de desligamento oculto revelado
Para ver como esses fragmentos atuam, a equipe combinou microscopia avançada com simulações computacionais. Microscopia crioeletrônica de alta resolução mostrou que determinados fragmentos de três letras contendo 2′‑O‑metil‑guanosina se prendem a uma ranhura previamente subestimada formada entre as duas metades da proteína TLR7. Quando esse bolso está preenchido, o receptor permanece em uma conformação “aberta” de repouso que não pode sinalizar, mesmo se RNA ativador estiver presente em outro lugar. A guanosina modificada na frente do fragmento aninha‑se profundamente em um aglomerado de aminoácidos aromáticos, formando interações de empilhamento e pontes de hidrogênio apertadas. O RNA comum, não modificado, não consegue se fixar nesse sítio quase tão bem, tornando esses fragmentos metilados antagonistas naturais poderosos.
Freios naturais do RNA ribossômico e mutações associadas a doenças
A história fica ainda mais intrigante ao considerar de onde esses fragmentos vêm. Os autores apontam que nossos ribossomos — as máquinas celulares que sintetizam proteínas — estão repletos de mais de cem marcas 2′‑O‑metil, muitas delas em guanosina em padrões de três letras que correspondem aos melhores motivos inibitórios. Quando o RNA ribossômico é fragmentado durante a renovação celular normal, esses pedaços aparecem dentro das células imunológicas. Experimentos mostraram que RNA ribossômico purificado pode suprimir a atividade de TLR7 e TLR8, e que reduzir a enzima que adiciona metil (fibrilarina) enfraquece esse efeito. Além disso, mutações humanas raras encontradas em pacientes com lúpus ou condições relacionadas alteram aminoácidos-chave no bolso antagonista do TLR7 ou TLR8. Essas mudanças reduzem a ligação dos fragmentos modificados, afrouxando o freio natural e promovendo inflamação autoimune.
Implicações para vacinas e terapias autoimunes
Em camundongos, fragmentos sintéticos de três letras projetados para imitar esses motivos naturais conseguiram reduzir a inflamação mediada por TLR7 em modelos de doença de pele e diminuíram os efeitos inflamatórios de um mRNA não modificado entregue em nanopartículas lipídicas, semelhante às usadas em vacinas. Para um leitor não especialista, a mensagem principal é que nossas células geram constantemente pequenos pedaços de RNA quimicamente marcados que acionam um desligamento especial em sensores imunes-chave, impedindo que eles interpretem erroneamente detritos celulares cotidianos como uma ameaça. Quando esse interruptor de desligamento é enfraquecido — por mutação genética ou talvez por processamento de RNA desequilibrado — o sistema imune tem maior probabilidade de reagir contra o próprio corpo. Compreender e aproveitar esses “freios” naturais de RNA pode ajudar a projetar vacinas mais seguras e novos tratamentos para doenças autoimunes.
Citação: Alharbi, A.S., Sapkota, S., Zhang, Z. et al. 2′-O-Methyl-guanosine RNA fragments antagonize TLR7 and TLR8 to limit autoimmunity. Nat Immunol 27, 762–775 (2026). https://doi.org/10.1038/s41590-026-02429-2
Palavras-chave: imunidade inata, receptores Toll‑like, modificações do RNA, autoimunidade, RNA ribossômico