Clear Sky Science · es
Fragmentos de ARN con 2′-O‑metil‑guanosina antagonizan TLR7 y TLR8 para limitar la autoinmunidad
Por qué nuestro sistema inmunitario debe distinguir amigo de enemigo
Cada día, nuestros cuerpos eliminan silenciosamente miles de millones de células en descomposición sin provocar inflamación dañina. Al mismo tiempo, el sistema inmunitario debe estar preparado para atacar virus y bacterias, muchos de los cuales llevan material genético similar al nuestro. Este artículo descubre un mecanismo de seguridad incorporado que ayuda a los sensores inmunitarios a evitar reaccionar en exceso ante el ARN propio del organismo, ofreciendo nuevas pistas sobre por qué algunas personas desarrollan enfermedades autoinmunes como el lupus y cómo podríamos diseñar mejor vacunas y fármacos antiinflamatorios.
Guardianes que escuchan señales de peligro
En el interior de las células inmunitarias se encuentran dos “puestos de escucha” moleculares llamados TLR7 y TLR8. Vigilan pequeñas burbujas membranosas que engullen fragmentos de ARN procedentes de virus, bacterias o células en descomposición. Cuando estos receptores detectan el tipo correcto de fragmentos cortos de ARN, adoptan una conformación activa y desencadenan la producción de moléculas antivirales e inflamatorias. Si responden con poca intensidad, infecciones como la COVID‑19 grave pueden convertirse en potencialmente mortales; si se activan con demasiada facilidad, el sistema inmunitario puede atacar tejidos sanos. Hasta ahora, los investigadores no comprendían del todo cómo estos sensores ignoran la avalancha de fragmentos de ARN inocuos que se generan cuando el organismo recicla sus propias células.
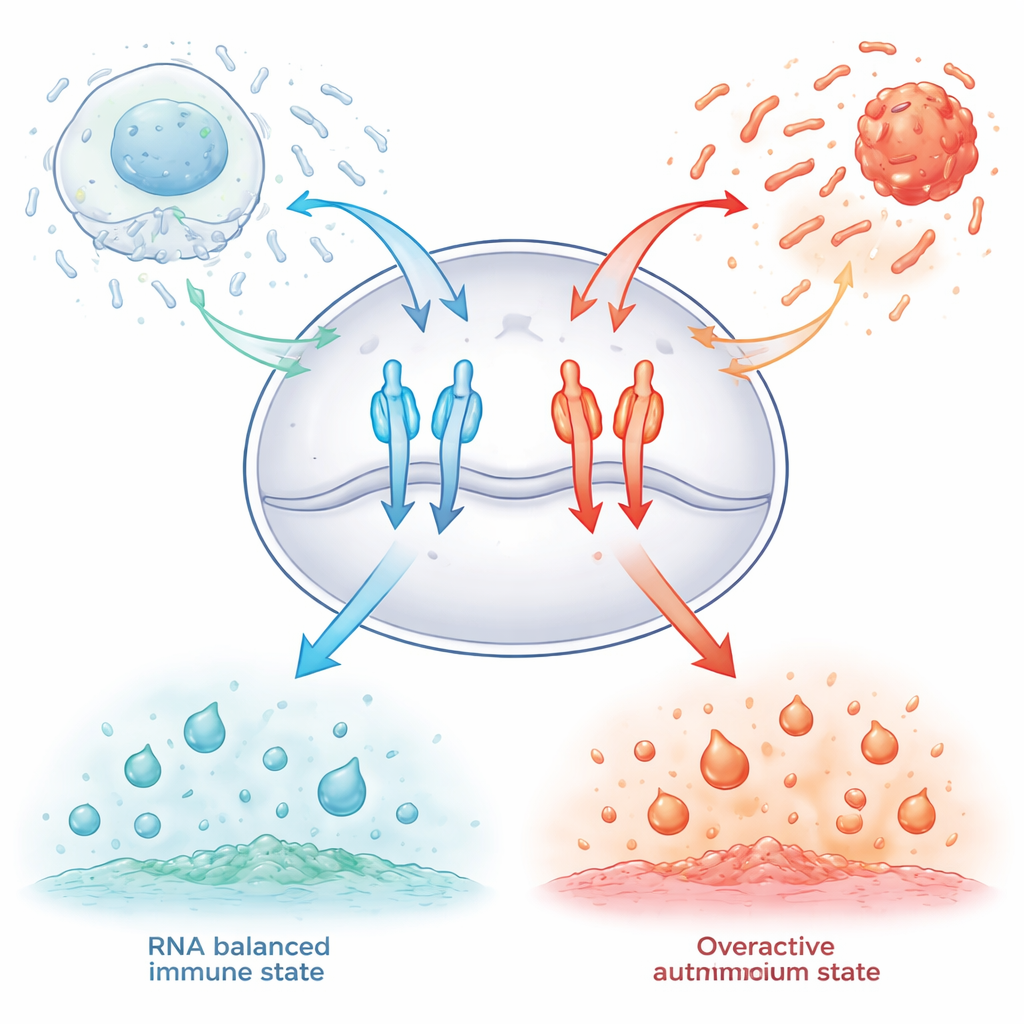
Fragmentos de ARN especiales que actúan como frenos moleculares
Los autores se centraron en piezas de ARN muy cortas, de tres letras, que llevan una sutil modificación química: un grupo metilo en el azúcar de una base guanosina, conocido como 2′‑O‑metil‑guanosina. Al probar sistemáticamente las 64 combinaciones posibles de tres letras en células humanas modificadas para expresar TLR7 o TLR8, hallaron que los fragmentos que comienzan con esta guanosina modificada pueden atenuar fuertemente la actividad de los receptores. Algunas combinaciones silenciaron TLR7, otras TLR8, y unas pocas incluso potenciaron las respuestas de TLR8, lo que demuestra que la secuencia exacta ajusta finamente el comportamiento de estos interruptores inmunitarios. Importante: estos pequeños fragmentos funcionaron no solo frente a estimulantes sintéticos tipo fármaco, sino también contra agonistas auténticos de ARN procedentes de virus y bacterias, y pudieron reducir la señalización inmune en células sanguíneas humanas.
Un bolsillo oculto que actúa como interruptor de apagado
Para entender cómo actúan estos fragmentos, el equipo combinó microscopía avanzada con simulaciones por ordenador. La crio‑microscopía electrónica de alta resolución mostró que determinados fragmentos de tres letras que contienen 2′‑O‑metil‑guanosina se anclan en una hendidura hasta ahora poco apreciada formada entre las dos mitades de la proteína TLR7. Cuando este bolsillo se ocupa, el receptor permanece en una conformación “abierta” en reposo que no puede señalizar, incluso si hay ARN activador en otra parte. La guanosina modificada en el extremo del fragmento se inserta profundamente en un racimo de aminoácidos aromáticos, formando apilamientos ajustados e interacciones por puentes de hidrógeno. El ARN ordinario, sin modificar, no puede sujetar este sitio casi tan bien, lo que convierte a estos fragmentos metilados en potentes antagonistas naturales.
Frenos naturales procedentes del ARN ribosómico y mutaciones asociadas a la enfermedad
La historia resulta aún más interesante al considerar el origen de estos fragmentos. Los autores señalan que nuestros ribosomas —las máquinas celulares que construyen proteínas— están repletos de más de cien marcas 2′‑O‑metil, muchas sobre guanosina en patrones de tres letras que coinciden con los motivos inhibidores más eficaces. Cuando el ARN ribosómico se fragmenta durante el recambio normal de células, estos fragmentos aparecen dentro de las células inmunitarias. Experimentos mostraron que el ARN ribosómico purificado puede suprimir la actividad de TLR7 y TLR8, y que reducir la enzima que añade metilos, fibrilarina, debilita este efecto. Además, raras mutaciones humanas encontradas en pacientes con lupus o afecciones relacionadas alteran aminoácidos clave en el bolsillo antagonista de TLR7 o TLR8. Estos cambios reducen la unión de los fragmentos modificados, aflojando el freno natural y promoviendo la inflamación autoinmune.
Implicaciones para vacunas y terapias contra la autoinmunidad
En ratones, fragmentos sintéticos de tres letras diseñados para imitar estos motivos naturales atenuaron con éxito la inflamación impulsada por TLR7 en modelos de enfermedad cutánea y redujeron los efectos inflamatorios secundarios de un ARN mensajero no modificado administrado en nanopartículas lipídicas, similares a las usadas en vacunas. Para un público no especializado, la idea esencial es que nuestras células generan constantemente pequeños fragmentos de ARN con marcas químicas que acoplan un interruptor de apagado especial en sensores inmunitarios clave, impidiendo que interpreten erróneamente los desechos celulares cotidianos como una amenaza. Cuando ese interruptor de apagado se debilita —por mutación genética o quizá por un procesamiento del ARN desequilibrado—, el sistema inmunitario tiene más probabilidades de fallar y atacar al propio organismo. Comprender y aprovechar estos “frenos” naturales de ARN podría ayudar a diseñar vacunas más seguras y nuevos tratamientos para enfermedades autoinmunes.
Cita: Alharbi, A.S., Sapkota, S., Zhang, Z. et al. 2′-O-Methyl-guanosine RNA fragments antagonize TLR7 and TLR8 to limit autoimmunity. Nat Immunol 27, 762–775 (2026). https://doi.org/10.1038/s41590-026-02429-2
Palabras clave: inmunidad innata, receptores tipo Toll, modificaciones del ARN, autoinmunidad, ARN ribosómico