Clear Sky Science · sv
Persistens av alveolära fibroblast‑härledda ADAMTS4+-celler i en preklinisk modell för fördröjd upplösning av pulmonell fibros
Varför lungsårvävnad spelar roll
När lungor skadas kan de läka med ärrvävnad, på samma sätt som huden efter ett djupt skärsår. Hos vissa personer, särskilt äldre vuxna, löper denna ärrbildning amok och förhårdnar lungorna, ett tillstånd som kallas idiopatisk pulmonell fibros. Andningen blir allt svårare och skadan återställs sällan. Denna studie ställer en skenbart enkel fråga med stora medicinska konsekvenser: varför bleknar lungsår i vissa situationer men består envist i andra, och kan vi styra lungan tillbaka mot läkning istället för permanent ärrbildning? 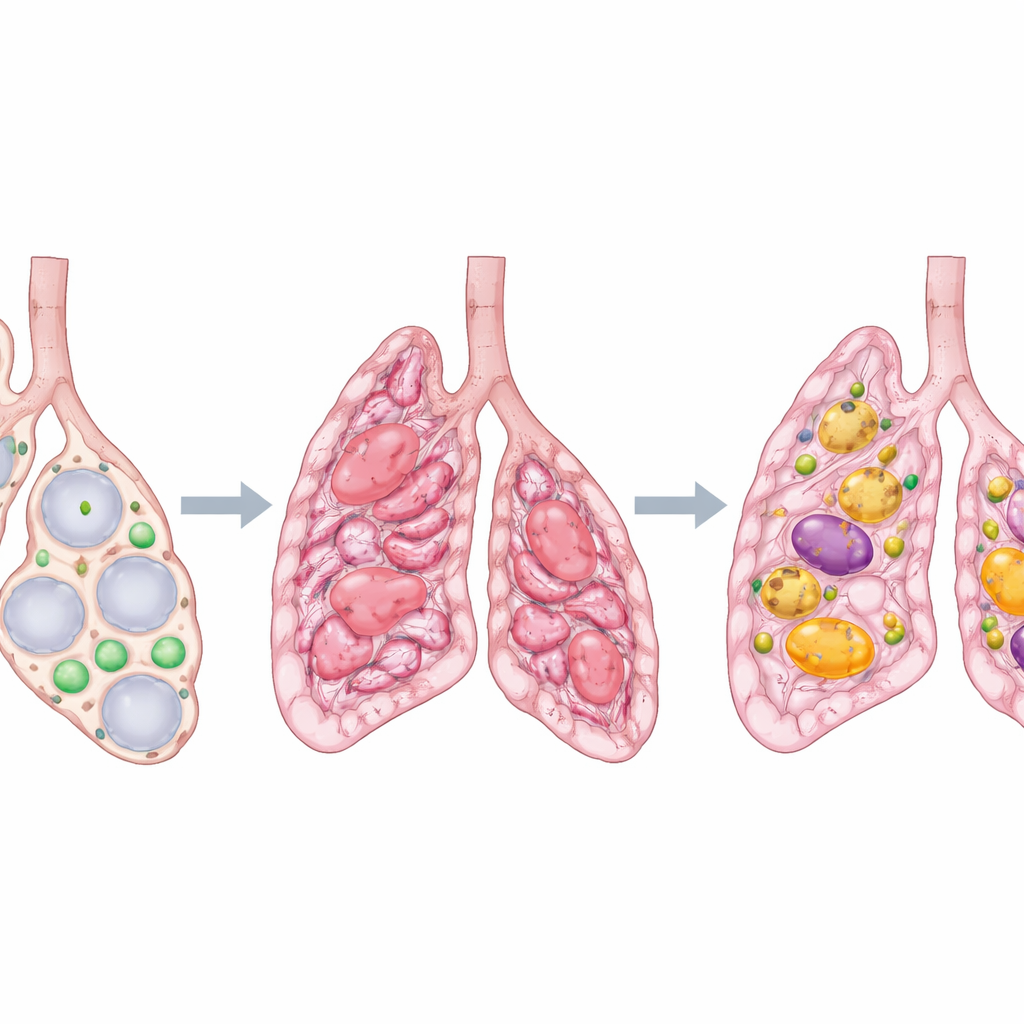
Gömda hjälpare i luftblåsorna
Långt inne i lungans små luftblåsor finns speciella stödjeceller som lever intill de celler som ansvarar för gasutbyte. Dessa stödjeceller, kallade lipofibroblaster, lagrar fettkorn och hjälper till att hålla luftblåsorna friska. Tidigare arbete visade att när lungan skadas kan lipofibroblaster omvandlas till myofibroblaster—celler som drar samman vävnader och lägger ner tjocka fibrer och bildar ärrvävnad. Hos unga möss kan många av dessa ärrbildande celler senare växla tillbaka till lipofibroblaster och bidra till att lungans struktur återhämtar sig. Men vid mänsklig sjukdom verkar denna återgång misslyckas och ärret fortsätter att växa.
Studera ärrbildning i åldrande lungor
För att bättre efterlikna mänsklig sjukdom använde forskarna äldre möss och följde lipofibroblast‑relaterade celler över tid efter en kemisk skada som orsakar lungfibros. Med avancerad mikroskopi och enkelcells‑RNA‑sekvensering följde de hur dessa celler ändrade identitet under maximal ärrbildning och senare under återhämtningsfaser. De fann att lipofibroblaster faktiskt omvandlas till myofibroblaster under aktiv ärrbildning, och att några senare återvänder och hjälper till att återbygga en mer normal vävnad. Denna återhämtning hos åldrade möss var dock långsam och ofullständig, vilket lämnade kvar fläckar av skadad lunga även efter strukturella förbättringar. 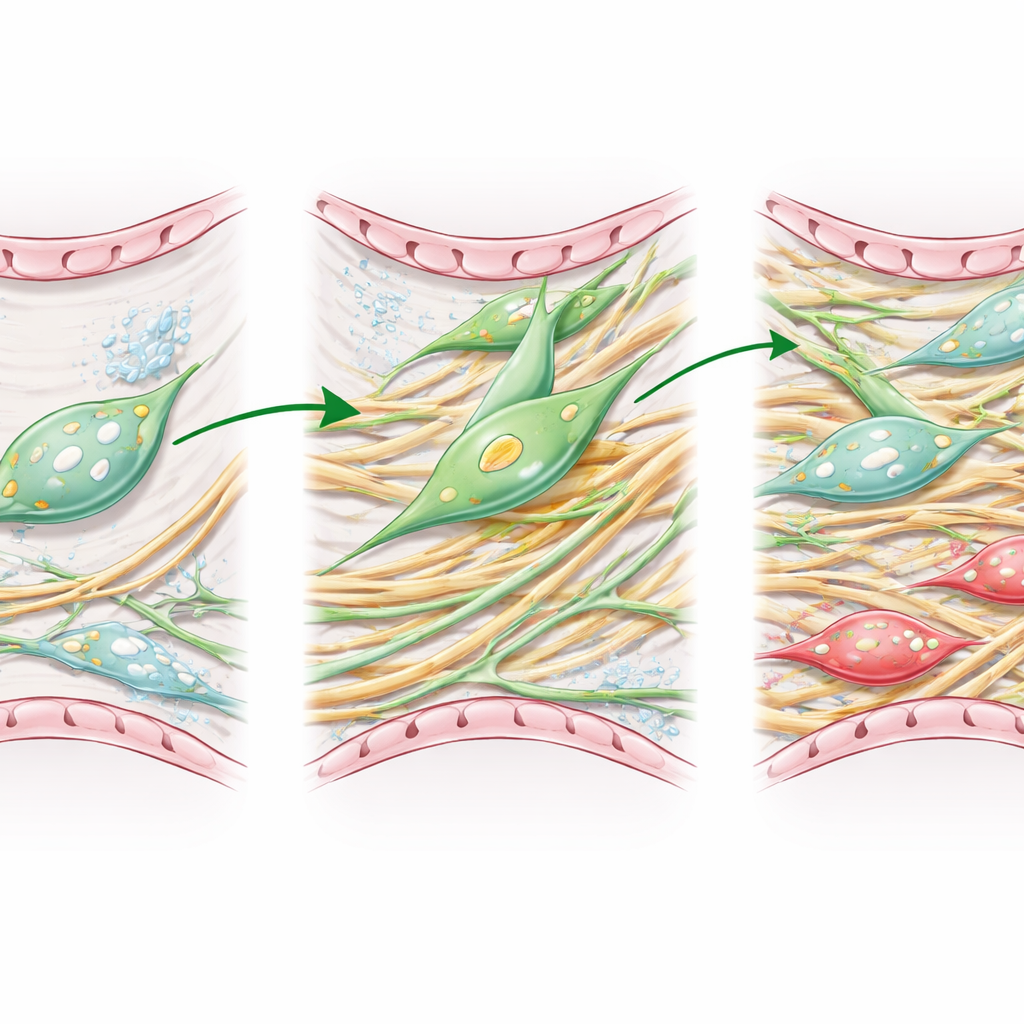
En persistenta störande celltyp
Genom att djupdyka i celldata märkte teamet en grupp fibroblast‑härledda celler märkta av ett protein‑kapande enzym kallat ADAMTS4. Dessa ADAMTS4‑positiva celler dök upp när ärr bildades och, avgörande, fanns kvar under den fördröjda läkningsfasen. Istället för att vara de klassiska kontraktila ärrcellerna liknade de mer alveolära stödjeceller men med en skadlig vridning: de bar hög nivå av ADAMTS4, vilket kan klyva en stor matrixmolekyl kallad versican. Denna nedbrytningsprodukt är känd för att locka immunceller och upprätthålla inflammation. Författarna föreslog att dessa persistenta ADAMTS4‑rika celler bidrar till att bevara en skadlig, inflammatorisk miljö som hindrar lungärr från att helt upplösas.
Från muslungor till mänsklig sjukdom
Forskarnas arbete stannade inte vid möss. De undersökte lungvävnad från patienter med idiopatisk pulmonell fibros och jämförde den med friska donationslungor. I de sjuka lungorna var gener kopplade till hälsosam lipofibroblast‑identitet minskade, medan gener kopplade till myofibroblaster och ADAMTS4 var ökade. Enkelcells‑ och rumsliga transkriptomkartor från mänskliga lungor visade färre normala alveolära stödjeceller och fler ADAMTS4‑rika, sårassocierade regioner. I precision‑skurna lungskivor från både möss och människor testade teamet sedan sätt att blockera ADAMTS4‑aktivitet, antingen med en bred naturlig inhibitorprotein (TIMP‑3), extra versican eller små interfererande RNA som minskade ADAMTS4‑produktionen. I samtliga fall minskade ärrmarkörer och markörer för friskare lungvävnad återställdes delvis.
Mot nya sätt att lösa upp lungsår
Enkelt uttryckt visar denna studie att en reversibel växling mellan fett‑lagrande stödjeceller och ärrbildande celler hjälper avgöra om lungfibros förvärras eller lindras. I åldrande lungor dröjer sig en subset av fibroblast‑härledda celler som bär höga nivåer av enzymet ADAMTS4 kvar i skadade områden och verkar låsa lungan i ett tillstånd av kronisk ärrbildning och inflammation. Genom att dämpa ADAMTS4 eller förändra dess interaktion med den omgivande matrixen kunde forskarna mjuka upp dessa ärr i prekliniska modeller. Trots att mer arbete krävs innan behandlingar når patienter, lyfter fynden fram ADAMTS4‑positiva fibroblast‑lika celler som ett lovande mål för att hjälpa lungan att röra sig bort från permanent ärrbildning och tillbaka mot verklig reparation.
Citering: Zabihi, M., Khadim, A., Lingampally, A. et al. Persistence of alveolar fibroblast-derived ADAMTS4+ cells in a preclinical model of delayed pulmonary fibrosis resolution. Nat Commun 17, 4205 (2026). https://doi.org/10.1038/s41467-026-72419-3
Nyckelord: idiopatisk pulmonell fibros, lungfibroblaster, vävnadssklerbildning, åldrande lunga, ADAMTS4