Clear Sky Science · fr
Persistance des cellules ADAMTS4+ dérivées des fibroblastes alvéolaires dans un modèle préclinique de résolution retardée de la fibrose pulmonaire
Pourquoi les cicatrices pulmonaires comptent
Quand les poumons sont blessés, ils peuvent guérir en formant du tissu cicatriciel, un peu comme la peau après une coupure profonde. Chez certaines personnes, en particulier les personnes âgées, cette cicatrisation s’emballe et durcit les poumons, une pathologie appelée fibrose pulmonaire idiopathique. La respiration devient de plus en plus difficile et les lésions se résolvent rarement. Cette étude pose une question apparemment simple mais aux grandes conséquences médicales : pourquoi les cicatrices pulmonaires s’estompent-elles dans certains cas mais persistent-elles obstinément dans d’autres, et peut‑on orienter le poumon vers une guérison plutôt que vers une cicatrisation permanente ? 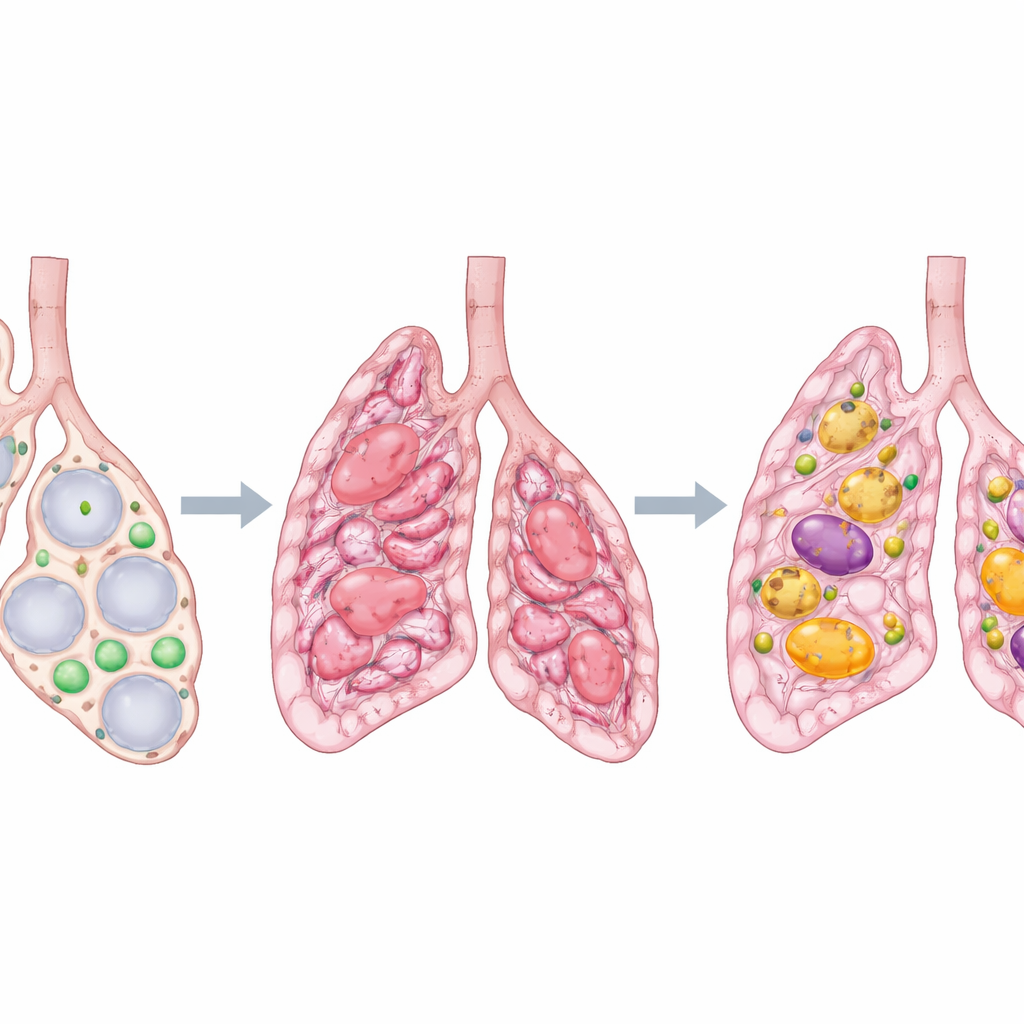
Des aides cachées dans les alvéoles
Au cœur des minuscules alvéoles pulmonaires, des cellules de soutien spéciales vivent à côté des cellules qui assurent les échanges gazeux. Ces cellules de soutien, appelées lipofibroblastes, stockent des gouttelettes de graisse et contribuent à maintenir la santé des alvéoles. Des travaux antérieurs ont montré que, lorsqu’un poumon est blessé, les lipofibroblastes peuvent se transformer en myofibroblastes — des cellules qui contractent les tissus et déposent des fibres épaisses, formant du tissu cicatriciel. Chez les souris jeunes, nombre de ces cellules productrices de cicatrices peuvent ensuite basculer de nouveau en lipofibroblastes, aidant la structure pulmonaire à se rétablir. Mais dans la maladie humaine, ce retour en arrière semble échouer, et la cicatrice continue de s’étendre.
Étudier la cicatrisation dans des poumons vieillissants
Pour mieux reproduire la maladie humaine, les chercheurs ont utilisé des souris âgées et suivi dans le temps les cellules liées aux lipofibroblastes après une lésion chimique provoquant une fibrose pulmonaire. Grâce à une microscopie avancée et au séquençage ARN unicellulaire, ils ont suivi comment ces cellules changeaient d’identité durant le pic de cicatrisation puis lors des phases de récupération. Ils ont constaté que les lipofibroblastes se transforment bien en myofibroblastes pendant la cicatrisation active, et que certains reviennent ensuite en arrière, participant à la reconstruction d’un tissu plus normal. Cependant, cette récupération chez les souris âgées était lente et incomplète, laissant des zones de poumon endommagées malgré des améliorations structurelles. 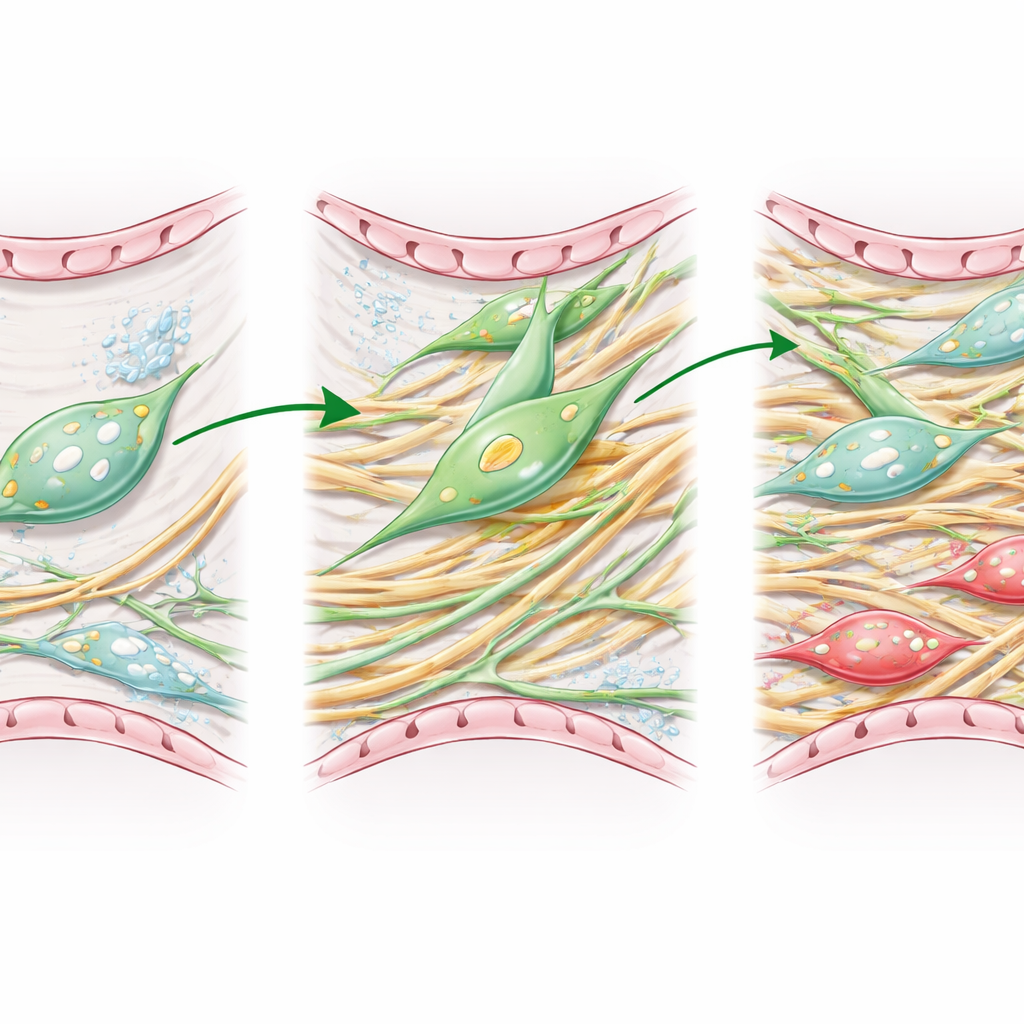
Un type cellulaire perturbateur et persistant
En approfondissant l’analyse cellulaire, l’équipe a repéré un groupe de cellules dérivées de fibroblastes marquées par une enzyme clivant les protéines nommée ADAMTS4. Ces cellules ADAMTS4‑positives sont apparues lors de la formation des cicatrices et, fait crucial, sont restées présentes pendant la phase de guérison retardée. Plutôt que d’être les cellules cicatricielles contractiles classiques, elles ressemblaient davantage aux cellules de soutien alvéolaires mais avec une caractéristique nocive : elles exprimaient fortement ADAMTS4, capable de dégrader une grosse molécule matricielle appelée versican. Ce produit de dégradation attire des cellules immunitaires et entretient l’inflammation. Les auteurs proposent que ces cellules persistantes riches en ADAMTS4 contribuent à maintenir un environnement inflammatoire et délétère qui empêche la résolution complète des cicatrices pulmonaires.
Des poumons de souris à la maladie humaine
Les chercheurs ne se sont pas limités aux souris. Ils ont examiné des tissus pulmonaires de patients atteints de fibrose pulmonaire idiopathique et les ont comparés à des poumons de donneurs sains. Dans les poumons malades, les gènes associés à l’identité des lipofibroblastes sains étaient réduits, tandis que ceux liés aux myofibroblastes et à ADAMTS4 étaient augmentés. Les cartes transcriptomiques unicellulaires et spatiales des poumons humains montraient moins de cellules de soutien alvéolaire normales et davantage de régions associées à la cicatrice riches en ADAMTS4. Dans des tranches de poumon découpées avec précision, issues de souris et d’humains, l’équipe a ensuite testé des moyens de bloquer l’activité d’ADAMTS4, soit avec un inhibiteur naturel large (TIMP‑3), soit avec du versican supplémentaire, soit avec de petits ARN interférents réduisant la production d’ADAMTS4. Dans chaque cas, les marqueurs de cicatrisation diminuaient et des marqueurs de tissu pulmonaire plus sain étaient partiellement restaurés.
Vers de nouvelles façons de dérouler les cicatrices pulmonaires
En bref, cette étude montre qu’un basculement réversible entre des cellules de soutien stockant des graisses et des cellules formant la cicatrice contribue à décider si la fibrose pulmonaire s’aggrave ou s’atténue. Dans les poumons vieillissants, un sous‑ensemble de cellules dérivées de fibroblastes exprimant des niveaux élevés de l’enzyme ADAMTS4 persiste dans les zones endommagées et semble verrouiller le poumon dans un état de cicatrisation chronique et d’inflammation. En diminuant ADAMTS4 ou en modifiant son interaction avec la matrice environnante, les chercheurs ont pu assouplir ces cicatrices dans des modèles précliniques. Bien que des travaux complémentaires soient nécessaires avant d’envisager des traitements pour les patients, ces résultats mettent en lumière les cellules fibroblastiques ADAMTS4‑positives comme une cible prometteuse pour aider le poumon à sortir de la cicatrisation permanente et à retrouver une réparation véritable.
Citation: Zabihi, M., Khadim, A., Lingampally, A. et al. Persistence of alveolar fibroblast-derived ADAMTS4+ cells in a preclinical model of delayed pulmonary fibrosis resolution. Nat Commun 17, 4205 (2026). https://doi.org/10.1038/s41467-026-72419-3
Mots-clés: fibrose pulmonaire idiopathique, fibroblastes pulmonaires, cicatrisation tissulaire, poumon âgé, ADAMTS4