Clear Sky Science · de
Anhaltende ADAMTS4+-Zellen aus alveolären Fibroblasten in einem präklinischen Modell verzögerter Auflösung pulmonaler Fibrose
Warum Lungenvernarbungen wichtig sind
Wenn die Lunge verletzt wird, kann sie mit Narbengewebe heilen, ähnlich wie die Haut nach einer tiefen Schnittwunde. Bei manchen Menschen, vor allem älteren Erwachsenen, gerät diese Vernarbung außer Kontrolle und verhärtet das Lungengewebe — ein Zustand, der als idiopathische pulmonale Fibrose bekannt ist. Das Atmen wird zunehmend schwerer, und die Schäden kehren selten vollständig zurück. Diese Studie stellt eine auf den ersten Blick einfache Frage mit großen medizinischen Folgen: Warum verblassen Lungenvernarbungen in manchen Fällen, bleiben in anderen hartnäckig bestehen, und lässt sich die Lunge eher zur Heilung statt zur dauerhaften Vernarbung bewegen? 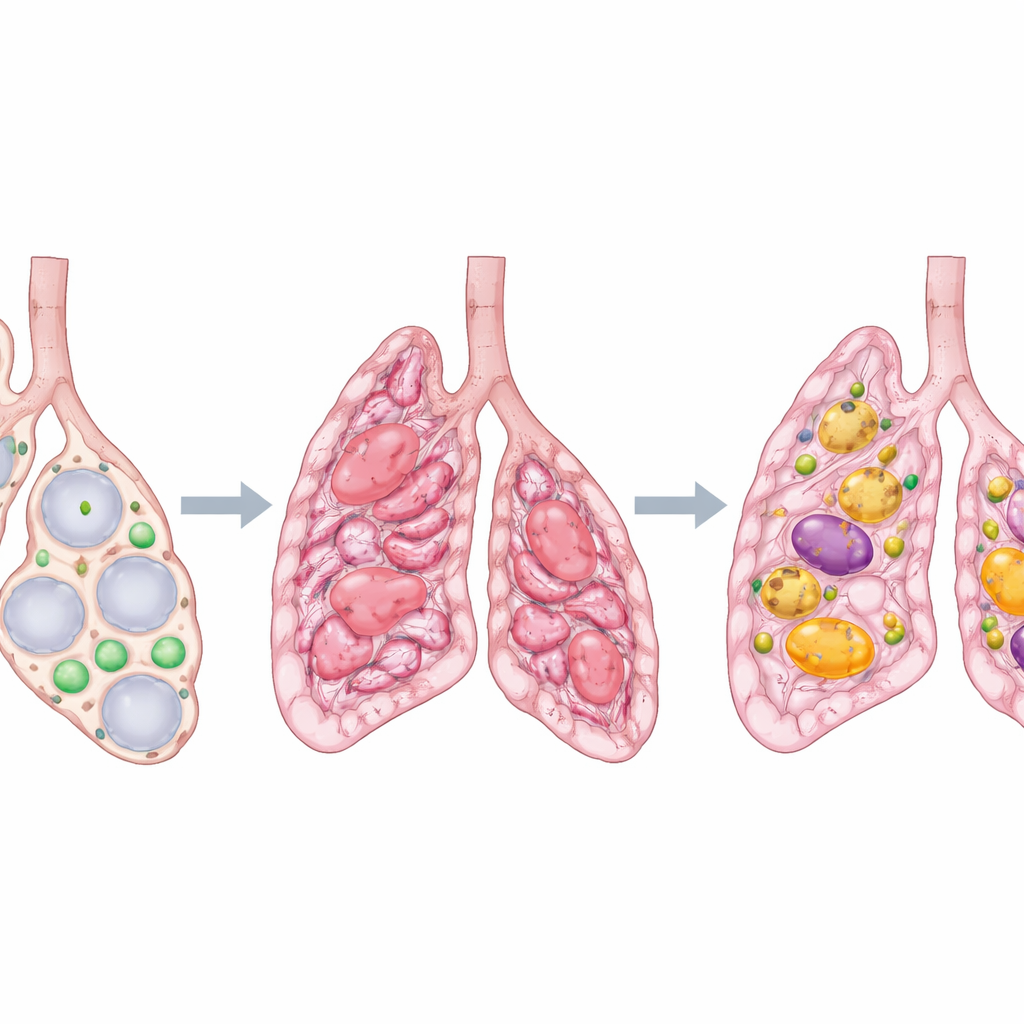
Verborgene Helfer in den Lungenbläschen
Tief in den kleinen Lungenbläschen (Alveolen) leben spezielle Stütz-Zellen neben den Zellen, die den Gasaustausch übernehmen. Diese sogenannten Lipofibroblasten speichern Fetttröpfchen und tragen zur Gesundheit der Alveolen bei. Frühere Arbeiten zeigten, dass sich Lipofibroblasten nach einer Schädigung in Myofibroblasten verwandeln können — Zellen, die Gewebe zusammenziehen und dichte Fasern ablagern und so Narben bilden. Bei jungen Mäusen können viele dieser narbenbildenden Zellen später wieder in Lipofibroblasten zurückschalten und so zur Wiederherstellung der normalen Gewebestruktur beitragen. Bei der menschlichen Erkrankung scheint diese Rückverwandlung jedoch zu versagen, und die Narbe wächst weiter.
Vernarbung in alternden Lungen untersuchen
Um die menschliche Erkrankung besser nachzubilden, verwendeten die Forschenden ältere Mäuse und verfolgten lipofibroblast-verwandte Zellen über die Zeit nach einer chemischen Verletzung, die eine Lungenfibrose auslöst. Mit fortgeschrittener Mikroskopie und Einzelzell-RNA-Sequenzierung beobachteten sie, wie sich diese Zellen in der Phase aktiver Vernarbung und während der späteren Erholungsphasen veränderten. Sie fanden heraus, dass Lipofibroblasten sich tatsächlich in Myofibroblasten verwandeln, und einige später zurückschalten, was beim Wiederaufbau eines normaleren Gewebes hilft. Diese Erholung verlief bei gealterten Mäusen jedoch langsam und unvollständig, sodass nach strukturellen Verbesserungen noch Flecken geschädigter Lunge zurückblieben. 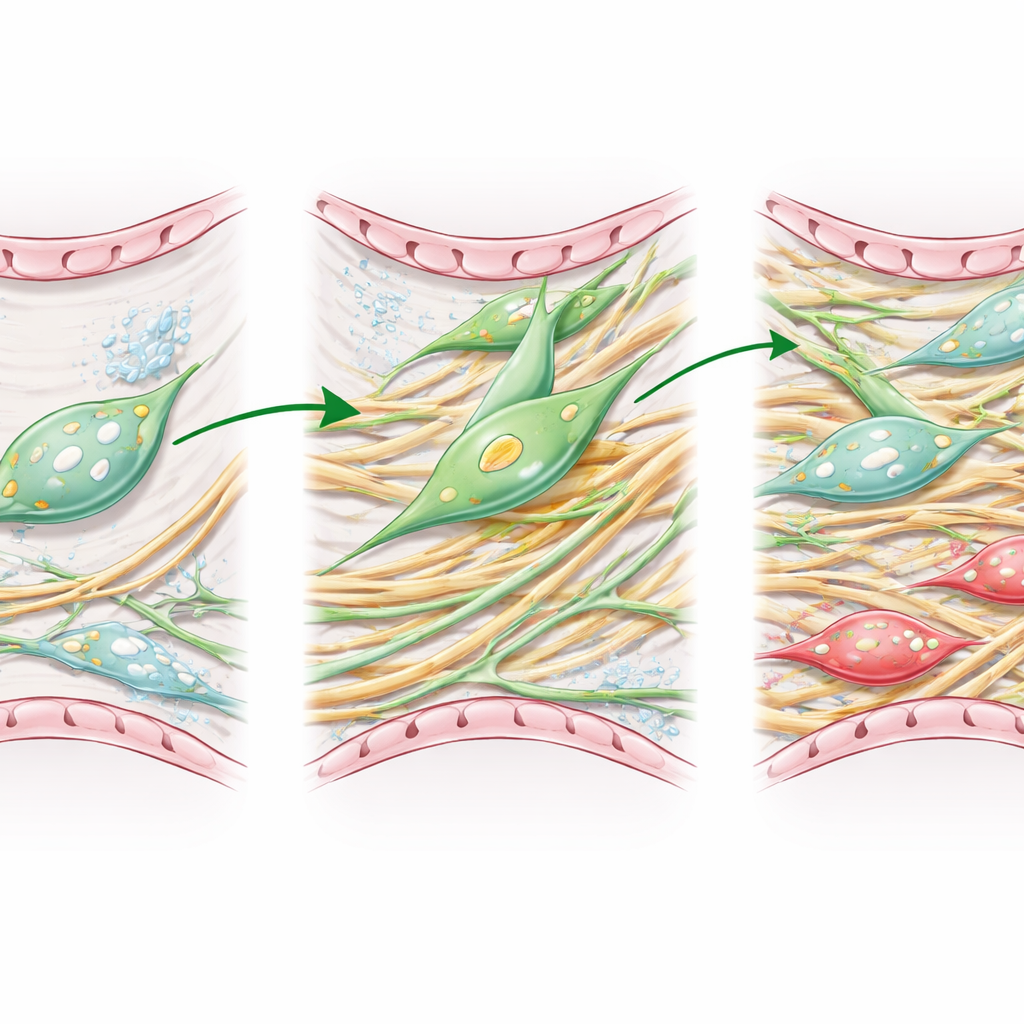
Ein hartnäckiger Störenfried Zelltyp
Bei genauerer Analyse der Zelldaten bemerkte das Team eine Gruppe von fibroblastisch abstammenden Zellen, die durch ein proteinspaltendes Enzym namens ADAMTS4 gekennzeichnet waren. Diese ADAMTS4-positiven Zellen traten während der Narbenbildung auf und blieben entscheidend auch während der verzögerten Heilungsphase bestehen. Statt klassische kontraktile Narbenzellen zu sein, ähnelten sie eher den alveolären Stützzellen, trugen jedoch eine schädliche Besonderheit: hohe ADAMTS4-Werte, die das große Matrixmolekül Versican zerschneiden können. Dieses Abbauprodukt zieht bekanntermaßen Immunzellen an und fördert Entzündungen. Die Autorinnen und Autoren schlagen vor, dass diese persistierenden, ADAMTS4-reichen Zellen eine schädliche, entzündungsfördernde Umgebung aufrechterhalten, die verhindert, dass Lungenvernarbungen vollständig abklingen.
Von Mäuselungen zur menschlichen Erkrankung
Die Forschenden blieben nicht bei Tiermodellen stehen. Sie untersuchten Lungengewebe von Patientinnen und Patienten mit idiopathischer pulmonaler Fibrose und verglichen es mit gesunden Spenderlungen. In den erkrankten Lungen waren Gene, die mit einer gesunden Lipofibroblasten-Identität verknüpft sind, reduziert, während Gene, die Myofibroblasten und ADAMTS4 zugeordnet sind, erhöht waren. Einzelzell- und räumliche Transkriptomkarten menschlicher Lungen zeigten weniger normale alveoläre Stützzellen und mehr ADAMTS4-reiche, narbenassoziierte Regionen. In präzisionsgeschnittenen Lungenpräparaten aus Maus und Mensch testete das Team anschließend Wege, die ADAMTS4-Aktivität zu blockieren — entweder mit einem breit wirkenden natürlichen Inhibitorprotein (TIMP-3), zusätzlichem Versican oder kleinen interfering RNAs, die die ADAMTS4-Produktion reduzierten. In jedem Fall gingen Narbenmarker zurück und Merkmale gesünderer Lungengewebe wurden teilweise wiederhergestellt.
Auf dem Weg zu neuen Methoden, Lungenvernarbungen zu lösen
Kurz gesagt zeigt die Studie, dass ein reversibler Umschaltmechanismus zwischen fett-speichernden Stützzellen und narbenbildenden Zellen mitentscheidet, ob eine Lungenfibrose sich verschlechtert oder abnimmt. In alternden Lungen verbleibt eine Untergruppe fibroblastisch abstammender Zellen mit hohen Pegeln des Enzyms ADAMTS4 in geschädigten Bereichen und scheint die Lunge in einen Zustand chronischer Vernarbung und Entzündung zu verriegeln. Durch das Herunterregulieren von ADAMTS4 oder das Verändern seiner Wechselwirkung mit der umgebenden Matrix konnten die Forschenden diese Narben in präklinischen Modellen aufweichen. Obwohl vor einer Anwendung beim Menschen noch weitere Arbeiten nötig sind, rücken die Ergebnisse ADAMTS4-positive, fibroblastähnliche Zellen als vielversprechendes Ziel in den Fokus, um die Lunge von dauerhafter Vernarbung zurück zu echter Reparatur zu bewegen.
Zitation: Zabihi, M., Khadim, A., Lingampally, A. et al. Persistence of alveolar fibroblast-derived ADAMTS4+ cells in a preclinical model of delayed pulmonary fibrosis resolution. Nat Commun 17, 4205 (2026). https://doi.org/10.1038/s41467-026-72419-3
Schlüsselwörter: idiopathische pulmonale Fibrose, Lungenfibroblasten, Gewebefibrose, alternde Lunge, ADAMTS4