Clear Sky Science · pt
Persistência de células ADAMTS4+ derivadas de fibroblastos alveolares em um modelo pré-clínico de resolução retardada da fibrose pulmonar
Por que as cicatrizes pulmonares importam
Quando os pulmões são lesionados, eles podem cicatrizar, de modo semelhante à pele após um corte profundo. Em algumas pessoas, especialmente em adultos mais velhos, essa cicatrização sai do controle e endurece os pulmões, uma condição conhecida como fibrose pulmonar idiopática. Respirar torna-se progressivamente mais difícil e o dano raramente regride. Este estudo faz uma pergunta aparentemente simples, mas de grandes consequências médicas: por que as cicatrizes pulmonares desaparecem em algumas situações, mas persistem teimosamente em outras, e podemos orientar o pulmão de volta à cura em vez da cicatrização permanente? 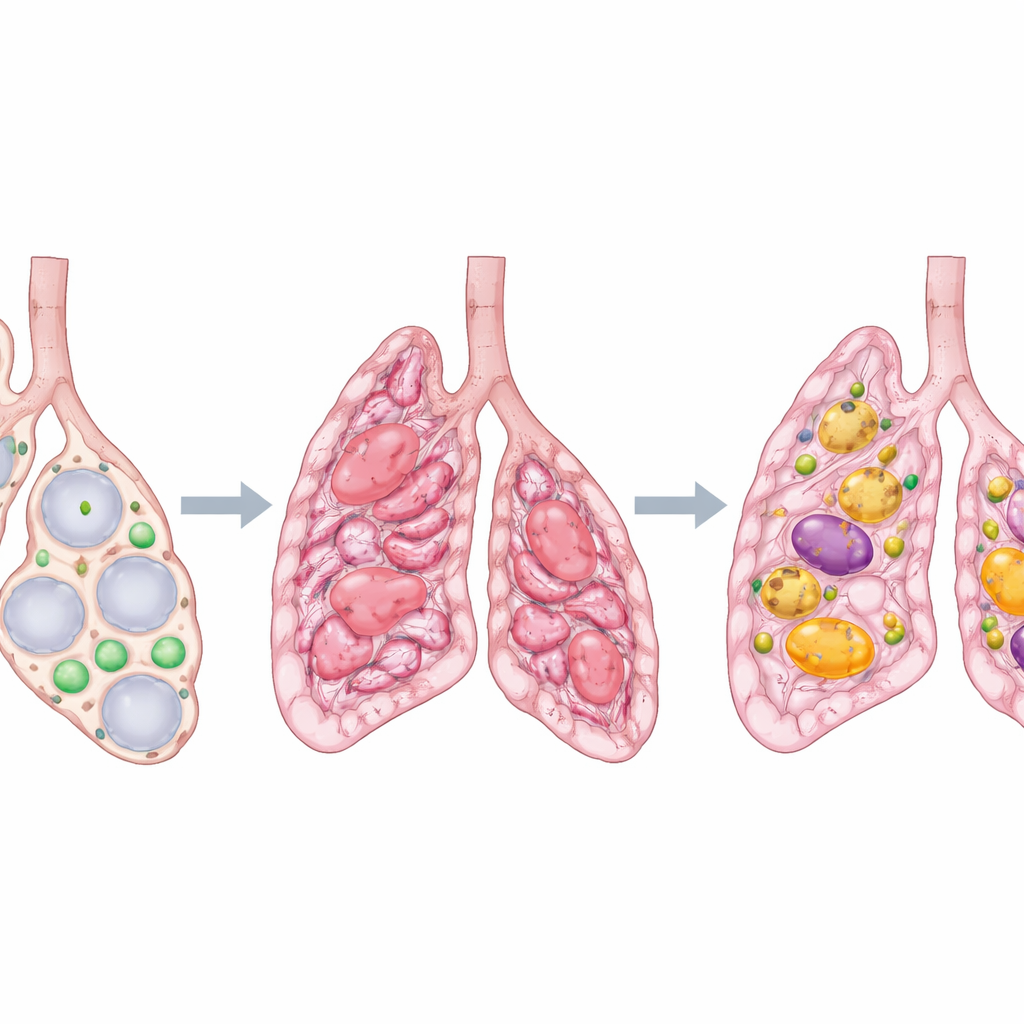
Ajuda oculta nos alvéolos
No interior dos minúsculos sacos de ar do pulmão, células de suporte especiais vivem ao lado das células responsáveis pela troca gasosa. Essas células de suporte, chamadas lipofibroblastos, armazenam gotículas de gordura e ajudam a manter os alvéolos saudáveis. Trabalhos anteriores mostraram que, quando o pulmão é lesionado, lipofibroblastos podem se transformar em miofibroblastos—células que contraem os tecidos e depositam fibras espessas, formando tecido cicatricial. Em camundongos jovens, muitas dessas células formadoras de cicatriz podem depois reverter para lipofibroblastos, ajudando a estrutura pulmonar a se recuperar. Mas na doença humana essa reversão parece falhar, e a cicatriz continua a se expandir.
Estudando a cicatrização em pulmões envelhecidos
Para imitar melhor a doença humana, os pesquisadores usaram camundongos mais velhos e acompanharam células relacionadas a lipofibroblastos ao longo do tempo após uma lesão química que provoca fibrose pulmonar. Com microscopia avançada e sequenciamento de RNA de célula única, seguiram como essas células mudavam de identidade durante o pico da cicatrização e nas fases posteriores de recuperação. Descobriram que os lipofibroblastos realmente se transformam em miofibroblastos durante a cicatrização ativa, e que alguns mais tarde regridem, ajudando a reconstruir um tecido mais próximo do normal. Contudo, essa recuperação em camundongos envelhecidos foi lenta e incompleta, deixando áreas de pulmão danificado mesmo após melhorias estruturais. 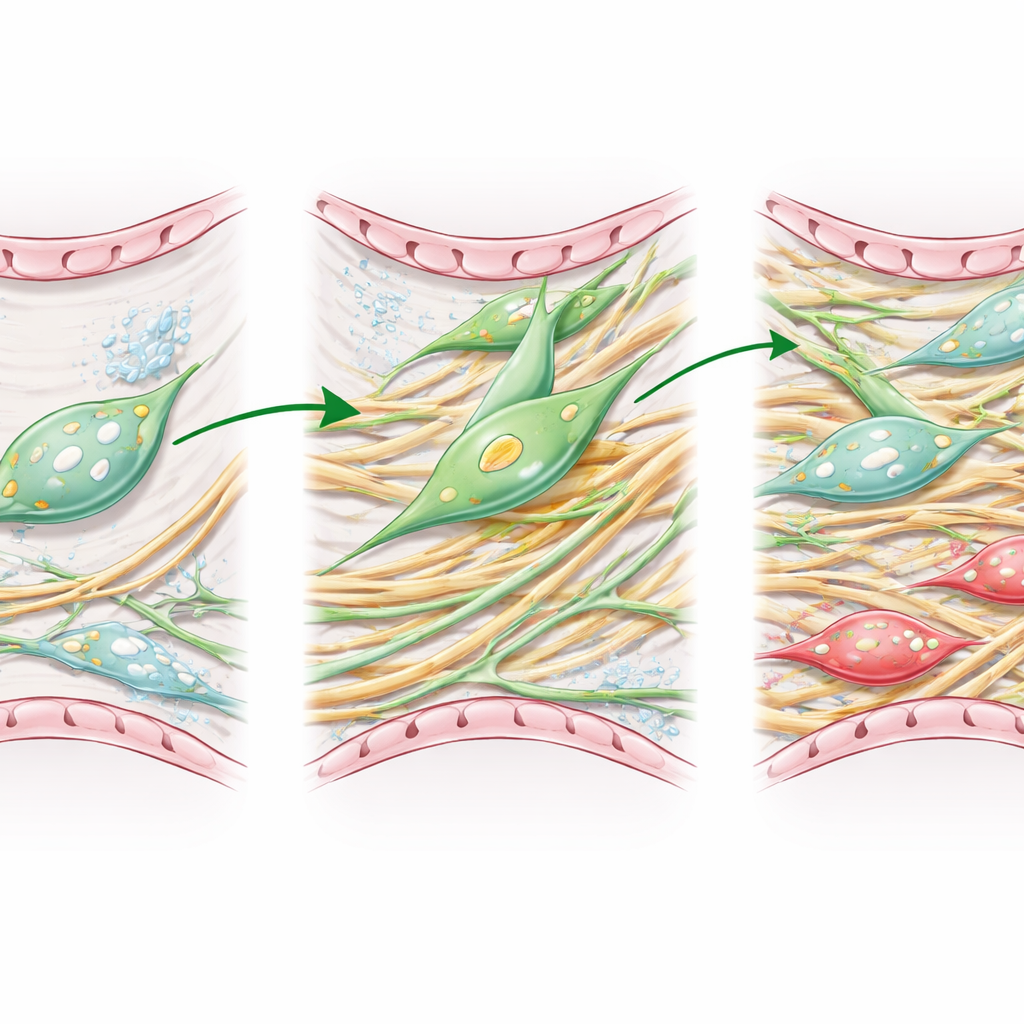
Um tipo de célula problemático e persistente
Aprofundando-se nos dados celulares, a equipe notou um grupo de células derivadas de fibroblastos marcado por uma enzima que corta proteínas chamada ADAMTS4. Essas células ADAMTS4-positivas surgiram quando as cicatrizes se formaram e, crucialmente, permaneceram durante a fase de cicatrização retardada. Em vez de serem as clássicas células contráteis de cicatriz, elas se assemelhavam mais às células de suporte alveolar, porém com uma reviravolta prejudicial: exibiam altos níveis de ADAMTS4, que pode degradar uma grande molécula da matriz chamada versican. Esse produto de degradação é conhecido por atrair células imunes e sustentar a inflamação. Os autores propuseram que essas células persistentes ricas em ADAMTS4 ajudam a manter um ambiente inflamatório e nocivo que impede a resolução completa das cicatrizes pulmonares.
Dos pulmões de camundongo à doença humana
Os pesquisadores não se limitaram aos camundongos. Examinaram tecido pulmonar de pacientes com fibrose pulmonar idiopática e compararam com pulmões de doadores saudáveis. Nos pulmões doentes, genes associados à identidade saudável dos lipofibroblastos estavam reduzidos, enquanto genes ligados a miofibroblastos e ADAMTS4 estavam aumentados. Mapas de transcriptômica de célula única e espacial de pulmões humanos mostraram menos células normais de suporte alveolar e mais regiões associadas à cicatriz ricas em ADAMTS4. Em fatias pulmonares de precisão (precision-cut) de camundongos e humanos, a equipe testou maneiras de bloquear a atividade de ADAMTS4, seja com um inibidor natural amplo (TIMP-3), versican suplementar ou RNA interferente que reduziu a produção de ADAMTS4. Em cada caso, marcadores de cicatrização diminuíram e marcadores de tecido pulmonar mais saudável foram parcialmente restaurados.
Rumo a novas maneiras de desfazer cicatrizes pulmonares
Em termos simples, este estudo mostra que um interruptor reversível entre células de suporte armazenadoras de gordura e células formadoras de cicatriz ajuda a decidir se a fibrose pulmonar piora ou cede. Em pulmões envelhecidos, um subconjunto de células derivadas de fibroblastos com altos níveis da enzima ADAMTS4 persiste em áreas danificadas e parece prender o pulmão em um estado de cicatrização crônica e inflamação. Ao reduzir o ADAMTS4 ou alterar sua interação com a matriz circundante, os pesquisadores conseguiram amolecer essas cicatrizes em modelos pré-clínicos. Embora sejam necessários mais estudos antes que tratamentos cheguem aos pacientes, os achados destacam as células semelhantes a fibroblastos ADAMTS4-positivas como um alvo promissor para ajudar o pulmão a sair da cicatrização permanente e voltar à reparação verdadeira.
Citação: Zabihi, M., Khadim, A., Lingampally, A. et al. Persistence of alveolar fibroblast-derived ADAMTS4+ cells in a preclinical model of delayed pulmonary fibrosis resolution. Nat Commun 17, 4205 (2026). https://doi.org/10.1038/s41467-026-72419-3
Palavras-chave: fibrose pulmonar idiopática, fibroblastos pulmonares, cicatrização tecidual, pulmão envelhecido, ADAMTS4