Clear Sky Science · es
Persistencia de células ADAMTS4+ derivadas de fibroblastos alveolares en un modelo preclínico de resolución retardada de fibrosis pulmonar
Por qué importan las cicatrices pulmonares
Cuando los pulmones se lesionan, pueden curarse formando tejido cicatricial, de modo similar a la piel tras un corte profundo. En algunas personas, especialmente en adultos mayores, esta cicatrización se desboca y endurece los pulmones, una condición conocida como fibrosis pulmonar idiopática. La respiración se vuelve cada vez más difícil y el daño rara vez se revierte. Este estudio plantea una pregunta aparentemente sencilla con grandes consecuencias médicas: ¿por qué las cicatrices pulmonares desaparecen en algunas situaciones pero persisten obstinadamente en otras, y podemos orientar al pulmón hacia la reparación en lugar de la cicatrización permanente? 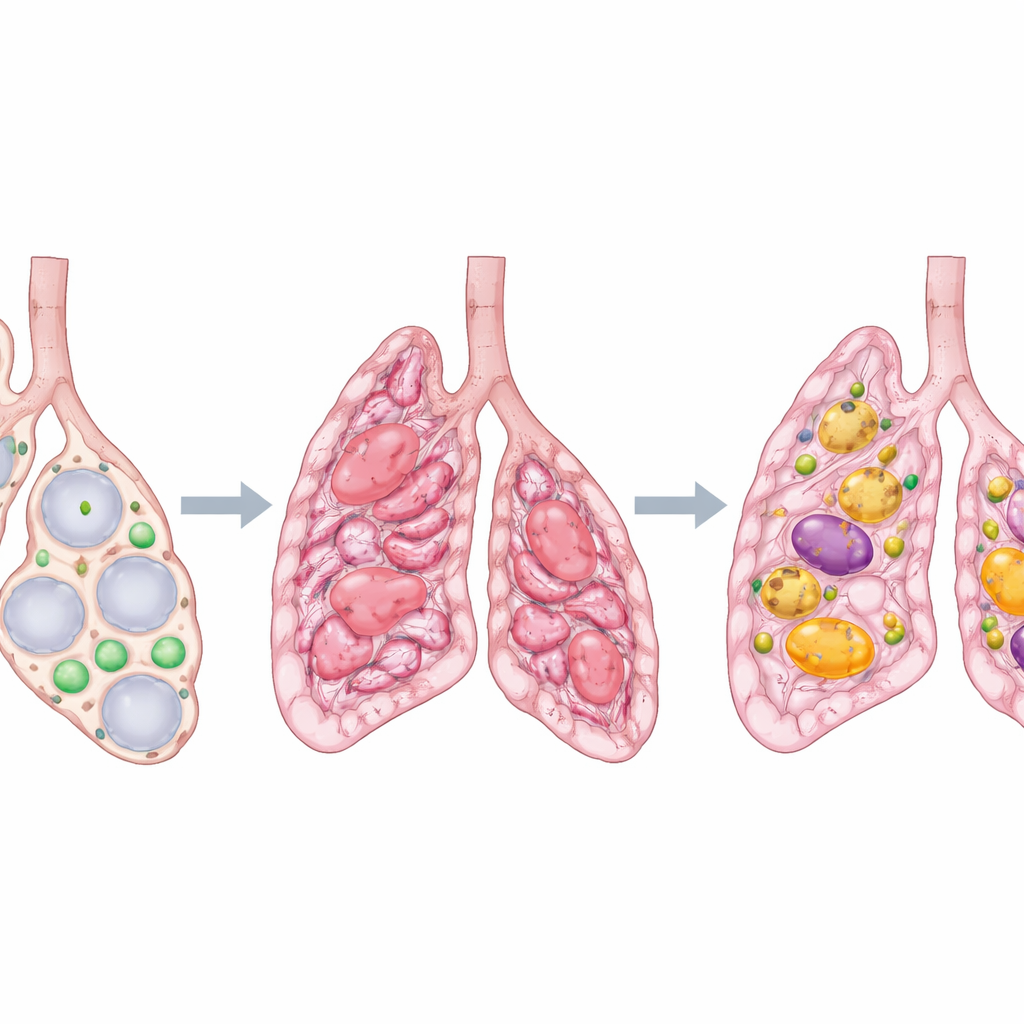
Ayudantes ocultos en los sacos de aire
En lo profundo de los pequeños sacos de aire del pulmón, células de soporte especiales viven junto a las células que realizan el intercambio gaseoso. Estas células de soporte, llamadas lipofibroblastos, almacenan gotas de grasa y contribuyen a mantener la salud de los alvéolos. Trabajos previos mostraron que, cuando el pulmón se lesiona, los lipofibroblastos pueden transformarse en miofibroblastos—células que contraen el tejido y depositan fibras densas, formando tejido cicatricial. En ratones jóvenes, muchas de estas células formadoras de cicatriz pueden después volver a convertirse en lipofibroblastos, ayudando a recuperar la estructura pulmonar. Pero en la enfermedad humana, esta reversión parece fallar y la cicatriz continúa expandiéndose.
Estudiando la cicatrización en pulmones envejecidos
Para imitar mejor la enfermedad humana, los investigadores usaron ratones de edad avanzada y siguieron las células relacionadas con los lipofibroblastos a lo largo del tiempo tras una lesión química que provoca fibrosis pulmonar. Con microscopía avanzada y secuenciación de ARN unicelular, rastrearon cómo cambiaba la identidad de estas células durante el pico de la cicatrización y en las fases posteriores de recuperación. Encontraron que los lipofibroblastos efectivamente se transforman en miofibroblastos durante la cicatrización activa, y que algunos más tarde revierten, ayudando a reconstruir un tejido más normal. Sin embargo, esta recuperación en ratones envejecidos fue lenta e incompleta, dejando parches de pulmón dañados incluso después de mejorías estructurales. 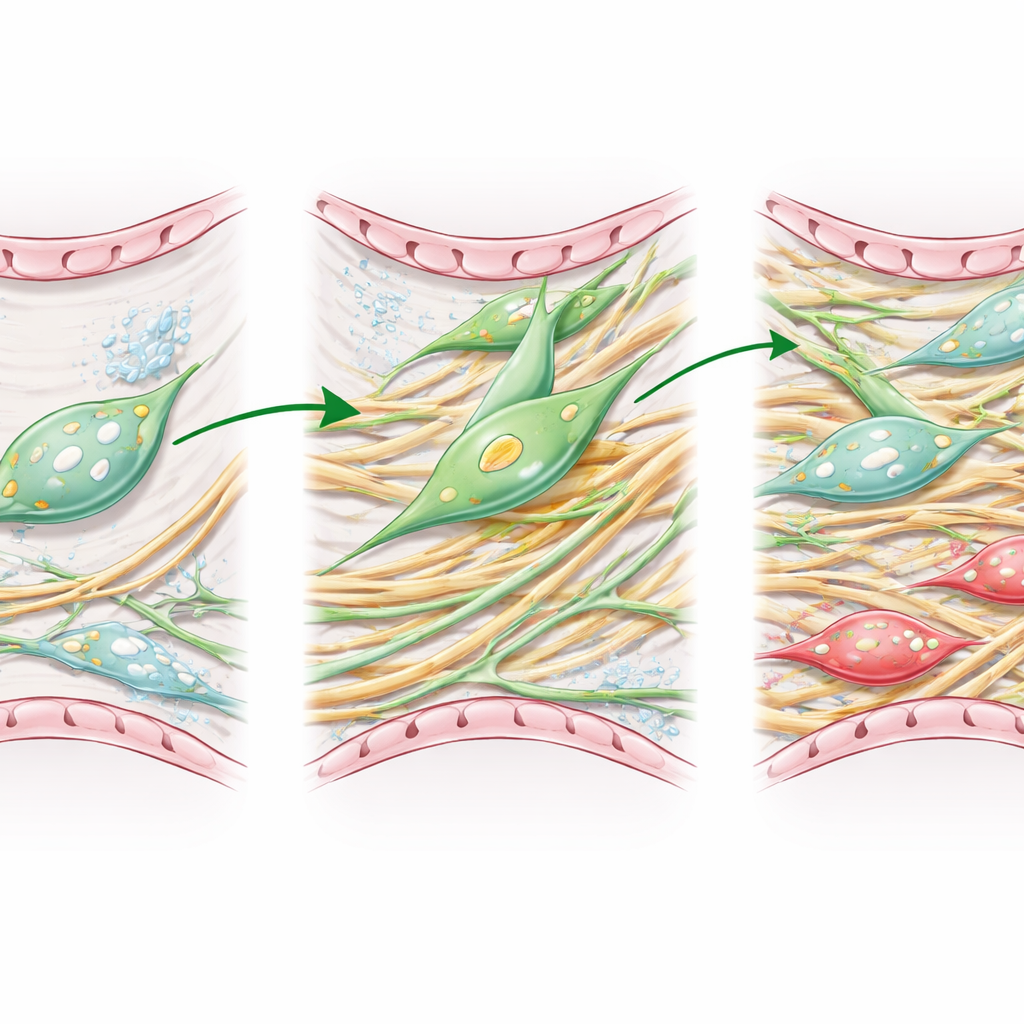
Un tipo celular problemático y persistente
Al profundizar en los datos celulares, el equipo observó un grupo de células derivadas de fibroblastos marcadas por una enzima que corta proteínas llamada ADAMTS4. Estas células ADAMTS4-positivas aparecieron mientras se formaban las cicatrices y, crucialmente, permanecieron durante la fase de curación retardada. Más que ser las clásicas células contráctiles de la cicatriz, se parecían más a las células de soporte alveolar pero con un giro dañino: expresaban altos niveles de ADAMTS4, que puede fragmentar una gran molécula de la matriz llamada versicana. Ese producto de degradación es conocido por atraer células inmunitarias y mantener la inflamación. Los autores propusieron que estas células persistentes ricas en ADAMTS4 ayudan a mantener un entorno inflamatorio perjudicial que impide la resolución completa de las cicatrices pulmonares.
De los pulmones de ratón a la enfermedad humana
Los investigadores no se quedaron solo en ratones. Examinaron tejido pulmonar de pacientes con fibrosis pulmonar idiopática y lo compararon con pulmones de donantes sanos. En los pulmones enfermos, los genes asociados con la identidad de lipofibroblastos saludables estaban reducidos, mientras que los genes vinculados a miofibroblastos y a ADAMTS4 aumentaban. Mapas transcriptómicos unicelulares y espaciales de pulmones humanos mostraron menos células de soporte alveolar normales y más regiones asociadas a cicatrices ricas en ADAMTS4. En cortes de pulmón de precisión tanto de ratones como de humanos, el equipo probó luego estrategias para bloquear la actividad de ADAMTS4, ya fuera con un inhibidor natural amplio (TIMP-3), con versicana extra o con ARN interferente pequeño que reducía la producción de ADAMTS4. En cada caso, los marcadores de cicatrización disminuyeron y los marcadores de tejido pulmonar más sano se restauraron en parte.
Hacia nuevas formas de deshacer las cicatrices pulmonares
En términos simples, este estudio muestra que un interruptor reversible entre células de soporte que almacenan grasa y células formadoras de cicatriz ayuda a decidir si la fibrosis pulmonar empeora o remite. En pulmones envejecidos, un subconjunto de células derivadas de fibroblastos que portan altos niveles de la enzima ADAMTS4 persiste en las áreas dañadas y parece fijar al pulmón en un estado de cicatrización crónica e inflamación. Al disminuir ADAMTS4 o alterar su interacción con la matriz circundante, los investigadores consiguieron ablandar estas cicatrices en modelos preclínicos. Aunque se necesita más trabajo antes de que lleguen tratamientos a los pacientes, los hallazgos señalan a las células fibroblastoides ADAMTS4-positivas como un objetivo prometedor para ayudar al pulmón a alejarse de la cicatrización permanente y volver hacia la reparación real.
Cita: Zabihi, M., Khadim, A., Lingampally, A. et al. Persistence of alveolar fibroblast-derived ADAMTS4+ cells in a preclinical model of delayed pulmonary fibrosis resolution. Nat Commun 17, 4205 (2026). https://doi.org/10.1038/s41467-026-72419-3
Palabras clave: fibrosis pulmonar idiopática, fibroblastos pulmonares, cicatrización tisular, pulmón envejecido, ADAMTS4