Clear Sky Science · sv
Proteomomfattande prediktion av funktionell effekt av missense-varianter med ProteoCast
Varför små mutationer spelar roll för hälsa och sjukdom
Varje människa bär på otaliga små DNA-förändringar, men bara vissa av dessa förändringar stör hur våra proteiner fungerar och bidrar till sjukdom. Att skilja ofarliga skillnader från farliga är en stor utmaning, särskilt nu när vi kan redigera genom med verktyg som CRISPR. Denna studie presenterar ProteoCast, en beräkningsmetod som använder evolutionens egen historia för att förutsäga vilka enkelbokstavsförändringar i proteiner som sannolikt får betydelse, och visar att den i praktiken kan skanna i princip hela en organisms proteinsamling på en gång.

Läsa evolutionens fingeravtryck på proteiner
ProteoCast bygger på en enkel idé: om en viss position i ett protein knappt har förändrats under hundratals miljoner år, är det mer sannolikt att en förändring där idag är skadlig. Författarna matar in varje bananflugeproteinsekvens i stora evolutionära databaser för att samla närbesläktade proteiner från många arter. Med dessa uppskattar ProteoCast hur störande varje möjlig aminosyrasubstitution skulle vara på varje position och skapar ett ”mutationslandskap” för proteinet. Metoden grupperar sedan förutsagda förändringar i tre intuitiva kategorier—neutrala, måttligt påverkande eller starkt påverkande—och märker dessutom varje position i proteinet som antingen tolerant eller känslig för mutationer.
Testa prediktioner i en hel djurart
Teamet tillämpade ProteoCast på i princip hela proteomet hos bananflugan Drosophila melanogaster, vilket omfattade mer än 22 000 proteinformer och ungefär 300 miljoner möjliga missense-mutationer. De jämförde ProteoCasts förutsägelser med nästan 400 000 kända genetiska varianter, inklusive naturliga skillnader i vilda och inavelpopulationer samt experimentellt studerade mutationer kända för att orsaka partiell funktionstapp eller direkt letalitet. ProteoCast flaggade korrekt ungefär 85 % av de letala mutationerna och 73 % av de partiella förlustmutationerna som måttligt eller starkt påverkande, samtidigt som majoriteten av populationsvarianterna klassificerades som neutrala. Med andra ord visade sig mönstret av evolutionär konservering ensam vara mycket informativt för vilka förändringar som skadar organismens fitness.
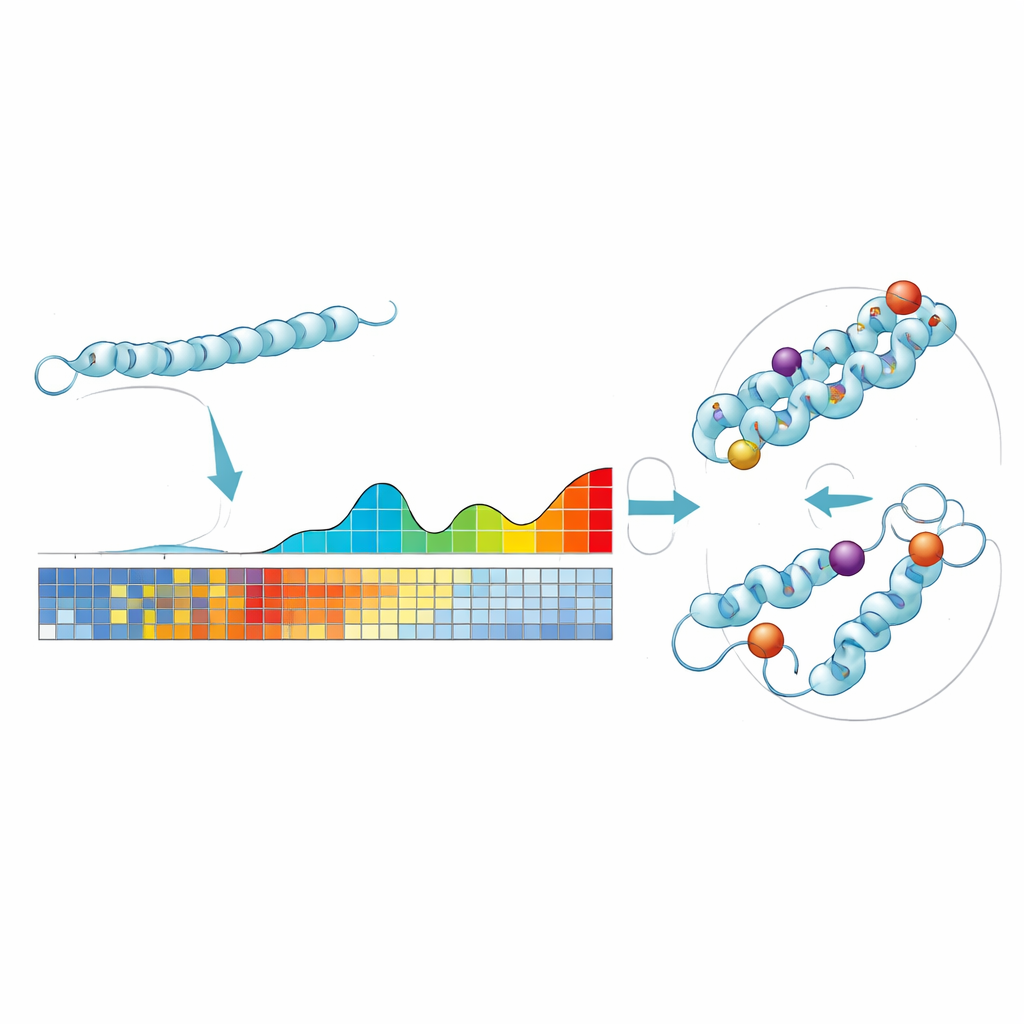
Från datorscorer till verklig genredigering
För att se om ProteoCasts output kan vägleda experiment använde författarna den för att välja specifika enstaka aminosyrasubstitutioner för riktad genredigering i flugor. De koncentrerade sig på ett enzym som är involverat i produktionen av NAD, en viktig metabolisk kofaktor. ProteoCast pekade ut flera substitutioner nära enzymets aktiva yta eller dimergräns som starkt påverkande, och andra substitutioner i ytliga regioner som neutrala, även när de drastiskt ändrade aminosyrans kemi eller storlek. När dessa fem mutationer introducerades med CRISPR orsakade de tre som förutsågs vara skadliga recessiv utvecklingsletalitet, medan de två som förutsågs vara neutrala gav friska flugor, i linje med de beräkningsmässiga prognoserna.
Hitta dolda reglerspakar i svajiga regioner
Många viktiga regleringsställen i proteiner finns i ”ostrukturerade” regioner som svajar omkring istället för att bilda stabila tredimensionella former, vilket gör dem svåra att studera. ProteoCast kartlägger sina mutationspoäng på 3D-modeller från AlphaFold och delar sedan upp varje protein i segment med liknande känslighet. Regioner där en klustring av positioner är ovanligt känsliga motsvarar ofta bindningsmotiv eller hotspotter för post-translationella modifieringar—subtila reglerspakar som justerar ett proteins aktivitet. Över hela flugproteomet överlappade ProteoCasts högkänsliga segment med de flesta kända korta linjära motiven och en stor andel modifieringsställen, och de lyfte också fram tidigare oannoterade segment som sannolikt deltar i reglering eller protein–protein-interaktioner.
Bred påverkan bortom bananflugor
Även om arbetet kretsar kring bananflugor är principen bakom ProteoCast generell: evolutionen kodar rik information om vilka positioner i ett protein som kan förändras utan konsekvenser och vilka som är kritiska. Författarna visar att samma ramverk fungerar väl för mänskliga sjukdomsvarianter och för kurerade uppsättningar av regleringsställen från jäst och intrinsiskt oordnade bindningsregioner. Eftersom metoden är snabb, skalbar och inte kräver dyr hårdvara kan ProteoCast tillämpas på vilken organism som helst med proteinsekvensdata. För icke-specialister är budskapet att genom att låta evolutionen vara experimentören får vi en kraftfull, genomomfattande karta över vilka små genetiska förändringar som mest sannolikt har betydelse för hälsa, sjukdom och framtida terapier.
Citering: Abakarova, M., Freiberger, M.I., Liehrmann, A. et al. Proteome-wide prediction of the functional impact of missense variants with ProteoCast. Nat Commun 17, 3813 (2026). https://doi.org/10.1038/s41467-026-72140-1
Nyckelord: missense-mutationer, proteinevolution, Drosophila, prediktion av varianteffekter, funktionell genomik