Clear Sky Science · es
Predicción a escala proteómica del impacto funcional de variantes missense con ProteoCast
Por qué importan las mutaciones diminutas para la salud y la enfermedad
Cada persona lleva innumerables pequeños cambios en su ADN, pero solo algunos de esos ajustes alteran el funcionamiento de nuestras proteínas y contribuyen a la enfermedad. Distinguir las diferencias inofensivas de las peligrosas es un gran desafío, especialmente ahora que podemos editar genomas con herramientas como CRISPR. Este estudio presenta ProteoCast, un método computacional que aprovecha la historia de la propia evolución para predecir qué cambios de una sola letra en las proteínas probablemente tengan importancia, y demuestra que puede examinar prácticamente la colección completa de proteínas de un organismo a la vez.

Leyendo la huella de la evolución en las proteínas
ProteoCast se basa en una idea simple: si una posición concreta en una proteína apenas ha cambiado durante cientos de millones de años, alterarla hoy es más probable que sea perjudicial. Los autores introducen cada secuencia proteica de la mosca de la fruta en grandes bases de datos evolutivas para reunir proteínas relacionadas de muchas especies. Con estos datos, ProteoCast estima cuán disruptiva sería cada sustitución aminoacídica posible en cada posición, creando un “paisaje mutacional” para esa proteína. El método agrupa luego los cambios predichos en tres categorías intuitivas—neutro, de impacto leve o de impacto fuerte—y además etiqueta cada posición de la proteína como tolerante o sensible a la mutación.
Probando predicciones en todo un animal
El equipo aplicó ProteoCast a virtualmente todo el proteoma de la mosca de la fruta Drosophila melanogaster, cubriendo más de 22.000 formas proteicas y aproximadamente 300 millones de posibles mutaciones missense. Compararon las predicciones de ProteoCast con casi 400.000 variantes genéticas conocidas, incluyendo diferencias naturales observadas en poblaciones silvestres y endogámicas de moscas y mutaciones estudiadas experimentalmente que se sabe causan pérdida parcial de función o letalidad total. ProteoCast identificó correctamente alrededor del 85% de las mutaciones letales y el 73% de las de pérdida parcial como de impacto leve o fuerte, mientras clasificaba la gran mayoría de las variantes poblacionales como neutras. En otras palabras, el patrón de conservación evolutiva por sí solo resultó ser altamente informativo sobre qué cambios afectan la aptitud del organismo en su conjunto.
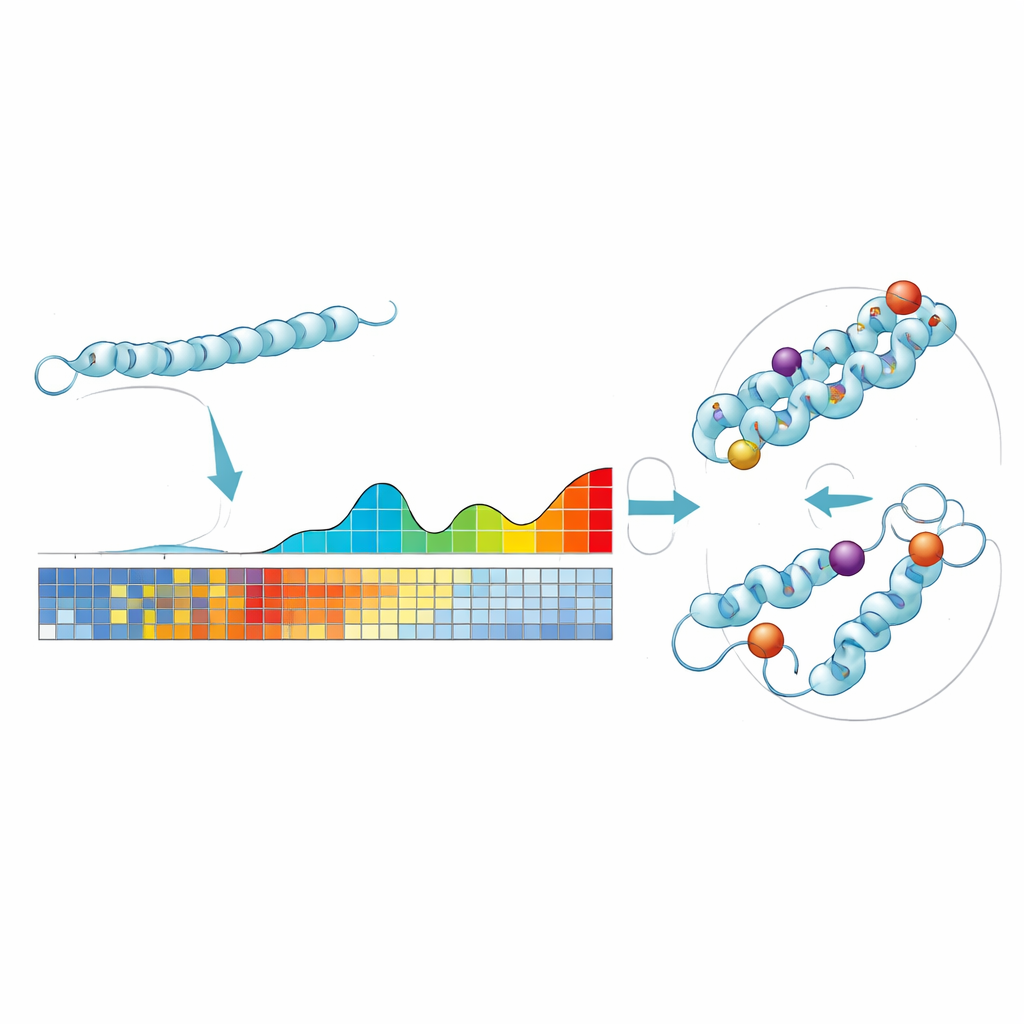
De las puntuaciones informáticas a la edición genómica real
Para ver si la salida de ProteoCast puede guiar experimentos, los autores la usaron para seleccionar cambios específicos de un solo aminoácido para la edición genómica dirigida en moscas. Se centraron en una enzima implicada en la producción de NAD, un cofactor metabólico clave. ProteoCast señaló varias sustituciones cercanas al sitio activo o a la interfaz de dímero como de fuerte impacto, y otras sustituciones en regiones superficiales como neutrales, incluso cuando cambiaban drásticamente la química o el tamaño del aminoácido. Cuando estas cinco mutaciones se introdujeron mediante CRISPR, las tres predichas como dañinas provocaron letalidad de desarrollo recesiva, mientras que las dos predichas como neutras dieron lugar a moscas sanas, coincidiendo con las previsiones computacionales.
Encontrando interruptores de control ocultos en regiones flexibles
Muchos sitios importantes de regulación en las proteínas se encuentran en regiones “no estructuradas” que se mueven libremente en lugar de formar formas 3D estables, lo que las hace difíciles de estudiar. ProteoCast proyecta sus puntuaciones de mutación en modelos 3D de AlphaFold y luego segmenta cada proteína en regiones de sensibilidad similar. Las regiones donde un conjunto de posiciones es inusualmente sensible suelen corresponder a motivos de unión o puntos calientes de modificaciones postraduccionales—interruptores de control sutiles que ajustan la actividad de una proteína. En el proteoma de la mosca, los segmentos de alta sensibilidad identificados por ProteoCast se solaparon con la mayoría de los motivos lineales cortos conocidos y con una gran fracción de sitios de modificación, y también resaltaron segmentos previamente no anotados que probablemente participan en regulación o interacciones proteína–proteína.
Impacto amplio más allá de las moscas de la fruta
Aunque el trabajo se centra en las moscas de la fruta, el principio detrás de ProteoCast es general: la evolución codifica información rica sobre qué posiciones en una proteína pueden cambiarse sin consecuencias y cuáles son críticas. Los autores muestran que el mismo marco funciona bien con variantes humanas asociadas a enfermedades y con conjuntos curados de sitios regulatorios de levadura y regiones de unión intrínsecamente desordenadas. Debido a que es rápido, escalable y no requiere hardware costoso, ProteoCast puede aplicarse a cualquier organismo con datos de secuencias proteicas. Para los no especialistas, el mensaje clave es que, dejando que la evolución actúe como experimentadora, ganamos un mapa a escala genómica de qué pequeños cambios genéticos tienen más probabilidad de importar para la salud, la enfermedad y las futuras terapias.
Cita: Abakarova, M., Freiberger, M.I., Liehrmann, A. et al. Proteome-wide prediction of the functional impact of missense variants with ProteoCast. Nat Commun 17, 3813 (2026). https://doi.org/10.1038/s41467-026-72140-1
Palabras clave: mutaciones missense, evolución de proteínas, Drosophila, predicción del efecto de variantes, genómica funcional