Clear Sky Science · it
Predizione su tutto il proteoma dell’impatto funzionale delle varianti missenso con ProteoCast
Perché piccole mutazioni contano per la salute e la malattia
Ogni essere umano porta in sé innumerevoli piccoli cambiamenti nel DNA, ma solo alcuni di questi alterano il funzionamento delle nostre proteine e contribuiscono alle malattie. Separare le differenze innocue da quelle pericolose è una sfida enorme, soprattutto ora che possiamo modificare i genomi con strumenti come CRISPR. Questo studio presenta ProteoCast, un metodo computazionale che sfrutta la storia stessa dell’evoluzione per predire quali cambiamenti di una singola lettera nelle proteine sono più probabili che abbiano effetti, e mostra che può analizzare praticamente l’intero repertorio proteico di un organismo in una sola volta.

Leggere l’impronta dell’evoluzione sulle proteine
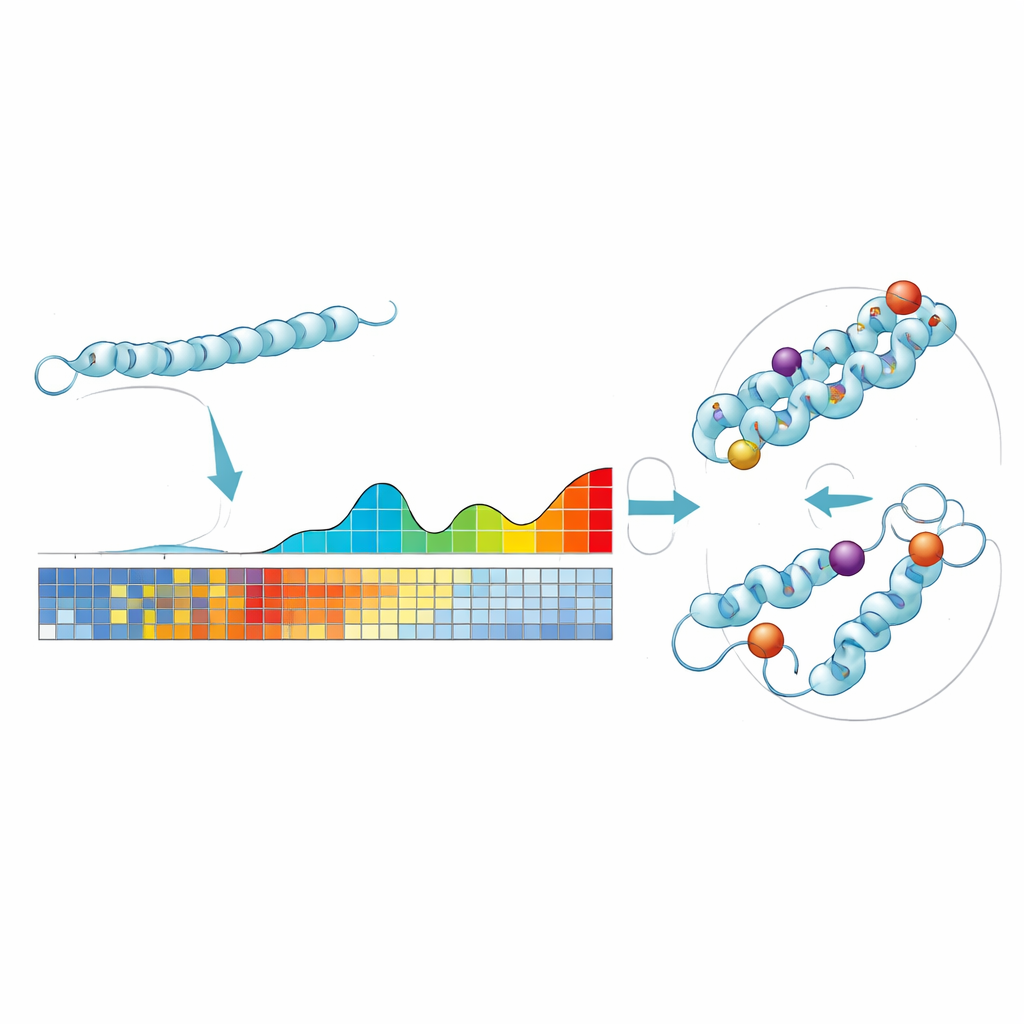
ProteoCast si basa su un’idea semplice: se una posizione particolare in una proteina è cambiata pochissimo in centinaia di milioni di anni, allora alterarla oggi è più probabile che sia dannoso. Gli autori inseriscono ogni sequenza proteica della mosca in grandi banche dati evolutive per raccogliere proteine correlate da molte specie. Usando queste informazioni, ProteoCast stima quanto sarebbe disruptive ogni possibile sostituzione amminoacidica in ogni posizione, creando un “paesaggio mutazionale” per quella proteina. Il metodo quindi raggruppa i cambiamenti previsti in tre categorie intuitive—neutrale, moderatamente impattante o fortemente impattante—e etichetta anche ogni posizione della proteina come tollerante o sensibile alla mutazione.
Mettere alla prova le predizioni su un intero animale
Il team ha applicato ProteoCast praticamente all’intero proteoma della mosca della frutta Drosophila melanogaster, coprendo oltre 22.000 forme proteiche e circa 300 milioni di possibili mutazioni missenso. Hanno confrontato le predizioni di ProteoCast con quasi 400.000 varianti genetiche note, incluse differenze naturali osservate in popolazioni selvatiche e allevate di mosche e mutazioni studiate sperimentalmente note per causare perdita parziale di funzione o letalità completa. ProteoCast ha correttamente segnalato circa l’85% delle mutazioni letali e il 73% delle mutazioni con perdita parziale come moderate o impattanti, classificando nel contempo la grande maggioranza delle varianti di popolazione come neutre. In altre parole, il pattern di conservazione evolutiva da solo si è rivelato altamente informativo su quali cambiamenti danneggiano il fitness dell’intero organismo.
Dai punteggi al computer agli interventi reali sul genoma
Per verificare se l’output di ProteoCast può guidare gli esperimenti, gli autori lo hanno usato per scegliere specifiche sostituzioni di singoli amminoacidi per editing mirato del genoma nelle mosche. Si sono concentrati su un enzima coinvolto nella produzione di NAD, un cofattore metabolico chiave. ProteoCast ha individuato diverse sostituzioni vicino al sito attivo dell’enzima o all’interfaccia di dimerizzazione come fortemente impattanti, e altre sostituzioni in regioni superficiali come neutre, anche quando cambiavano drasticamente la chimica o la dimensione dell’amminoacido. Quando queste cinque mutazioni sono state introdotte con CRISPR, le tre previste come dannose hanno causato letalità dello sviluppo in forma recessiva, mentre le due previste come neutre hanno prodotto mosche sane, in accordo con le previsioni computazionali.
Scoprire interruttori di controllo nascosti in regioni flessibili
Molti siti di regolazione importanti nelle proteine si trovano in regioni “non strutturate” che fluttuano piuttosto che formare forme 3D stabili, il che le rende difficili da studiare. ProteoCast mappa i suoi punteggi di mutazione su modelli 3D ottenuti da AlphaFold e segmenta ogni proteina in regioni di sensibilità simile. Le regioni in cui un gruppo di posizioni è insolitamente sensibile corrispondono spesso a motivi di legame o a hotspot di modificazioni post-traduzionali—interruttori di controllo sottili che modulano l’attività proteica. Nel proteoma della mosca, i segmenti ad alta sensibilità individuati da ProteoCast si sovrapponevano alla maggior parte dei noti short linear motifs e a una larga frazione dei siti di modificazione, ed evidenziavano anche segmenti precedentemente non annotati che probabilmente partecipano alla regolazione o alle interazioni proteina–proteina.
Impatto ampio oltre le mosche della frutta
Sebbene il lavoro sia incentrato sulle mosche della frutta, il principio alla base di ProteoCast è generale: l’evoluzione codifica informazioni ricche su quali posizioni in una proteina possono essere modificate senza conseguenze e quali sono critiche. Gli autori mostrano che lo stesso approccio funziona bene sulle varianti umane associate a malattie e su insiemi curati di siti regolatori di lievito e regioni disordinate intrinsecamente coinvolte nel binding. Poiché è rapido, scalabile e non richiede hardware costoso, ProteoCast può essere applicato a qualsiasi organismo con dati di sequenza proteica. Per i non specialisti, il messaggio chiave è che lasciando all’evoluzione il ruolo di sperimentatore otteniamo una mappa potente e genome‑wide di quali piccoli cambiamenti genetici sono più probabili che contino per la salute, le malattie e le terapie future.
Citazione: Abakarova, M., Freiberger, M.I., Liehrmann, A. et al. Proteome-wide prediction of the functional impact of missense variants with ProteoCast. Nat Commun 17, 3813 (2026). https://doi.org/10.1038/s41467-026-72140-1
Parole chiave: mutazioni missenso, evoluzione delle proteine, Drosophila, predizione dell’effetto delle varianti, genomica funzionale