Clear Sky Science · pt
Predição em todo o proteoma do impacto funcional de variantes missense com ProteoCast
Por que mutações minúsculas importam para a saúde e a doença
Cada pessoa carrega incontáveis pequenas alterações no DNA, mas apenas algumas dessas mudanças perturbam o funcionamento das proteínas e contribuem para doenças. Separar variações inofensivas daquelas perigosas é um enorme desafio, especialmente agora que podemos editar genomas com ferramentas como o CRISPR. Este estudo apresenta o ProteoCast, um método computacional que usa a própria história da evolução para prever quais mudanças de uma única letra nas proteínas têm maior probabilidade de importar, e demonstra que ele pode analisar basicamente o conjunto completo de proteínas de um organismo de uma só vez.

Lendo a impressão digital da evolução nas proteínas
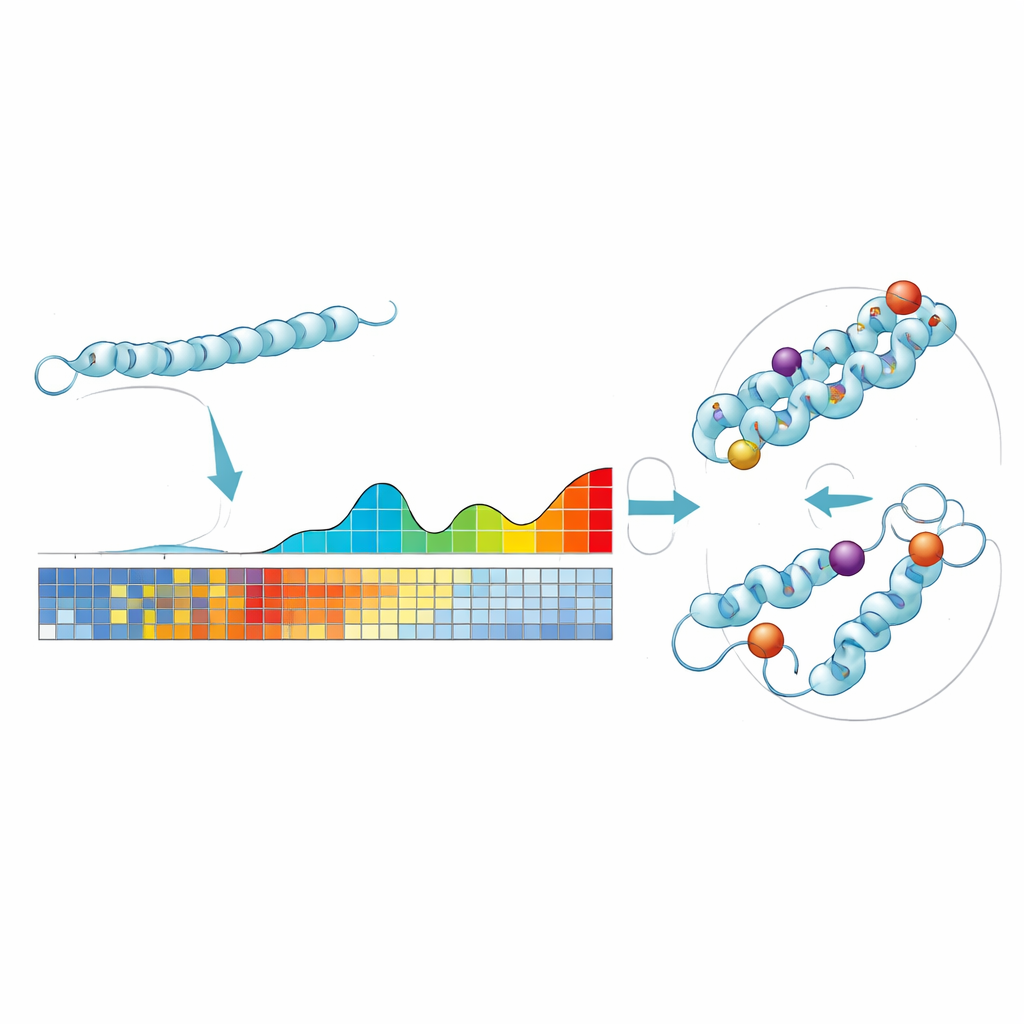
O ProteoCast parte de uma ideia simples: se uma posição específica em uma proteína mal mudou ao longo de centenas de milhões de anos, então alterá-la hoje tem maior probabilidade de ser prejudicial. Os autores inserem cada sequência proteica de mosca-das-frutas em grandes bancos de dados evolutivos para reunir proteínas relacionadas de muitas espécies. Usando esses dados, o ProteoCast estima quão disruptiva seria cada possível substituição de aminoácido em cada posição, criando uma “paisagem mutacional” para aquela proteína. O método então agrupa as mudanças previstas em três categorias intuitivas — neutra, de impacto leve ou de forte impacto — e também rotula cada posição da proteína como tolerante ou sensível à mutação.
Testando previsões em todo um animal
A equipe aplicou o ProteoCast virtualmente a todo o proteoma da mosca-das-frutas Drosophila melanogaster, cobrindo mais de 22.000 formas proteicas e cerca de 300 milhões de possíveis mutações missense. Compararam as previsões do ProteoCast com quase 400.000 variantes genéticas conhecidas, incluindo diferenças naturais observadas em populações selvagens e endogâmicas de moscas e mutações estudadas experimentalmente que causam perda de função parcial ou letalidade completa. O ProteoCast sinalizou corretamente cerca de 85% das mutações letais e 73% das mutações de perda parcial como de impacto leve ou forte, enquanto classificou a grande maioria das variantes populacionais como neutras. Em outras palavras, o padrão de conservação evolutiva por si só revelou-se altamente informativo sobre quais mudanças prejudicam a aptidão do organismo como um todo.
De escores computacionais à edição genômica na prática
Para verificar se a saída do ProteoCast pode orientar experimentos, os autores o usaram para selecionar mudanças específicas de um único aminoácido para edição genômica dirigida em moscas. Eles focaram em uma enzima envolvida na produção de NAD, um cofator metabólico chave. O ProteoCast destacou várias substituições próximas ao sítio ativo ou à interface de dímero da enzima como de forte impacto, e outras substituições em regiões de superfície como neutras, mesmo quando alteravam drasticamente a química ou o tamanho do aminoácido. Quando essas cinco mutações foram introduzidas por CRISPR, as três previstas como danosas causaram letalidade desenvolvimental recessiva, enquanto as duas previstas como neutras resultaram em moscas saudáveis, correspondendo às previsões computacionais.
Encontrando interruptores de controle ocultos em regiões flexíveis
Muitos sítios regulatórios importantes em proteínas estão em regiões “não estruturadas” que ficam flexíveis em vez de formar formas 3D estáveis, tornando-os difíceis de estudar. O ProteoCast mapeia seus escores de mutação em modelos 3D do AlphaFold e então segmenta cada proteína em regiões de sensibilidade semelhante. Regiões onde um aglomerado de posições é incomumente sensível frequentemente correspondem a motivos de ligação ou pontos de modificação pós‑traducional — interruptores de controle sutis que ajustam a atividade de uma proteína. No proteoma da mosca, os segmentos de alta sensibilidade do ProteoCast coincidiram com a maioria dos motivos lineares curtos conhecidos e com uma grande fração dos sítios de modificação, e também realçaram segmentos previamente não anotados que provavelmente participam da regulação ou de interações proteína–proteína.
Impacto amplo além das moscas-das-frutas
Embora o trabalho se concentre em moscas-das-frutas, o princípio por trás do ProteoCast é geral: a evolução codifica informação rica sobre quais posições em uma proteína podem ser alteradas sem consequências e quais são críticas. Os autores mostram que a mesma estrutura funciona bem em variantes humanas associadas a doenças e em conjuntos curados de sítios regulatórios de leveduras e regiões de ligação intrinsecamente desordenadas. Por ser rápido, escalável e não requerer hardware caro, o ProteoCast pode ser aplicado a qualquer organismo com dados de sequência proteica. Para não especialistas, a mensagem principal é que, ao deixar a evolução ser o experimentador, ganhamos um mapa genômico poderoso de quais pequenas mudanças genéticas têm maior probabilidade de importar para a saúde, a doença e futuras terapias.
Citação: Abakarova, M., Freiberger, M.I., Liehrmann, A. et al. Proteome-wide prediction of the functional impact of missense variants with ProteoCast. Nat Commun 17, 3813 (2026). https://doi.org/10.1038/s41467-026-72140-1
Palavras-chave: mutações missense, evolução proteica, Drosophila, predição de efeito de variantes, genômica funcional